
| A. | 碳化钙(CaC2)的电子式:Ca2+[:C::C:]2- | |
| B. | ${\;}_{8}^{18}$O2-离子的结构示意图: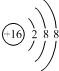 | |
| C. | 2-甲基-2-丙醇的结构简式: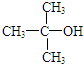 | |
| D. | Na2S水解的离子方程式:S2-+2H2O?2H2S+2OH- |
分析 A.碳化钙的电子式中,碳碳键应该为碳碳三键;
B. 为硫离子结构示意图,氧离子的核电荷数为8,核外电子总数为10;
为硫离子结构示意图,氧离子的核电荷数为8,核外电子总数为10;
C.2-甲基-2-丙醇的主链含有3个C,羟基和甲基都在2号C;
D.硫离子的水解分步进行,主要以第一步为主,其水解的离子方程式只写出第一步即可.
解答 解:A.碳化钙中的碳碳键应该为碳碳三键,其正确的电子式为: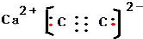 ,故A错误;
,故A错误;
B. 是硫离子结构示意图,氧离子的核电荷数应该为8,核外电子总数为10,氧离子正确的结构示意图为:
是硫离子结构示意图,氧离子的核电荷数应该为8,核外电子总数为10,氧离子正确的结构示意图为: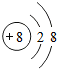 ,故B错误;
,故B错误;
C.2-甲基-2-丙醇分子中,羟基和甲基都处于2号C,其结构简式为: ,故C正确;
,故C正确;
D.硫离子水解主要以第一步为主,正确的离子方程式为:S2-+H2O?HS-+OH-,故D错误;
故选C.
点评 本题考查了常见化学用语的书写方法,题目难度中等,涉及结构简式、离子结构示意图、电子式及水解的离子方程式等知识,注意熟练掌握常见化学用语的概念及书写原则,试题培养了学生规范答题的能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 向氯化铝溶液中滴加过量氨水,生成白色胶状沉淀:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| B. | 加入足量的氢氧化镁以除去氯化镁溶液中的少量氯化铁:Fe3++3OH-═Fe(OH)3↓ | |
| C. | 常温下0.1mol/L 氯化铵溶液pH=5:NH4++H2O?NH3•H2O+H+ | |
| D. | 电解精炼铜时阳极铜溶解:Cu-2e-═Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
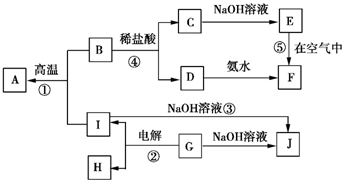 A~I分别表示中学化学中常见的一种物质,它们之间的相互关系如图所示(部分反应物、生成物没有列出),且A、B、C、D、E、F六种物质中均含同一种元素.
A~I分别表示中学化学中常见的一种物质,它们之间的相互关系如图所示(部分反应物、生成物没有列出),且A、B、C、D、E、F六种物质中均含同一种元素.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
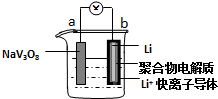
| A. | 放电时,该电池的总反应为:xLi+NaV3O8═NaLixV3O8 | |
| B. | 充电过程中Li+从阳极向阴极迁移 | |
| C. | 充电过程中阳极的电极反应式为NaLixV3O8-xe-═NaV3O8+xLi+,NaLixV3O8中钒的化合价发生变化 | |
| D. | 该电池可以用硫酸钠溶液作电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室里熔化氢氧化钠时,可选用石英坩埚和铁坩埚 | |
| B. | 不法商家制取的“地沟油”具有固定的熔沸点 | |
| C. | 食品保鲜膜按材质可分为聚乙烯(PE)、聚氯乙烯(PVC)、聚偏二氯乙烯(PVDC)等,PVC的单体可由PE的单体与氯化氢加成制得 | |
| D. | 家庭用食用醋代替CO2来增强漂白粉的漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
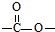 ”结构存在的同分异构体的数目有( )
”结构存在的同分异构体的数目有( )| A. | 2种 | B. | 4种 | C. | 6种 | D. | 8种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
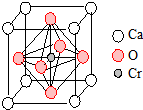 翡翠的主要成分为NaAlSi2O6,还含有其他多种金属阳离子,其中Cr3+的含量决定其绿色的深浅.
翡翠的主要成分为NaAlSi2O6,还含有其他多种金属阳离子,其中Cr3+的含量决定其绿色的深浅.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②④ | C. | ④⑥ | D. | ④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com