
| A.②→④→①→③→⑤ | B.②→①→③→④→⑤ |
| C.③→①→②→⑤→④ | D.①→③→⑤→②→④ |
 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.3-4-1-2 | B.1-2-4-3 | C.4-2-3-1 | D.3-4-2-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| | 实验操作 | 实验现象 | 实验结论 |
| 猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水 | _____________________ | 猜想a、c不成立,猜想b成立。 |
| 探究 | ①用带火星的木条伸入过氧化钠与水反应的试管中 | 木条复燃 | 生成物有___________ |
| ②往①试管内的溶液中滴加___________ ______________ | _____________________ | 生成物有氢氧化钠 |
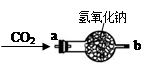
| 实验操作 | 实验现象 | 实验结论 |
| ①将CO2从a口处通入装置内,再把带火星的木条放在装置b口处 | 木条复燃 | CO2在常温下能与过氧化钠反应,该反应的化学方程式为: ____________________________ |
| ②取出充分反应后的固体生成物于试管中,往试管内滴加稀盐酸,将生成的氢气通入澄清石灰水中 | 有气泡产生 石灰水变浑浊 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
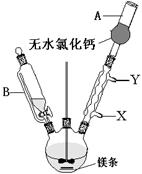
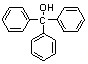 )是重要的有机合成中间体,实验室中合成三苯甲醇时采用图2所示的装置,其合成流程如图1所示。
)是重要的有机合成中间体,实验室中合成三苯甲醇时采用图2所示的装置,其合成流程如图1所示。
 (碱式溴化镁);
(碱式溴化镁);| 物质 | 熔点 | 沸点 | 溶解性 |
| 三苯甲醇 | 164.2℃ | 380℃ | 不溶于水,溶于乙醇、乙醚等有机溶剂 |
| 乙醚 | -116.3℃ | 34.6℃ | 微溶于水,溶于乙醇、苯等有机溶剂 |
| 溴苯 | -30.7°C | 156.2°C | 不溶于水,溶于乙醇、乙醚等多数有机溶剂 |
| 苯甲酸乙酯 | -34.6°C | 212.6°C | 不溶于水 |
| Mg(OH)Br | 常温下为固体 | 能溶于水,不溶于醇、醚等有机溶剂 | |


查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
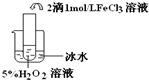
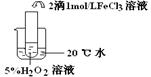
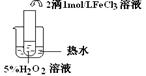
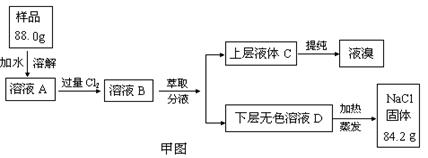
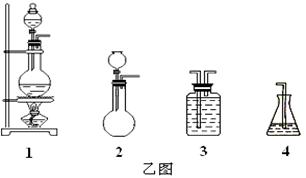
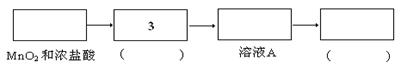
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
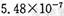 ,饱和亚硫酸中
,饱和亚硫酸中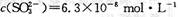 。
。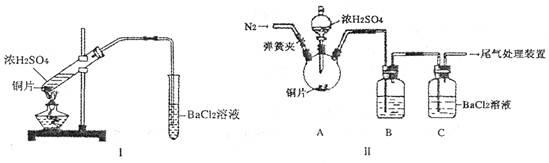
| A.NaOH溶液 | B.Na[Al(OH)4]溶液 | C.H2O2溶液 | D.酸性 KMnO4溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com