
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.40gNaOH中含有的共用电子对数为2NA
B.常温常压下,1.8g甲基(—CD3)中含有的中子数为0.9NA
C.31g白磷(![]() )含有共价键的总数为6NA
)含有共价键的总数为6NA
D.标况下,22.4LH2O中所含氢氧键的数目约为2NA
科目:高中化学 来源: 题型:
【题目】在0.1mol·L-1CH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO-+H+对于该平衡,下列叙述正确的是( )
CH3COO-+H+对于该平衡,下列叙述正确的是( )
A.加入水时,平衡向逆方向移动
B.加入少量NaOH固体,平衡向正方向移动
C.加入少量0.1mol·L-1HCl溶液,溶液中c(H+)不变
D.加入少量CH3COONa固体,平衡向正方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】熔融碳酸盐燃料电池的电解质为![]() 和
和![]() 的混合物,燃料为
的混合物,燃料为![]() ,氧化剂是含
,氧化剂是含![]() 的
的![]() ,两个电极均为惰性电极,在工作过程中,电解质熔融液的组成、相对浓度都不变。试回答:
,两个电极均为惰性电极,在工作过程中,电解质熔融液的组成、相对浓度都不变。试回答:
(1)负极的电极反应为________________;
(2)正极的电极反应为________________;
(3)工作时熔融液中的________________向负极移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰酸锂离子蓄电池是第二代锂离子动力电池。一种以软锰矿浆![]() 主要成分为MnO2,含少量Al2O3、Fe2O3、Fe2O、SiO2等杂质
主要成分为MnO2,含少量Al2O3、Fe2O3、Fe2O、SiO2等杂质![]() 为原料制备锰酸锂的流程如下图所示。
为原料制备锰酸锂的流程如下图所示。

⑴溶浸过程中,为提高SO2吸收率,可采取的措施有________![]() 填字母
填字母![]() 。
。
a.不断搅拌,使SO2和软锰矿浆充分接触 b. 增大通入SO2的速率
c. 减小软锰矿浆的进入量 d. 减小通入SO2的速率
⑵已知:室温下,Ksp[Al(OH)3] =1×10-33,Ksp[Fe(OH)3] =1×10-39,pH =7.1时Mn(OH)2开始沉淀。氧化除杂(室温)是除去MnSO4溶液中的Fe3+、Al3+(使其浓度小于1×10-6 mol·L-1),则需调节溶液pH的范围为________。
⑶硫酸锰与K2S2O8溶液在常温下混合一周,可慢慢得到球形二氧化锰(MnO2)。请写出发生反应的离子方程式:________。
⑷将MnO2和Li2CO3按物质的量4:1进行配料,充分搅拌,混合均匀然后升温至600~700℃,制取产品LiMn2O4。写出该反应的化学方程式:________。该反应中氧化剂为_______(填化学式)。
⑸锰酸锂可充电电池的总反应为Li1-xMn2O4 + LixC![]() LiMn2O4 + C(0 < x < 1)。
LiMn2O4 + C(0 < x < 1)。
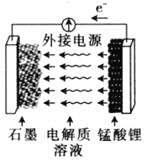
①充电时,电池的阳极反应式为________。
②废旧锰酸锂电池中可能残留单质锂,拆解不当易着火、爆炸,为了安全,拆解的注意事项是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年8月科学家在Science杂志首次报道了具有半导体特性的18个原子纯碳环分子(如图所示)。下列说法不正确的是
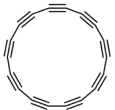
A.该分子属于有机物
B.该分子可能要比苯更加活泼
C.该分子所有的碳的杂化方式都是sp
D.该分子具有半导体的功能,可以使类似的直碳链成为分子级电子元件
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中充入![]() 和
和![]() ,压强为
,压强为![]() ,并在一定温度下使其发生反应
,并在一定温度下使其发生反应![]() 。下列说法正确的是( )
。下列说法正确的是( )
A.保持容器容积不变,向其中加入![]() ,化学反应速率不变
,化学反应速率不变
B.保持容器容积不变,向其中加入1molAr,化学反应速率增大
C.保持容器内压强不变,向其中加入1molAr,化学反应速率不变
D.保持容器内压强不变,向其中加入![]() ,化学反应速率将发生变化
,化学反应速率将发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组公司开发了Li-SO2Cl2军用电池,其示意图如图所示,已知电池反应为:2Li+SO2Cl2=2LiCl+SO2↑。下列叙述中错误的是
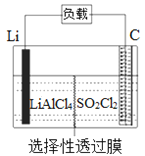
A. 电池工作时负极材料是Li,发生氧化反应
B. 将电解质溶液改为LiCl的水溶液,电池性能会更好
C. 电池工作时电子流向:锂电极→导线→负载→碳棒
D. 电池工作过程中,石墨电极反应式为SO2Cl2+2e=2Cl+SO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见无机物A、B、C、D存在如图转化关系:
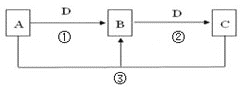
(1)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一![]() 遇空气会变色,则反应
遇空气会变色,则反应![]() 的化学方程式为_________________________________________________。
的化学方程式为_________________________________________________。
(2)若A为常见挥发性强酸,D是生产生活中用量最大用途最广的金属单质,则B的化学式是_____________________。
(3)若A、C、D都是常见气体,C是形成酸雨的主要气体,则A的电子式是____________。
(4)若A、B、C的水溶液均显碱性,焰色反应均为黄色,D为![]() ,举出C的一种用途_______________________。
,举出C的一种用途_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国工程院院士李兰娟团队,于 2020 年 2 月 4 日公布治疗新冠病毒感染的肺炎最新研究成果。他们初步测试发现,在体外细胞实验中,阿比朵尔在 10~30 微摩尔浓度 下,与药物未处理的对照组比较,能有效抑制冠状病毒达 60 倍,并有显著抑制病毒对细 胞的病变效应。 因此“阿比朵尔”成为抗击新型冠状病毒潜在用药,其合成路线如下:
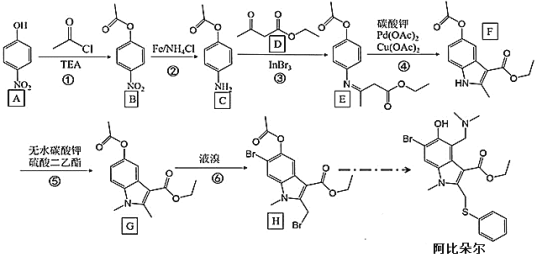
回答下列问题:
(1)有机物 A 的名称是____________。
(2)反应②、⑥反应类型分别是_________、______________。
(3)F 中含氧官能团的名称是_______________;G 的分子式为_______________。
(4)请写出反应③的化学反应方程式______________________________________。
(5)M 是 B 的一种同分异构体,满足下列条件的同分异构体有________种:①苯环上有3 个取代基;②能发生银镜反应;③能发生水解反应,且 1 mol M 水解消耗 4mol NaOH。其中核磁共振氢谱为有 4 组峰,峰面积之比为 2:2:2:1 的结构简式为_____。
(6)设计由甲苯和 2-丙醇为原料制备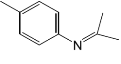 的合成路线_____。
的合成路线_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com