
| 乙同学正确 | 选用试剂 | 实验现象 |
| 第一种方法 | ||
| 第二种方法 |
分析 (1)根据Cl2单质溶于水变成黄色溶液,Fe2+被氧化成Fe3+使溶液变成黄色;
(2)Cl2氧化性较强,能将亚铁离子氧化为三价铁,三价铁在水溶液中是黄色的,可以从是否有Cl2以及是否生成三价铁两个角度来设计实验验证.
解答 解:(1)因Cl2单质溶于水变成黄色溶液,Fe2+被氧化成Fe3+使溶液变成黄色,
故答案为:Cl2;Fe3+;
(2)因Cl2氧化性较强,能将亚铁离子氧化为三价铁而使溶液变为黄色,可以进行试验看是否存在Cl2单质,也可以用硫氰化钾溶液检验三价铁的存在,
故答案为:
| 乙 同学正确 | 选用试剂 | 实验现象 |
| 第一种方法 | C | 有机层(下层)无色 |
| 第二种方法 | D | 溶液呈血红色 |
点评 本题考查物质的性质及氧化还原反应,为高频考点,把握氧化性的强弱及实验设计的能力为解答的关键,侧重分析与实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
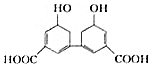 中国是中草药的发源地,目前中国大约有12000种药用植物.从某中草药提取的有机物有结构如图所示.下列说法正确的是( )
中国是中草药的发源地,目前中国大约有12000种药用植物.从某中草药提取的有机物有结构如图所示.下列说法正确的是( )| A. | 分子式为C14H18O4 | |
| B. | 环上氢原子的一氯取代物3种 | |
| C. | 1mol该有机物与足量的NaOH溶液反应最多消耗4molNaOH | |
| D. | 能发生酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
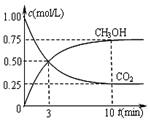 工业上以煤和水为原料通过一系列转化可变为清洁能源氢气或工业原料甲醇.
工业上以煤和水为原料通过一系列转化可变为清洁能源氢气或工业原料甲醇.| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应Ⅰ 恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应Ⅱ 绝热恒容 | 0min | 0 | 0 | 2 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Z为金属 | |
| B. | WY比WR稳定 | |
| C. | X的最高价氧化物对应的水化物为弱酸 | |
| D. | XR3是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH:②>③>④>① | B. | c(CH3COO-):②>④>③>① | ||
| C. | c(H+):①>③>②>④ | D. | c(CH3COOH):①>④>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
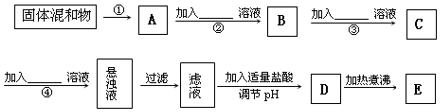
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
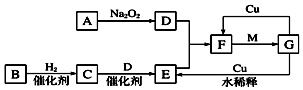
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com