
在反应3S+6KOH=2K2S+K2SO3+3H2O中,被还原的硫与被氧化的硫的质量比为( )。
A.2:1 B.1:2 C.3:1 D.1:3
科目:高中化学 来源: 题型:
随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了延长食品的保质期,防止食品受潮及富脂食品氧化变质,在包装袋中应放入的化学物质是( )
A.无水硫酸铜、蔗糖 B.食盐、硫酸亚铁
C.生石灰、硫酸亚铁 D.生石灰、食盐
查看答案和解析>>
科目:高中化学 来源: 题型:
已知胆矾溶于水时溶液温度降低,胆矾分解的热化学方程式为:
CuSO4•5H2O(s)=CuSO4(s)+5H2O(l) △H= +Q1 kJ/mol
室温下,若将1 mol无水硫酸铜溶解为溶液时放热Q2kJ,则( )
A.Q1>Q2 B.Q1=Q2 C.Q1<Q2 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。请回答:
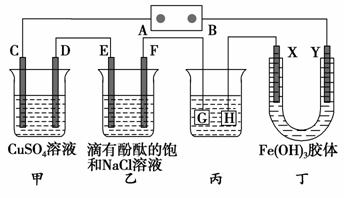
(1)B极是电源的________,一段时间后,甲中溶液颜色________,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明____________________,在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为______________。
(3)现用丙装置给铜件镀银,则H应该是________(填“镀层金属”或“镀件”),电镀液是________溶液。当乙中溶液的pH是13时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为________,甲中溶液的pH________(填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,不属于氧化还原反应的是( )。
A.2CO+O2 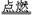 2CO2 B.CH4+2O2
2CO2 B.CH4+2O2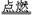 CO2+2H2O
CO2+2H2O
C.2KClO3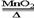 2KCl+3O2↑ D.2Fe(OH)3
2KCl+3O2↑ D.2Fe(OH)3 Fe2O3 +3H2O
Fe2O3 +3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,分别以高锰酸钾、氯酸钾、过氧化氢为原料制取氧气,当制得同温、同压下相同体积的氧气时,三个反应中转移的电子数之比为( )。
A.1 :1 :l B.2 :2 :1 C. 2 :3 :l D.4:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化铜有多种用途,如作玻璃着色剂、油类脱硫剂等。为获得纯净的氧化铜以探究其性质,某同学用工业硫酸铜(含硫酸亚铁等杂质)进行如 下实验:
下实验:
⑴制备氧化铜
工业CuSO4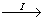
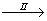 CuSO4溶液
CuSO4溶液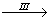 CuSO4·5H2O
CuSO4·5H2O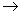 ……
…… CuO
CuO
①步骤Ⅰ的目的是除不溶性杂质,操作是:___________________________。
②步骤Ⅱ的目的是除铁,操作是:滴加H2O2溶液,稍加热;当Fe2+完全转化后, 慢慢加入Cu2(OH)2CO3粉末,搅拌,以控制pH =3.5;加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH =1。控制溶液pH =3.5的原因是: 。
慢慢加入Cu2(OH)2CO3粉末,搅拌,以控制pH =3.5;加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH =1。控制溶液pH =3.5的原因是: 。
③步骤Ⅲ的目的是得到CuSO4·5H2O固体,操作是: 、过滤、水浴加热烘干。水浴加热的特点是:_________________________________。
⑵探究氧化铜的性质
①取A、B两支试管,往A中加入适量的CuO粉末,再分别向A和B加入等体积3% H2O2溶液,只观察到A中有大量气泡,结论是:______________________。
②为探究试管A中的反应速率,收集气体并测定其体积必需的实验仪器有: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
等质量的①CH4、②H2、③HCl、④SO2,在标准状况下所占体积由大到小排列的顺序是
A ②>①>③>④ B ④>③>①>②
C ③>②>④>① D ①>④>②>③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com