
【题目】芳香烃化合物A(C9H12O)常用于药物及香料的合成,A的苯环上只有一个支链,支链上只有两种不同环境的氢原子,A有如下转化关系:

已知以下信息:
①
②![]()
请回答下列问题:
(1)A生成B的反应类型为________,由D生成E的反应条件为___________。
(2)F的官能团名称为________,_____________。
(3)I的结构简式为______________。
(4)由E生成F的反应方程式为________________。
(5)F有多种同分异构体,写出符合下列条件的同分异构体的结构简式为______________。
①能发生水解反应和银镜反应;
②属于芳香族化合物且分子中只有一个甲基;
③具有5个核磁共振氢谱峰
(6)糠叉丙酮(![]() )是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁醇(CH3)3COH]和糠醛(
)是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁醇(CH3)3COH]和糠醛(![]() )为原料制备糠叉丙酮的合成路线(无机试剂任用,用结构简式表示有机物),用箭头表示转化关系,箭头上往明试剂和反应条件)。_________________
)为原料制备糠叉丙酮的合成路线(无机试剂任用,用结构简式表示有机物),用箭头表示转化关系,箭头上往明试剂和反应条件)。_________________
【答案】 消去反应 NaOH水溶液、加热 羟基 醛基 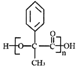
![]() 、
、![]()
![]()
【解析】芳香烃化合物A的分子式为C9H12O,A的苯环上只有一个支链,支链上只有两种不同环境的氢原子,所以A的结构简式为: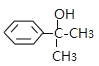 ;根据有机物B能与溴发生加成反应,有机物B含有不饱和键,所以A→B为消去反应生成烯烃,结构简式为
;根据有机物B能与溴发生加成反应,有机物B含有不饱和键,所以A→B为消去反应生成烯烃,结构简式为![]() (B);有机物D的结构简式为
(B);有机物D的结构简式为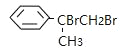 ,该有机物发生水解反应生成
,该有机物发生水解反应生成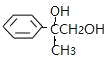 (E),有机物
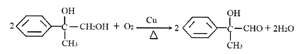
(E),有机物 发生催化氧化为
发生催化氧化为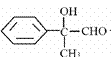 ( F),该有机物被银氨溶液氧化并酸化后为
( F),该有机物被银氨溶液氧化并酸化后为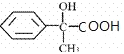 (H),H发生缩聚反应生成高分子(I),结构简式为
(H),H发生缩聚反应生成高分子(I),结构简式为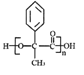 。
。
(1)根据以上分析, 生成
生成![]() 的反应类型为消去反应;
的反应类型为消去反应; 在NaOH水溶液、加热条件下生成
在NaOH水溶液、加热条件下生成 ;正确答案:消去反应;NaOH水溶液、加热。
;正确答案:消去反应;NaOH水溶液、加热。
(2)有机物F为 ,含有的官能团为羟基、 醛基;正确答案:羟基、 醛基。
,含有的官能团为羟基、 醛基;正确答案:羟基、 醛基。
(3) (H),H发生缩聚反应生成高分子(I),结构简式为
(H),H发生缩聚反应生成高分子(I),结构简式为 ;正确答案:
;正确答案: 。
。
(4)根据以上分析可知: 催化氧化为
催化氧化为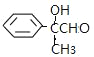 的反应方程式为
的反应方程式为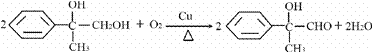 ;正确答案:
;正确答案: 。
。
(5) 的同分异构体,①能发生水解反应和银镜反应,说明是甲酸酯;②属于芳香族化合物且分子中只有一个甲基;③具有5个核磁共振氢谱峰,符合条件的同分异构体的结构简式为
的同分异构体,①能发生水解反应和银镜反应,说明是甲酸酯;②属于芳香族化合物且分子中只有一个甲基;③具有5个核磁共振氢谱峰,符合条件的同分异构体的结构简式为![]() 或
或![]() ;正确答案:
;正确答案:![]() 或
或![]() 。
。
(6)根据RCOCH3+R′CHO![]() RCOCH=CHR′,(CH3)3COH发生消去反应生成
RCOCH=CHR′,(CH3)3COH发生消去反应生成![]() ,
,![]() 再氧化为
再氧化为![]() ,
,![]() 与
与![]() 在一定条件下生成
在一定条件下生成![]() ,合成路线为:
,合成路线为:![]() ;正确答案:
;正确答案:![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列各组指定的元素,不能形成AB2型化合物的是( )
A.2s22p2 和2s22p4 B. 3s23p4 和2s22p4 C.3s2和2s22p5 D. 3s1和3s23p5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一张照片,一只可爱的小猫站在一块高分子合成材料上,下面是烈火灼烧,而小猫却若无其事。这说明此高分子材料一定具有的性质是
A. 良好的导热性 B. 良好的绝缘性 C. 良好绝热性 D. 熔点低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.铁是生产、生活及生命中的重要元素。
(1)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性能使血红蛋白丧失与O2结合能力。药品美蓝是其有效的解毒剂,解毒时美蓝发生_____反应(填“氧化”或“还原”)。
(2)现有一瓶放置了一段时间的某浓度的FeCl3溶液,请设计实验检验其中是否含有Fe3+_____。
(3)普通铁粉与水蒸气在高温下反应生成铁的某种氧化物和氢气,该氧化物和氢气在高温下发生逆反应得到“引火铁”。若一定量的普通铁粉和水蒸气在高温下反应生成44.8LH2(已换算到标况下),则转移电子数目为_______;“引火铁” 是一种极细的铁粉,它在空气中可以自燃,其原因是_____________。
II.化合物M是某种具有磁学性质的新型电子材料的主要成分,由两种元素组成。为了研究其组成,设计如下实验:
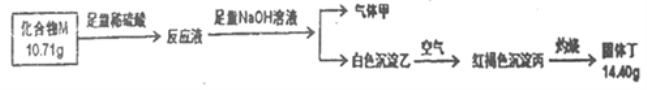
气体甲可使湿润红色石蕊试纸交蓝。请回答:
(1)M的化学式___________,气体甲的电子式__________。
(2)白色沉淀乙在空气中变成红褐色沉淀丙的原因是(用化学方程式表示)_______________。(3)高温条件下,丁与甲反应生成两种单质和水,该反应的化学方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铈(Ce)是镧系金属元素。空气污染物NO通常用含Ce4+的溶液吸收,生成HNO2、NO3ˉ,再利用电解法将上述吸收液中的HNO2转化为无毒物质,同时生成Ce4+,其原理如图所示。下列说法正确的是
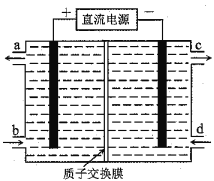
A. H+由右室进入左室
B. Ce4+从电解槽的c口流出,且可循环使用
C. 阴极的电极反应式:2HNO2+6H++6eˉ=N2↑+4H2O
D. 若用甲烷燃料电池作为电源,当消耗标准状况下33.6L甲烷时,理论上可转化HNO22mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【选做-选修3:物质结构与性质】硒化锌是一种半导体材料,回答下列问题。
(1)锌在周期表中的位置_______;Se基态原子价电子排布图为______。元素锌、硫和硒第一电离能较大的是________(填元素符号)。
(2)Na2SeO3分子中Se原子的杂化类型为_______;H2SeO4的酸性比H2SeO3强,原因是_______。
(3)气态SeO3分子的立体构型为_______;下列与SeO3互为等电子体的有__(填序号)。
A.CO32- B.NO3- C.NCl3 D.SO32-
(4)硒化锌的晶胞结构如图所示,图中X和Y点所堆积的原子均为______(填元素符号);该晶胞中硒原子所处空隙类型为_____(填“立方体”、“正四面体”或正八面体”);若该品晶胞密度为ρg/cm3,硒化锌的摩尔质量为Mg/mol。用NA代表阿伏加德罗常数的数值,则晶胞参数a为_______nm。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关煤的说法正确的是
A. 煤中含有苯、二甲苯、焦炉气
B. 煤的干馏是物理变化
C. 煤由有机物和少量无机物组成,煤的干馏是化学变化
D. 煤主要含有碳和氢两种元素,同时还含有少量的硫、氧、氮等元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com