
| A. | 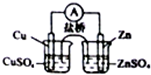 构成铜锌原电池 | B. | 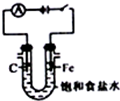 电解制氢气、氯气 | ||
| C. | 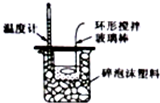 中和反应热量测定 | D. | 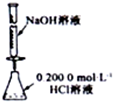 酸碱中和滴定 |
分析 A.构成Cu、Zn原电池;
B.Fe与电源正极相连,为阳极;
C.温度计测定反应液的温度;
D.NaOH与二氧化硅反应生成具有粘合性的硅酸钠.
解答 解:A.图中两个半反应构成Cu、Zn原电池,故A正确;
B.Fe与电源正极相连,为阳极,阳极Fe失去电子生成亚铁离子,不能得到氯气,故B错误;
C.温度计测定反应液的温度,图中温度计的位置不合理,故C错误;
D.NaOH与二氧化硅反应生成具有粘合性的硅酸钠,则NaOH应选碱式滴定管,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握原电池原理、电解原理、中和热测定及中和滴定实验是解本题关键,侧重分析与实验能力的考查,题目难度不大.


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案科目:高中化学 来源: 题型:选择题
| A. | 从试剂瓶中取出的任何药品,若药品有剩余都不能再放回原试剂瓶中 | |
| B. | 除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 | |
| C. | 用蒸发的方法,除去酒精溶液中少量的水分 | |
| D. | 用托盘天平称量25.20gNaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠常用于远途运输鱼苗的供氧 | |
| B. | 侯式制碱法的工艺过程中应用了物质的溶解性差异 | |
| C. | 加工后具有吸水性的植物纤维可用作食品干燥剂 | |
| D. | 使用含有钙离子浓度较大的地下水洗衣服,肥皂的去污能力减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
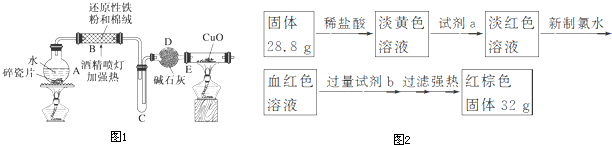
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属的电化学腐蚀比化学腐蚀更普遍 | |
| B. | 航海船船底四周镶嵌锌块保护船体,利用的是牺牲阳极保护法 | |
| C. | 用铝制铆钉连接铁板,铝钉易被腐蚀 | |
| D. | 原电池中电子由正扱流入负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 采用催化转化技术,可将汽车尾气中的一氧化碳和氮氧化物转化为无毒气体 | |
| B. | “雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮的氧化物无关 | |
| C. | 利用风能、太阳能等清洁能源代替化石燃料,可减少环境污染 | |
| D. | 氮化硅陶瓷是一种新型无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
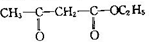 )和聚乙烯醇(PVA)都是重要的有机化工产品,其合成路线如图所示.
)和聚乙烯醇(PVA)都是重要的有机化工产品,其合成路线如图所示.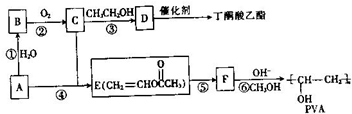
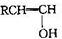 不稳定会自动转化为RCH2CHO.
不稳定会自动转化为RCH2CHO.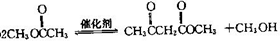
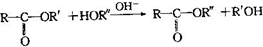
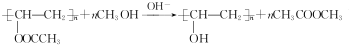 ,该反应的反应类型为取代反应.
,该反应的反应类型为取代反应.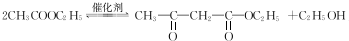 ,Na与生成的乙醇反应,平衡右移,提高D的转化率.(根据化学方程式和平衡移动原理回答)
,Na与生成的乙醇反应,平衡右移,提高D的转化率.(根据化学方程式和平衡移动原理回答) 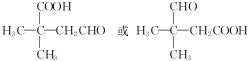 (填结构简式).
(填结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 编号 | 实验操作 | 实验现象 | 结论及解释 |
| 1 | 分别取4种溶液,滴加紫色石蕊溶液 | 溶液变红的是①④溶液 | 略 |
| 2 | 向含酚酞的NaOH溶液中,各滴加等量的②③两种溶液 | ②中无明显现象 ③中红色明显变浅 | 滴加③时反应的化学方程式: C6H5OH+NaOH→C6H5ONa+H2O |
| 3 | 配制等物质的量浓度的CH3COONa、NaHCO3溶液,并比较其pH | NaHCO3溶液pH大于CH3COONa溶液 | 略 |
| 4 | 将CO2通入C6H5ONa溶液中 | 产生白色浑浊 | 反应的化学方程式:C6H5ONa+CO2+H2O=C6H5OH+NaHCO3 |
| 结论:4种物质的羟基中的氢原子的活泼性由强到弱的顺序是(填序号)④①③② | |||
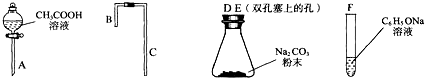
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
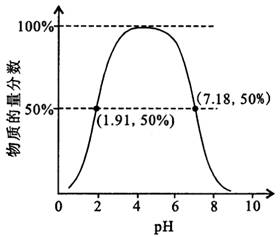
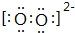 .
. 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com