
| ¢Ł | ¢Ś | ¢Ū | ¢Ü | ¢Ż | ¢Ž | ¢ß | ¢ą | |
| Ō×Ó°ė¾¶£Ø10-10m£© | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| ×īøß»ņ×īµĶ»ÆŗĻ¼Ū | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
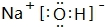 £®
£®·ÖĪö ¶ĢÖÜĘŚŌŖĖŲÖŠ£¬¢ŁĆ»ÓŠ×īøß¼Ū”¢Ö»ÓŠ×īµĶ¼Ū-2£¬æÉĶĘÖŖ¢ŁĪŖO£»¢Ū¢Ž¶¼ÓŠ×īøß¼Ū+1£¬“¦ÓŚ¢ńA×壬ĒŅ¢ŽµÄŌ×Ó°ė¾¶½Ļ“󣬢ŪµÄŌ×Ó°ė¾¶²»ŹĒĖłÓŠŌŖĖŲÖŠ×īŠ”µÄ£¬¹Ź¢ŪĪŖLi”¢¢ŽĪŖNa£»¢ŚÓŠ×īøß¼Ū+2£¬“¦ÓŚ¢ņA×壬Ō×Ó°ė¾¶“óÓŚLi£¬¹Ź¢ŚĪŖMg£»¢Ü¢ß¶¼ÓŠ×īøß¼Ū+5”¢×īµĶ¼Ū-3£¬“¦ÓŚ¢õA×壬ĒŅ¢ÜµÄŌ×Ó°ė¾¶½Ļ“󣬹Ź¢ÜĪŖP”¢¢ßĪŖN£»¢ŻÓŠ×īøß¼Ū+7”¢×īµĶ¼Ū-1£¬Ōņ¢ŻĪŖCl£»¢ąÖ»ÓŠ×īøß¼Ū+3£¬“¦ÓŚ¢óA×壬Ō×Ó°ė¾¶Š”ÓŚP£¬¹Ź¢ąĪŖB£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗ¶ĢÖÜĘŚŌŖĖŲÖŠ£¬¢ŁĆ»ÓŠ×īøß¼Ū”¢Ö»ÓŠ×īµĶ¼Ū-2£¬æÉĶĘÖŖ¢ŁĪŖO£»¢Ū¢Ž¶¼ÓŠ×īøß¼Ū+1£¬“¦ÓŚ¢ńA×壬ĒŅ¢ŽµÄŌ×Ó°ė¾¶½Ļ“󣬢ŪµÄŌ×Ó°ė¾¶²»ŹĒĖłÓŠŌŖĖŲÖŠ×īŠ”µÄ£¬¹Ź¢ŪĪŖLi”¢¢ŽĪŖNa£»¢ŚÓŠ×īøß¼Ū+2£¬“¦ÓŚ¢ņA×壬Ō×Ó°ė¾¶“óÓŚLi£¬¹Ź¢ŚĪŖMg£»¢Ü¢ß¶¼ÓŠ×īøß¼Ū+5”¢×īµĶ¼Ū-3£¬“¦ÓŚ¢õA×壬ĒŅ¢ÜµÄŌ×Ó°ė¾¶½Ļ“󣬹Ź¢ÜĪŖP”¢¢ßĪŖN£»¢ŻÓŠ×īøß¼Ū+7”¢×īµĶ¼Ū-1£¬Ōņ¢ŻĪŖCl£»¢ąÖ»ÓŠ×īøß¼Ū+3£¬“¦ÓŚ¢óA×壬Ō×Ó°ė¾¶Š”ÓŚP£¬¹Ź¢ąĪŖB£¬
£Ø1£©¢ŁĪŖOŌŖĖŲ£¬ŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆŹĒ£ŗµŚ¶žÖÜĘŚµŚVIA×壬¹Ź“š°øĪŖ£ŗµŚ¶žÖÜĘŚµŚVIA×壻
£Ø2£©ŌŚ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļÖŠ£¬ĖįŠŌ×īĒæµÄ»ÆŗĻĪļµÄ·Ö×ÓŹ½ŹĒHClO4£»¼īŠŌ×īĒæµÄ»ÆŗĻĪļĪŖNaOH£¬µē×ÓŹ½ŹĒ£ŗ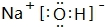 £¬¹Ź“š°øĪŖ£ŗHClO4£»
£¬¹Ź“š°øĪŖ£ŗHClO4£»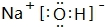 £»
£»
£Ø3£©¢ÜĪŖP”¢¢ßĪŖN£¬¶žÕßĶ¬Ö÷×壬µē×Ó²ćŌ½¶ą·Ē½šŹōŠŌŌ½Čõ£¬¹Ź·Ē½šŹōŠŌN£¾P£¬ŌņĒā»ÆĪļĪČ¶ØŠŌNH3£¾PH3£¬¹Ź“š°øĪŖ£ŗNH3£¾PH3£»
£Ø4£©¢ßµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļĪŖĻõĖį£¬ĖüµÄĒā»ÆĪļĪŖ°±Ęų£¬¶žÕß·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗNH3+HNO3=NH4NO3£¬¹Ź“š°øĪŖ£ŗNH3+HNO3=NH4NO3£»
£Ø5£©¢Ś×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļĪŖMg£ØOH£©2£¬¢ŻµÄĒā»ÆĪļĖ®ČÜŅŗĪŖŃĪĖį£¬¶žÕß·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖMg£ØOH£©2+2H+=Mg2++2H2O£¬¹Ź“š°øĪŖ£ŗMg£ØOH£©2+2H+=Mg2++2H2O£®
µćĘĄ ±¾Ģāæ¼²é½į¹¹ŠŌÖŹĪ»ÖĆ¹ŲĻµÓ¦ÓĆ£¬ÄѶČÖŠµČ£¬¹Ų¼üŹĒøł¾Ż»ÆŗĻ¼ŪÓėŌ×Ó°ė¾¶ĶʶĻŌŖĖŲ£¬×¢ŅāŌŖĖŲÖÜĘŚĀɵĥķ½āÕĘĪÕ£®


 Ļ°Ģā¾«Ń”ĻµĮŠ“š°ø
Ļ°Ģā¾«Ń”ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
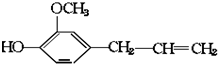 ĘäæÉÄܾßÓŠµÄŠŌÖŹŹĒ£Ø””””£©
ĘäæÉÄܾßÓŠµÄŠŌÖŹŹĒ£Ø””””£©| A£® | ¢Ś¢Ū | B£® | ¢Ł¢Ś¢Ū¢Ü | C£® | ¢Ł¢Ś¢Ū¢Ü¢Ż | D£® | ¢Ł¢Ś¢Ū¢Ż¢Ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SO2¼ČæÉŅŌŹĒŗ¬ĮņĪļÖŹµÄŃõ»Æ²śĪļ£¬ÓÖæÉŅŌŹĒŗ¬ĮņĪļÖŹµÄ»¹Ō²śĪļ | |
| B£® | SO2ŹĒĮņŌŚæÕĘųÖŠ²»ĶźČ«Č¼ÉյIJśĪļ£¬SO3ŹĒĮņŌŚæÕĘųÖŠĶźČ«Č¼ÉյIJśĪļ | |
| C£® | “óĘųÖŠSO2µÄÖ÷ŅŖĄ“Ō“ŹĒĘū³µÅųöµÄĪ²Ęų | |
| D£® | SO2¾ßÓŠĘư׊Ō£¬Ņņ¶ųæÉŅŌŹ¹ŹÆČļŹŌŅŗĶŹÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
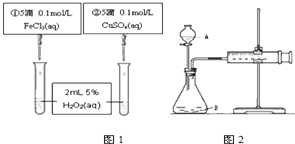
| A£® | Ķ¼1ŹµŃéæÉĶعż¹Ū²ģ²śÉśĘųÅŻæģĀżĄ“±Č½Ļ·“Ó¦ĖŁĀŹµÄ“óŠ” | |
| B£® | ČōĶ¼1ĖłŹ¾ŹµŃéÖŠ·“Ó¦ĖŁĀŹĪŖ¢Ł£¾¢Ś£¬ŌņŅ»¶ØĖµĆ÷Fe3+±ČCu2+¶ŌH2O2·Ö½ā“߻Ɗ§¹ūŗĆ | |
| C£® | ÓĆĶ¼2×°ÖĆæɲā¶Ø·“Ó¦²śÉśµÄĘųĢåĢå»ż | |
| D£® | ĪŖ¼ģ²éĶ¼2×°ÖƵÄĘųĆÜŠŌ£¬æɹŲ±ÕA“¦»īČū£¬½«×¢ÉäĘ÷»īČūĄ³öŅ»¶Ø¾ąĄė£¬Ņ»¶ĪŹ±¼äŗóĖÉæŖ»īČū£¬¹Ū²ģ»īČūŹĒ·ń»Ųµ½ŌĪ» |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĪŖ·ĄÖ¹ĢśÉśŠā£¬ŌŚĘä±ķĆęĶæŅ»²ć·ĄŠāÓĶĘį | |
| B£® | ĪŖ·ĄÖ¹»šŌÖ£¬ŌŚĆę·Ū³§”¢¼ÓÓĶÕ¾µČ³”ĖłŅŖŃĻ½ūŃĢ»š | |
| C£® | ĪŖ¼ÓæģH2O2µÄ·Ö½āĖŁĀŹ£¬°Ń·“ӦȯĘ÷·Åµ½ĄäĖ®ÖŠĄäČ“ | |
| D£® | ĪŖ¼ÓæģKClO3µÄ·Ö½āĖŁĀŹ£¬¼ÓČėMnO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 7 | B£® | 6 | C£® | 5 | D£® | 4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ļņ0.10mol•L-1NH4HCO3ČÜŅŗÖŠĶØČėCO2£ŗc£ØNH4+£©=c£ØHCO3-£©+c£ØCO32-£© | |
| B£® | 0.10mol•L-1CH3COONaČÜŅŗÖŠĶØČėHCl£ŗc£ØNa+£©£¾c£ØCl-£©£¾c£ØCH3COOH£© | |
| C£® | 0.10mol•L-1Na2SO3ČÜŅŗĶØČėSO2£ŗc£ØNa+£©=2[c£ØSO32-£©+c£ØHSO3-£©+c£ØH2SO3£©] | |
| D£® | Ļņ0.10mol•L-1NaHSO3ČÜŅŗÖŠĶØČėNH3£ŗc£ØNa+£©£¾c£ØSO32-£©£¾c£ØNH4+£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
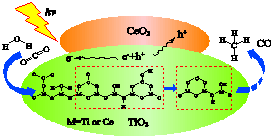 2016Äź3ŌĀŠĀ½®Ąķ»Æ¼¼ŹõŃŠ¾æĖłŹ×ĻČ·¢ĻÖ£ŗŌŚ¹ā”¢¼īŠŌCeO2ŠŽŹĪTiO2µÄø“ŗĻÄÉĆײÄĮĻµÄ“ß»Æ×÷ÓĆĻĀ£¬¶žŃõ»ÆĢ¼ŗĶĖ®æÉ×Ŗ»ÆĪŖ¼×ĶéŗĶŅ»Ńõ»ÆĢ¼£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
2016Äź3ŌĀŠĀ½®Ąķ»Æ¼¼ŹõŃŠ¾æĖłŹ×ĻČ·¢ĻÖ£ŗŌŚ¹ā”¢¼īŠŌCeO2ŠŽŹĪTiO2µÄø“ŗĻÄÉĆײÄĮĻµÄ“ß»Æ×÷ÓĆĻĀ£¬¶žŃõ»ÆĢ¼ŗĶĖ®æÉ×Ŗ»ÆĪŖ¼×ĶéŗĶŅ»Ńõ»ÆĢ¼£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | “Ė·“Ó¦æɽ«¹āÄÜ×Ŗ»ÆĪŖ»ÆѧÄÜ | |
| B£® | CO2ŗĶCH4¾łŗ¬¼«ŠŌ¹²¼Ū¼ü | |
| C£® | ²śĪļæÉÄÜ»¹ÓŠO2 | |
| D£® | CO2ČÜÓŚĖ®³ŹĖįŠŌµÄŌŅņ£ŗCO2+H2O?H2CO3H2CO3?2H++CO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓėĖ®Ļą±Č£¬AgClŌŚNa2CO3ČÜŅŗÖŠµÄČܽā¶Č¼°ČܶȻż¾łŌö“ó | |
| B£® | ·“Ó¦ŗóµÄČÜŅŗÖŠ£ŗc£ØNa+£©£¾c£ØCO32-£©£¾c£ØCl-£©=c£ØAg+£©£¾c£ØOH-£©£¾c£ØH+£© | |
| C£® | ČÜŅŗÖŠc£ØCl-£©=2”Į10-5mol•L-1 | |
| D£® | ³Įµķ×Ŗ»Æ·“Ó¦£»2AgCl£Øs£©+CO32-£Øaq£©?Ag2CO3£Øs£©+2Cl-£Øaq£©µÄĘ½ŗā³£ŹżĪŖ2”Į10-9 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com