
| A.NH4Cl | B.HNO3 | C.H2 | D.Na2O2 |
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源:不详 题型:单选题
| A.非金属原子间以共价键结合的物质一定是共价化合物 |
| B.含有共价键的化合物一定是共价化合物 |
| C.凡是能电离出离子的化合物一定是离子化合物 |
| D.凡是含有离子键的化合物一定是离子化合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.[Co(NH3)4 Cl2] Cl | B.[Co(NH3)3 Cl3] |
| C.[Co(NH3)6] Cl3 | D.[Cu(NH3)4]Cl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | Al | B | Be | C | Cl | F | Li |
| X的数值 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | N |
| X的数值 | | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 | |
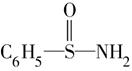 ,在S—N键,你认为该共用电子对偏向于________原子(填元素符号)。
,在S—N键,你认为该共用电子对偏向于________原子(填元素符号)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分子晶体中一定存在分子间作用力,不一定存在共价键 |
| B.含有极性键的分子一定是极性分子 |
| C.含有金属离子的晶体一定是离子晶体 |
| D.元素的非金属型越强,其单质的活泼型一定越强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
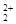 与互为等电子体,O22+的电子式可表示为 ;
与互为等电子体,O22+的电子式可表示为 ;查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.PH3分子中有未成键的孤对电子 | B.PH3是非极性分子 |
| C.它的分子构型是平面三角形 | D.磷原子采用sp2杂化方式 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氧元素的一种同位素 | B.臭氧的同素异形体 |
| C.一种新的氧化物 | D.一种新的化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com