
| A. | 洗涤沉淀时,应用玻璃棒轻轻搅拌,使得沉淀表面上的杂质溶于水中 | |
| B. | 将两块未擦去氧化膜的铝片分别投入1mol?L-1CuSO4溶液、1mol?L-1CuCl2溶液中,一段时间后,铝片表面都观察不到明显的反应现象 | |
| C. | 由锌、铜、稀硫酸构成的原电池溶液中加入适量的H2O2能提高电池的放电效率 | |
| D. | 在淀粉溶液中加入适量稀硫酸微热,再加少量新制氢氧化铜浊液加热,若无砖红色沉淀产生,则淀粉未发生水解 |
分析 A.洗涤沉淀,不能搅拌;
B.CuSO4和CuCl2溶液中铜离子水解,溶液显酸性,能先与氧化铝反应;
C.H2O2具有较强的氧化性,可在正极上得到电子;
D.葡萄糖和新制氢氧化铜悬浊液的反应必须在碱性条件下.
解答 解:A.洗涤沉淀的操作是将沉淀置于过滤器中,边加蒸馏水冲洗,但不能搅拌,故A错误;
B.CuSO4和CuCl2溶液中铜离子水解,溶液显酸性,能先与氧化铝反应,去除氧化膜后,活泼的铝与酸反应会产生气体,同时铝也置换出铜,有红色物质析出,故B错误;
C.Zn-Cu稀H2SO4构成的原电池,溶液中加入适量H2O2,氧化性的电极电位上升了,所以能提高电池放电效率,故C正确;
D.葡萄糖和新制氢氧化铜悬浊液的反应必须在碱性条件下,该实验中没有加入NaOH中和未反应的稀硫酸,所以实验不成功,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及沉淀洗涤、氧化铝的性质、原电池原理及物质检验,明确实验原理及物质性质是解本题关键,易错选项是D,注意该实验必须在碱性条件下进行,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①戊烷②丙烷③丁烷沸点高低顺序为①>③>② | |
| B. | CH4与Cl2以体积比1:4混合,光照时可制得纯净的CCl4 | |
| C. | 苯能在一定条件下跟H2加成生成环己烷 | |
| D. | CH2=CH2+H2O→CH3-CH2OH 是加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
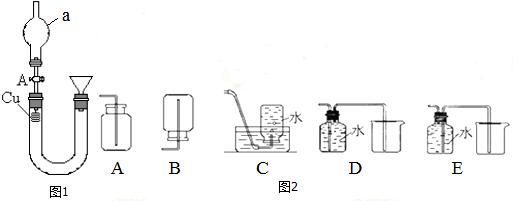
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 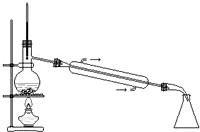 实验室中制取少量蒸馏水 | B. | 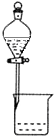 分离碘和酒精 | ||
| C. | 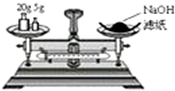 称量氢氧化钠固体 | D. |  配制100 mL 0.10 mol•L-1盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、OH-、NO${\;}_{3}^{-}$、Na+ | B. | K+、Cu2+、SO42-、Cl- | ||
| C. | Na+、K+、HCO3-、SO42- | D. | Mg2+、SO42-、Na+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 海水成分 | Na+ | Ca2+ | Mg2+ | HCO3- | Zn2+ |
| 含量/mol•L-1 | 0.4 | 0.002 | 0.045 | 0.002 | 10-7 |
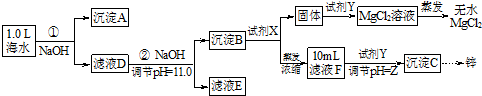
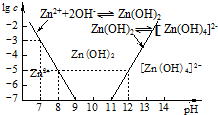
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
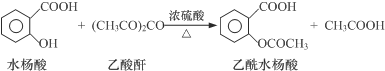
| 试剂 | 沸点(℃) | 溶解度 | 化学性质 |
| 水杨酸 | 211 | 微溶于冷水,易溶于热水 | |
| 乙酸酐 | 139 | 在水中逐渐分解 | |
| 乙酰水杨酸 | 微溶于水 | 与碳酸钠反应生成水溶性盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2LHF中含有H-F键的数目为0.5NA | |
| B. | 常温下,1.0L pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA | |
| C. | 常温下,56g铁片投入足量浓H2SO4中生成NA个SO2分子 | |
| D. | 电解饱和食盐水,阳极产生22.4L气体时,电路中通过的电子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Ba(0H)2溶液中滴H2SO4溶液至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| B. | 明矾溶液中加氢氧化钡溶液,使其产生沉淀的物质的量达最大值:Al3++2SO42-+2Ba+4OH-═2BaSO4↓+AlO2-+2H2O | |
| C. | Mg(HCO3)2溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+MgCO3↓ | |
| D. | 向100mL0.1mol/L的FeBr2溶液中通入0.012molCl2:10Fe2++14Br-+12Cl2═10Fe3++7Br2+24Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com