
 ��
��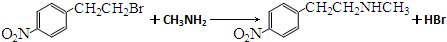 ��
�� ���������л���ѧ�ϳɵ��м��壬���������ϳ�F�IJ��ֲ��裬���һ���Ա�Ϊ��ʼԭ���Ʊ�����ͪ�ĺϳ�·��
���������л���ѧ�ϳɵ��м��壬���������ϳ�F�IJ��ֲ��裬���һ���Ա�Ϊ��ʼԭ���Ʊ�����ͪ�ĺϳ�·��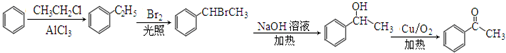 ��
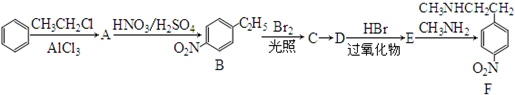
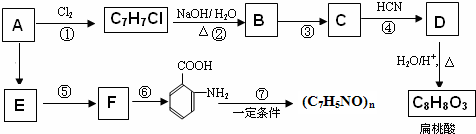
�� ���� ���������鷴Ӧ����A��A�����ᷢ����Ӧ����B������B�ṹ��ʽ֪������������ķ�ӦΪȡ����Ӧ����AΪ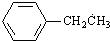 ����
����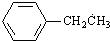 ����������Ӧ����B��C�ĺ˴Ź���������ʾ�����ַ壬�ҷ�������Ϊ2��2��1��3������B�����ڹ��������·���ȡ������CΪ
����������Ӧ����B��C�ĺ˴Ź���������ʾ�����ַ壬�ҷ�������Ϊ2��2��1��3������B�����ڹ��������·���ȡ������CΪ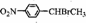 ��
��
C������Ӧ����D��D������Ϣ�ڵķ�Ӧ����E��E��Ӧ����F������F�ṹ��ʽ֪��
C������ȥ��Ӧ��DΪ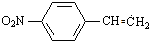 ��D���廯�ⷢ��������Ϣ���еļӳɷ�Ӧ����EΪ
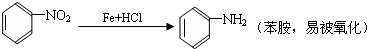
��D���廯�ⷢ��������Ϣ���еļӳɷ�Ӧ����EΪ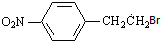 ��E��CH3NH2����ȡ������F��
��E��CH3NH2����ȡ������F��
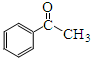
��5���Ա�Ϊ��ʼԭ���Ʊ�����ͪ�������ñ��������鷢��ȡ�������ұ����ұ����巢��ȡ�������屽���ټ���ˮ�⡢�����ɵñ���ͪ���ݴ˷������
��� �⣺���������鷴Ӧ����A��A�����ᷢ����Ӧ����B������B�ṹ��ʽ֪������������ķ�ӦΪȡ����Ӧ����AΪ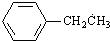 ����
����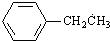 ����������Ӧ����B��C�ĺ˴Ź���������ʾ�����ַ壬�ҷ�������Ϊ2��2��1��3������B�����ڹ��������·���ȡ������CΪ
����������Ӧ����B��C�ĺ˴Ź���������ʾ�����ַ壬�ҷ�������Ϊ2��2��1��3������B�����ڹ��������·���ȡ������CΪ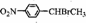 ��
��
C������Ӧ����D��D������Ϣ�ڵķ�Ӧ����E��E��Ӧ����F������F�ṹ��ʽ֪��
C������ȥ��Ӧ��DΪ ��D���廯�ⷢ��������Ϣ���еļӳɷ�Ӧ����EΪ
��D���廯�ⷢ��������Ϣ���еļӳɷ�Ӧ����EΪ ��E��CH3NH2����ȡ������F��
��E��CH3NH2����ȡ������F��
��1��ͨ�����Ϸ���֪����ת��ΪA�ķ�ӦΪȡ����Ӧ���ʴ�Ϊ��ȡ����Ӧ��
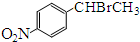
��2��C��D��±��������ȥ��Ӧ����Ҫ��������NaOH����Һ�����ȣ�DΪ ���Ǽ��к�������̼ԭ�ӣ����Բ�����˳���칹��C�Ľṹ��ʽΪ
���Ǽ��к�������̼ԭ�ӣ����Բ�����˳���칹��C�Ľṹ��ʽΪ ���ʴ�Ϊ��NaOH����Һ�����ȣ� �����ڣ�
���ʴ�Ϊ��NaOH����Һ�����ȣ� �����ڣ� ��
��
��3��E����ȡ����Ӧ����F����Ӧ����ʽΪ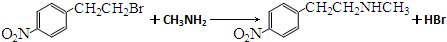 ���ʴ�Ϊ��
���ʴ�Ϊ��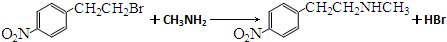 ��
��
��4�������ڷ����廯���˵�����б�����
�ڷ��ӽṹ��û�м������а�����
���ܷ���������Ӧ��ˮ�ⷴӦ��˵������ȩ����������������NaOH��Ӧ�����ʵ���֮��Ϊ1��2��˵����Ϊ���ᱽ����
ȡ����ΪHCOO-��-CH2NH2��
���ڼ�����ֽṹ��
�ʴ�Ϊ��3��
��5�����������鷢��ȡ����Ӧ�����ұ����ұ����巢��ȡ����Ӧ��Ȼ����ˮ�ⷴӦ���������������Ӧ���ɱ���ͪ���ϳ�·��Ϊ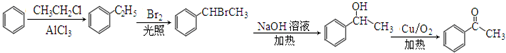 ���ʴ�Ϊ��
���ʴ�Ϊ��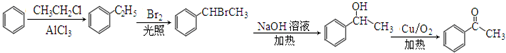 ��
��
���� ���⿼���л����ƶϺ��л���ϳɣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������ƶϼ�֪ʶ�ۺ��������������ݷ�Ӧǰ�����ʽṹ�仯��������Ϣ�����ƶϣ��ѵ��Ǻϳ�·����Ƽ�ͬ���칹�������жϣ���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ҵ�ƽ����ƣ���ⱥ��ʳ��ˮ | |
| B�� | ��ҵ��������Ҫ�õ���ԭ��������ʯ����̿����������ʯ�� | |
| C�� | ұ��þ������ˮ���Ȼ�þ������һ�������¼��ȵõ���ˮ�Ȼ�þ����������Ȼ�þ�����Եõ�����þ | |
| D�� | ���Ṥҵ�����������������£��ӽӴ��ҽ����������������в����ܺ���SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
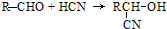
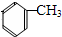 ��������
��������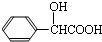 ��
�� ��
�� ��
��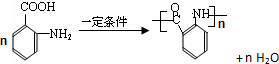 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
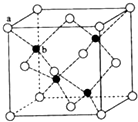 E��G��M��Q��T������ԭ���������������ǰ������Ԫ�أ�E��G��M��λ��P����ͬһ���ڵ�Ԫ�أ�M�ļ۲�����Ų�ΪNsnnp2n��E��Mԭ�Ӻ����δ�ɶԵ�������ȣ�QM2��GM2-Ϊ�ȵ����壻TΪ����Ԫ�أ���ԭ�Ӻ���û��δ�ɶԵ��ӣ���ش��������⣺
E��G��M��Q��T������ԭ���������������ǰ������Ԫ�أ�E��G��M��λ��P����ͬһ���ڵ�Ԫ�أ�M�ļ۲�����Ų�ΪNsnnp2n��E��Mԭ�Ӻ����δ�ɶԵ�������ȣ�QM2��GM2-Ϊ�ȵ����壻TΪ����Ԫ�أ���ԭ�Ӻ���û��δ�ɶԵ��ӣ���ش��������⣺ ��E��M�縺�����1.0���ɴ˿����ж�EMӦ��Ϊ���Խ�ǿ�ķ��ӣ���ʵ����EM���ӵļ��Լ������������ԭ��ӵ縺�Է�����CO�еĹ��õ��Ӷ�ƫ����ԭ�ӣ����������γ���λ���ĵ��Ӷ�������ԭ�ӵ������ṩ�ģ������˹��õ��Ӷ�ƫ��O�������ļ��ԣ�
��E��M�縺�����1.0���ɴ˿����ж�EMӦ��Ϊ���Խ�ǿ�ķ��ӣ���ʵ����EM���ӵļ��Լ������������ԭ��ӵ縺�Է�����CO�еĹ��õ��Ӷ�ƫ����ԭ�ӣ����������γ���λ���ĵ��Ӷ�������ԭ�ӵ������ṩ�ģ������˹��õ��Ӷ�ƫ��O�������ļ��ԣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
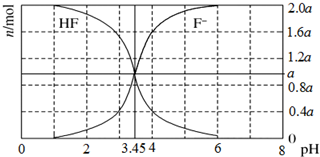 25��ʱ����2a mol/LNaOH��Һ�ζ�1.0L 2a mol/L�������Һ���õ����Һ��HF��F-�����ʵ�������ҺpH�ı仯��ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
25��ʱ����2a mol/LNaOH��Һ�ζ�1.0L 2a mol/L�������Һ���õ����Һ��HF��F-�����ʵ�������ҺpH�ı仯��ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | pH=3.45ʱ����Һ�У�c��Na+��+c��H+��=c��HF��+c��OH-�� | |
| B�� | pH=3ʱ����Һ�У�c��Na+����c��F-�� | |
| C�� | n��F-��=0.6a molʱ����Һ�У�c��Na+����c��HF�� | |
| D�� | pH=4ʱ����Һ�У�c��HF��+c��Na+��+c��H+��-c��OH-��=2a mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶�ɴ�С��˳��W��Y��Z��X | |
| B�� | ����̬�⻯����ȶ�����ǿ������˳��Y��Z��W | |
| C�� | �ڻ�����Y2X2��Z2X4�����к��еĹ��õ��Ӷ������ | |
| D�� | ��Ԫ��W��Y��Z�У�����������ˮ����������ǿ����W |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
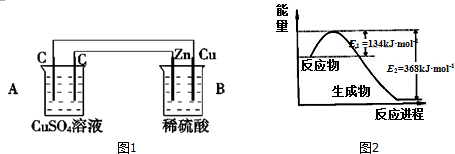
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 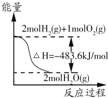 ��ʾ2 mol H2��g�������е�����һ����2 mol��̬ˮ�����е�������483.6 kJ | |
| B�� | 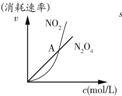 ��ʾ���º��������·����Ŀ��淴Ӧ2NO2��g��?N2O4��g���У������ʵ�Ũ��������������֮��Ĺ�ϵ�����н���A��Ӧ��״̬Ϊ��ѧƽ��״̬ | |
| C�� | 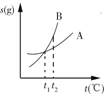 ��ʾA��B�����ʵ��ܽ�����¶ȱ仯�������t1��ʱ��A��B������Һ�ֱ�������t2��ʱ�����ʵ���������B��A | |
| D�� | 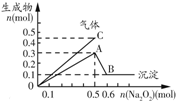 ��ʾ��һ������Mg2+��NH4+��Al3+�����Һ�м���Na2O2���������ɳ�������������Ĺ�ϵ�������Һ��n��Mg2+����n��NH4+����n��Al3+���ı�Ϊ1��2��2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com