
”¾ĢāÄæ”æĆĄ¹śŹ„Ā·Ņ×Ė¹“óѧъÖĘŠĀŠĶµÄŅŅ“¼Č¼ĮĻµē³Ų£¬ÓĆÖŹ×Ó£ØH+£©ČܼĮ£¬ŌŚ200”ę×óÓŅ¹©µē£®µē³Ų×Ü·“Ó¦ĪŖ£ŗC2H5OH+3O2”ś2CO2+3H2O£¬ČēĶ¼ŹĒøƵē³ŲµÄŹ¾ŅāĶ¼£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £© 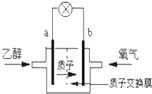
A.a¼«ĪŖµē³ŲµÄÕż¼«
B.µē³Ų¹¤×÷Ź±µēĮ÷ÓÉa¼«ŃŲµ¼Ļß¾µĘÅŻŌŁµ½b¼«
C.µē³ŲÕż¼«µÄµē¼«·“Ó¦ĪŖ£ŗ4H++O2+4e©ØT2H2O
D.µē³Ų¹¤×÷Ź±£¬1molŅŅ“¼±»Ńõ»ÆŹ±¾ĶÓŠ6molµē×Ó×ŖŅĘ
”¾“š°ø”æC
”¾½āĪö”æ½ā£ŗA£®Ōµē³Ų¹¤×÷Ź±£¬ŃōĄė×ÓĻņÕż¼«ŅĘ¶Æ£¬ŌņaĪŖøŗ¼«£¬¹ŹA“ķĪó£»
B£®µē³Ų¹¤×÷Ź±£¬µēĮ÷ÓÉÕż¼«¾ĶāµēĀ·Į÷Ļņøŗ¼«£¬ŌŚøƵē³ŲÖŠÓÉb¼«Į÷Ļņa¼«£¬¹ŹB“ķĪó£»
C£®Õż¼«ŃõĘųµĆµ½µē×Ó±»»¹Ō£¬µē¼«·“Ó¦Ź½ĪŖ4H++O2+4e©=2H2O£¬¹ŹCÕżČ·£»
D£®ŅŅ“¼ÖŠCŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ©2¼Ū£¬±»Ńõ»ÆŗóÉżøßµ½+4¼Ū£¬Ōņµē³Ų¹¤×÷Ź±£¬1molŅŅ“¼±»Ńõ»ÆŹ±¾ĶÓŠ12molµē×Ó×ŖŅĘ£¬¹ŹD“ķĪó£®
¹ŹŃ”C£®
ÓÉÖŹ×ÓµÄŅĘ¶Æ·½ĻņæÉÖŖaĪŖøŗ¼«£¬a¼«ÉĻŹĒŅŅ“¼Ź§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬ŅŅ“¼±»Ńõ»ÆÉś³ÉCO2ŗĶH+ £¬ µē¼«·“Ó¦Ź½ĪŖC2H5OH+3H2O©12e©ØT2CO2+12H+ £¬ bĪŖÕż¼«£¬·¢Éś»¹Ō·“Ó¦£¬µē¼«·½³ĢŹ½ĪŖ4H++O2+4e©ØT2H2O£¬ŅŌ“Ė½ā“šøĆĢā£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹÖŠ£¬²»ÄÜÓė½šŹōÄĘ·“Ó¦µÄŹĒ
A.ĀČĘųB.Ė®C.ŅŅ“¼D.ĆŗÓĶ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A.µā»ÆŅųæÉÓĆÓŚČĖ¹¤½µÓź
B.¹čĖįÄʵÄĖ®ČÜŅŗæÉÓĆÓŚ½ØÖžŠŠŅµµÄš¤ŗĻ¼Į
C.¾Ę¾«ŌŚŹµŃéĢØÉĻ×Å»šæÉÓĆĖ®×÷Ćš»š¼Į
D.Ą¶ĀĢŌåŌŚŃō¹ā×÷ÓĆĻĀæÉŹ¹Ė®·Ö½ā²śÉśĒāĘų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ²»ČÜÓŚĖ®ĒŅ±ČĖ®ĒįµÄŅ»×éŅŗĢåŹĒ£Ø £©
A.¼×±½”¢ĖÄĀČ»ÆĢ¼
B.±½”¢ĘūÓĶ
C.Ļõ»ł±½”¢Ņ»ĀȱūĶé
D.¾Ę¾«”¢äå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹĖłŗ¬Ō×ÓŹżÓɶąµ½ÉŁµÄĖ³ŠņŹĒ £Ø £©
¢Ł1.204”Į1024øöC ¢Ś0.7 mol NH3 ¢Ū1.204”Į1023øöÄĘŌ×Ó ¢Ü0.2 mol H2SO4 ¢Ż1mol He
A. ¢Ł¢Ū¢Ś¢Ü¢Ż B. ¢Ś¢Ł¢Ü¢Ż¢Ū C. ¢Ś¢Ü¢Ł¢Ż¢Ū D. ¢Ü¢Ż¢Ś¢Ł¢Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŃŠ¾æČ¼ĮĻµÄČ¼ÉÕŗĶ¶ŌĪŪČ¾ĘųĢå²śĪļµÄĪŽŗ¦»Æ“¦Ąķ£¬¶ŌÓŚ·ĄÖ¹“óĘųĪŪČ¾ÓŠÖŲŅŖŅāŅ壮
£Ø1£©½«Ćŗ×Ŗ»ÆĪŖĒå½ąĘųĢåČ¼ĮĻ£®ŅŃÖŖ£ŗ
2H2£Øg£©+O2£Øg£©ØT2H2O£Øg£©”÷H=©484.0kJmol©1£»
2C£Øs£©+O2£Øg£©ØT2CO£Øg£©”÷H=©220.0kJmol©1£»
Š“³ö½¹ĢæÓėĖ®ÕōĘų·“Ó¦ÖĘH2ŗĶCOµÄČČ»Æѧ·½³ĢŹ½
£Ø2£©ŅŃÖŖŅ»¶ØĪĀ¶ČŗĶŃ¹ĒæĻĀ£¬ÓÉH2ŗĶCO·“Ó¦ŗĻ³ÉÓÅÖŹČ¼ĮĻ¼×“¼£ŗ
CO£Øg£©+2H2£Øg£©CH3OH£Øg£©”÷H=©91kJmol©1
¢ŁŌŚĻąĶ¬Ģõ¼žĻĀŅŖĻėµĆµ½182kJČČĮ棬¼ÓČėø÷ĪļÖŹµÄĪļÖŹµÄĮææÉÄÜŹĒ
A£®2mol COŗĶ4mol H2 B£®2mol CO”¢4mol H2 ŗĶ1mol CH3OH£Øg£©
C£®4mol COŗĶ4mol H2 D£®4mol COŗĶ6mol H2
¢Ś½«1mol COŗĶ2mol H2³äČėŅ»ĆܱÕČŻĘ÷ÖŠ£¬±£³ÖŗćĪĀŗćŃ¹Ź±½ųŠŠ·“Ó¦£¬“ļµ½Ę½ŗāŹ±£¬²āµĆCOµÄ×Ŗ»ÆĀŹĪŖ20%£®ČōŌŚĻąĶ¬Ģõ¼žĻĀ£¬ĘšŹ¼Ź±ŌŚøĆČŻĘ÷ÖŠ³äČė1mol CH3OH£Øg£©£¬·“Ó¦“ļµ½Ę½ŗāŹ±µÄČČĮæ±ä»ÆŹĒ£ØĢī”°ĪüŹÕ”±»ņ”°·Å³ö”±£©kJČČĮ森
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĘū³µĪ²ĘųŹĒŌģ³ÉĪķö²ĢģĘųµÄŌŅņÖ®Ņ»£®
£Ø1£©Ęū³µĪ²ĘųÖŠŗ¬ÓŠCO”¢NO2µČÓŠ¶¾ĘųĢå¶ŌĘū³µ¼Ó×°Ī²Ęų¾»»Æ×°ÖĆæÉŹ¹ÓŠ¶¾ĘųĢåĻą»„·“Ó¦×Ŗ»ÆĪŖĪŽ¶¾ĘųĢ壮 Š“³öøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ £®
N2£Øg£©+2O2£Øg£©ØT2NO2£Øg£©”÷H=+68.0kJmol©1£»
2C£Øs£©+O2£Øg£©ØT2CO£Øg£©”÷H=©221.0kJmol©1£»
C£Øs£©+O2£Øg£©ØTCO2£Øg£©”÷H=©393.5kJmol©1
£Ø2£©Ęū³µĪ²ĘųÖŠŗ¬ÓŠCOŗĶH2O£Øg£©ŌŚŅ»¶ØĢõ¼žĻĀæÉŅŌ·¢Éś·“Ó¦
CO£Øg£©+H2O£Øg£©CO2£Øg£©+H2£Øg£©”÷H£¼0.850”ęŌŚĢå»żĪŖ10L·“Ó¦Ę÷ÖŠĶØČėŅ»¶ØĮæµÄCOŗĶH2O£Øg£©·¢ÉśÉĻŹö·“Ó¦COŗĶH2O£Øg£©µÄÅØ¶Č±ä»ÆČēĶ¼ĖłŹ¾Ōņ0©4minŹĒĘ½¾ł·“Ó¦ĖŁĀŹv£ØH2O£©=“ĖŹ±K= £®
ĘšŹ¼ĪļÖŹµÄĮæ | ¼× | ŅŅ | ±ū |
n£ØH2O£©/mol | 0.10 | 0.20 | 0.20 |
n£ØCO£©/mol | 0.10 | 0.10 | 0.20 |
850”ęŌŚ¼×”¢ŅŅ”¢±ūČżøö1LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ£¬ĘšŹ¼Ź±°“ÕÕ±ķ½ųŠŠĶ¶ĮĻ£¬“ļµ½Ę½ŗāדĢ¬£®Ę½ŗāŹ±¼×ČŻĘ÷ÖŠCOµÄ×Ŗ»ÆĀŹŹĒ £® ±Č½ĻĻĀĮŠČŻĘ÷ÖŠCOµÄ×Ŗ»ÆĀŹ¼×ŅŅ£ØĢī”°“óÓŚ”±”¢”°£¼”±»ņ”°µČÓŚ”±£©£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĘū³µĪ²ĘųŹĒŌģ³ÉĪķö²ĢģĘųµÄŌŅņÖ®Ņ»£®
£Ø1£©Ęū³µĪ²ĘųÖŠŗ¬ÓŠCO”¢NO2µČÓŠ¶¾ĘųĢå¶ŌĘū³µ¼Ó×°Ī²Ęų¾»»Æ×°ÖĆæÉŹ¹ÓŠ¶¾ĘųĢåĻą»„·“Ó¦×Ŗ»ÆĪŖĪŽ¶¾ĘųĢ壮 Š“³öøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ £®
N2£Øg£©+2O2£Øg£©ØT2NO2£Øg£©”÷H=+68.0kJmol©1£»
2C£Øs£©+O2£Øg£©ØT2CO£Øg£©”÷H=©221.0kJmol©1£»
C£Øs£©+O2£Øg£©ØTCO2£Øg£©”÷H=©393.5kJmol©1
£Ø2£©Ęū³µĪ²ĘųÖŠŗ¬ÓŠCOŗĶH2O£Øg£©ŌŚŅ»¶ØĢõ¼žĻĀæÉŅŌ·¢Éś·“Ó¦
CO£Øg£©+H2O£Øg£©CO2£Øg£©+H2£Øg£©”÷H£¼0.850”ęŌŚĢå»żĪŖ10L·“Ó¦Ę÷ÖŠĶØČėŅ»¶ØĮæµÄCOŗĶH2O£Øg£©·¢ÉśÉĻŹö·“Ó¦COŗĶH2O£Øg£©µÄÅØ¶Č±ä»ÆČēĶ¼ĖłŹ¾Ōņ0©4minŹĒĘ½¾ł·“Ó¦ĖŁĀŹv£ØH2O£©=“ĖŹ±K= £®
ĘšŹ¼ĪļÖŹµÄĮæ | ¼× | ŅŅ | ±ū |
n£ØH2O£©/mol | 0.10 | 0.20 | 0.20 |
n£ØCO£©/mol | 0.10 | 0.10 | 0.20 |
850”ęŌŚ¼×”¢ŅŅ”¢±ūČżøö1LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ£¬ĘšŹ¼Ź±°“ÕÕ±ķ½ųŠŠĶ¶ĮĻ£¬“ļµ½Ę½ŗāדĢ¬£®Ę½ŗāŹ±¼×ČŻĘ÷ÖŠCOµÄ×Ŗ»ÆĀŹŹĒ £® ±Č½ĻĻĀĮŠČŻĘ÷ÖŠCOµÄ×Ŗ»ÆĀŹ¼×ŅŅ£ØĢī”°“óÓŚ”±”¢”°£¼”±»ņ”°µČÓŚ”±£©£®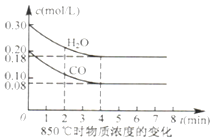
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ²éŌÄ׏ĮĻ·¢ĻÖ£¬½šŹōÄĘÄÜÓė¾Ę¾«ŌŚ³£ĪĀĻĀ·“Ó¦”£ŃŠ¾æŠŌѧĻ°Š”×éŅŖĢ½¾æ½šŹōÄĘÓė¾Ę¾«·“Ó¦ŅŌ¼°ĖüÓėĖ®·“Ó¦µÄŅģĶ¬µć£¬ĻĀĮŠŃŠ¾æ·½·ØÖŠĪŽŠčÓƵ½µÄŹĒ
A. ŹµŃé·Ø B. Ä£ŠĶ·Ø C. ¹Ū²ģ·Ø D. ±Č½Ļ·Ø
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com