
分析 (1)在氧化还原反应中,化合价升高数值=化合价降低数值=转移电子数,根据电子守恒配平化学方程式,化合价降低元素所在的反应物是氧化剂;
(2)①②A.H2O2+Ba(OH)2=BaO2+2H2O中各元素化合价不变,所以不属于氧化还原反应;
B.Ag2O+H2O2═2Ag+O2↑+H2O中Ag元素化合价由+1价变为0价、O元素化合价由-1价变为0价,所以氧化银是氧化剂、双氧水是还原剂;
C.2H2O2═2H2O+O2↑中O元素由-1价变为0价和-2价,所以双氧水是氧化剂和还原剂;
D.3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O中Cr元素化合价由+3价变为+6价、O元素化合价由-1价变为-2价,所以双氧水是氧化剂,硫酸铬为还原剂,据此分析①②解答;
③根据方程式Ag2O+H2O2=2Ag+O2↑+H2O中氧气计算;
④同一化学反应中,氧化剂的氧化性大于氧化产物的氧化性;
(3)除去KCl溶液和K2CO3的试剂是HCl,碳酸钾和HCl反应生成气体.
解答 解:(1)铁元素化合价从+2价升高到了+3价,升高了一价,氧气的化合价从0价降低到了-2价,生成一分子氧气,降低了4价,所以铁元素的前面乘以系数4,根据电荷守恒,氢离子前边是系数4,水前边系数是2,化合价降低元素是氧元素,所以O2是氧化剂,
故答案为:4;1;4;4;2;O2;
(2)A.H2O2+Ba(OH)2=BaO2+2H2O中各元素化合价不变,所以不属于氧化还原反应;
B.Ag2O+H2O2═2Ag+O2↑+H2O中Ag元素化合价由+1价变为0价、O元素化合价由-1价变为0价,所以氧化银是氧化剂、双氧水是还原剂;
C.2H2O2═2H2O+O2↑中O元素由-1价变为0价和-2价,所以双氧水是氧化剂和还原剂;
D.3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O中Cr元素化合价由+3价变为+6价、O元素化合价由-1价变为-2价,所以双氧水是氧化剂,硫酸铬为还原剂,
①H2O2仅体现氧化性的反应是D,故答案为:D;
②H2O2既体现氧化性又体现还原性的反应是C,故答案为:C;
③Ag元素化合价由+1价变为0价,化合价降低,故作Ag2O氧化剂被还原,
Ag2O+H2O2=2Ag+O2↑+H2O
232 22.4
m 11.2
$\frac{232}{m}=\frac{22.4}{11.2}$,m=116,故答案为:116;
④反应Ag2O+H2O2=2Ag+O2↑+H2O中,氧化银做氧化剂,双氧水作还原剂,则氧化性Ag2O>H2O2,反应3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O中,双氧水做氧化剂,铬酸钾做氧化产物,则氧化性H2O2>K2CrO4,故氧化性顺序为:Ag2O>H2O2>K2CrO4,故答案为:Ag2O>H2O2>K2CrO4;
(3)除去KCl溶液和K2CO3的试剂是盐酸,碳酸钾和HCl反应生成气体,离子方程式为CO32-+2H+=CO2↑+H2O,故答案为:CO32-+2H+=CO2↑+H2O.
点评 本题考查氧化还原反应,题目难度不大,注意从元素化合价的角度进行判断,把握氧化还原反应的特征和实质,注意元素化合价的变化.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年四川省高一上10月月考化学试卷(解析版) 题型:选择题
将溶质的质量分数为a%、物质的量浓度为c1 mol·L-1的稀硫酸加热蒸发掉一定量的水,使溶质的质量分数变为2a%,此时硫酸的物质的量浓度为c2 mol·L-1,则c1和c2的关系是( )
A.c2=2c1 B.c2>2c1 C.c2<2cl D.c1=2c2
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20mL 3mol•L-1Na2S2O3的溶液 | B. | 20mL 2mol•L-1Na2S2O3的溶液 | ||
| C. | 10mL 4mol•L-1Na2S2O3的溶液 | D. | 10mL 2mol•L-1Na2S2O3的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5s时,正、逆反应速率都达到最大 | |
| B. | 前5s内平均反应速率υ(Y)=0.1 mol/( L•s) | |
| C. | 达平衡时,各物质的浓度都保持不变,反应停止 | |
| D. | 升高温度,测得容器中密度不变时,表示该反应已经达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
 H++HA-,该滚液中由水电离出的c(H+)=10-10mol/L.
H++HA-,该滚液中由水电离出的c(H+)=10-10mol/L.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应①中,氧化剂与还原剂的物质的量之比为2:5 | |
| B. | 反应②中,Cu3P既是氧化产物又是还原产物 | |
| C. | 反应②中,当有5mol CuSO4发生反应时,共转移电子10mol | |
| D. | 反应①中CuSO4做氧化剂,反应②中CuSO4作还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
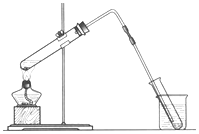 海洋是巨大的资源宝库,从海洋中可获得淡水、单质碘、食盐等物质.
海洋是巨大的资源宝库,从海洋中可获得淡水、单质碘、食盐等物质.| 杂质 | CaCl2 | MgCl2 | Na2SO4 |
| 除杂试剂 | Na2CO3 | NaOH | BaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入过量Cl2:Cl-、Fe2+、SO42-、Al3+ | |
| B. | 加入过量NaOH溶液:Na+、AlO2-、SO42-、OH- | |
| C. | 加入过量氨水:Na+、NH4+、SO42-、AlO2- | |
| D. | 加入过量铜粉:NO3-、Fe3+、SO42-、Al3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com