
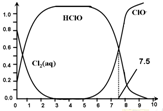
 氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强,25℃时氯气-氯水体系中存在以下平衡关系:
氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强,25℃时氯气-氯水体系中存在以下平衡关系:| A、Cl2(g)+H2O?2H++ClO-+Cl- K=10-10.9 |
| B、在氯处理水体系中,c(HClO)+c(ClO-)=c(H+)-c(OH-) |
| C、用氯处理饮用水时,pH=7.5时杀菌效果比pH=6.5时差 |
| D、氯处理饮用水时,在夏季的杀菌效果比在冬季好 |
| c(H+)c(ClO-) |
| c(HClO) |
| 10-7.5×c(ClO-) |
| c(HClO) |
| c(H+)c(ClO-) |
| c(HClO) |
| 10-7.5×c(ClO-) |
| c(HClO) |


科目:高中化学 来源: 题型:
| 城市 | 污染 指数 |
首要 污染物 |
空气质 量级别 |
城市 | 污染 指数 |
首要 污染物 |
空气质 量级别 |
| 北京 | 92 | TSP | Ⅱ | 济南 | 76 | TSP | Ⅱ |
| 天津 | 82 | TSP | Ⅱ | 武汉 | 83 | NOx | Ⅱ |
| 长春 | 103 | TSP | Ⅲ | 深圳 | 77 | NOx | Ⅱ |
| 上海 | 74 | NOx | Ⅱ | 汕头 | 54 | Ⅱ | |
| 杭州 | 67 | TSP | Ⅱ | 成都 | 87 | TSP | Ⅱ |
| 福州 | 42 | Ⅰ | 重庆 | 98 | SO2 | Ⅱ | |
| 厦门 | 25 | Ⅰ | 贵阳 | 69 | TSP | Ⅱ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、④⑤③ | B、⑥①⑤② |
| C、⑥①⑤③ | D、⑧②⑤③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溴化钠只有一部分反应,氟化钠未反应 |
| B、氟化银溶于水 |
| C、沉淀是氟化银 |
| D、沉淀是氟化银与溴化银的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验目的 | 实验方案 |
| A | 检验CH3CH2Br在NaOH溶液中是否发生水解 | 将CH3CH2Br与NaOH溶液共热.冷却后,取出上层水溶液,用稀HNO3酸化,加入AgNO3溶液,观察是否产生淡黄色沉淀 |
| B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
| C | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置.可观察到下层液体呈紫色 |
| D | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
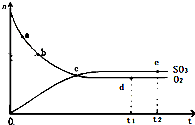 对于密闭容器中的反应:2SO2(g)+O2(g)?2SO3(g)△H<0,450℃时,n(SO3)和n(O2)随时间的变化关系如图所示,下列说法正确的是( )
对于密闭容器中的反应:2SO2(g)+O2(g)?2SO3(g)△H<0,450℃时,n(SO3)和n(O2)随时间的变化关系如图所示,下列说法正确的是( )| A、点c处反应达到平衡 |
| B、点a的正反应速率比点b的大 |
| C、点d(t1时刻)和点e(t2时刻)处n(SO2)不一样 |
| D、其他条件不变,600℃时反应至t1时刻,n(SO3)比上图中的d点值要大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 氢氧化钠溶液 | 分液 |
| B | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| C | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 蒸馏 |
| D | 乙炔(硫化氢) | 硫酸铜 | 洗气 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
| Cl2 |
| 460℃ |
| 蒸馏 |
| H2 |
| 1100℃ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com