
(16分)实验室中以粗铜(含杂质)为原料,某种制备铜的氯化物的流程如下:
按要求回答下列问题:
(1)操作①的所用到的玻璃仪器有______________。
(2)上述流程中,所得固体1需要加稀盐酸溶解,其理由是 ;
溶液1可加试剂X用于调节pH以除去杂质, X可选用下列试剂中的(填序号)___________。
A.NaOH B.NH3·H2O C.CuO D.CuSO4
(3)反应②是向溶液2中通入一定量的SO2,加热一段时间后生成CuCl白色沉淀。写出
制备CuCl的离子方程式: 。
(4)现用如图所示的实验仪器及药品来制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹省略)。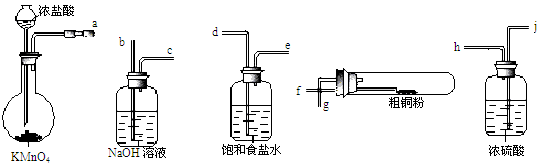
①按气流方向连接各仪器接口顺序是:a→ 、 → 、 → 、 → 。实验中大试管加热前要进行一步重要操作,其操作是 。
②反应时,盛粗铜粉的试管中的现象是 。
(5)在溶液2转化为CuCl2·2H2O的操作过程中,发现溶液颜色由蓝色变为绿色。小组同学欲探究其原因。已知:氯化铜溶液中有如下转化关系:
Cu(H2O)42+(aq) + 4Cl-(aq)  CuCl42-(aq) + 4 H2O (l)
CuCl42-(aq) + 4 H2O (l)
蓝色 绿色
该同学取氯化铜晶体配成蓝绿色溶液Y,进行如下实验,其中能证明溶液中有上述转化关系的是 (填序号)。
A.将Y稀释,发现溶液呈蓝色 B.在Y中加入CuCl2晶体,溶液变为绿色
C.在Y中加入NaCl固体,溶液变为绿色 D.取Y进行电解,溶液颜色最终消失
(1)漏斗、烧杯、玻璃棒;(2)抑制氯化铜、氯化铁水解;C D;
(3)SO2+2H2O+2Cu2++2Cl-=2CuCl+SO42-+4H+;
(4)①dehifgb;通入一段时间的氯气,将装置中的空气排尽;②产生大量棕黄色的烟;(5)ABC
解析试题分析:(1)操作①是过滤。所用到的玻璃仪器有漏斗、烧杯、玻璃棒;(2)Cu与Cl2反应得到CuCl2,杂质也与氯气反应得到金属氯化物。CuCl2是强酸弱碱盐,容易水解,为了抑制氯化铜、氯化铁水解溶解固体在稀盐酸的环境中。溶液1的主要成分是CuCl2,若加试剂X用于调节pH以除去杂质, X应该是含有Cu2+的物质。选项为CD。(3)根据题意结合电子守恒、电荷守恒及原子守恒可得方程式:SO2+2H2O+2Cu2++2Cl-=2CuCl+SO42-+4H+;(4)①要经过制取气体、除去杂质、气体干燥、发生反应、尾气处理等实验步骤。按气流方向连接各仪器接口顺序是:a→d→e→h→i→f→g→b。实验中大试管加热前要进行一步重要操作,其操作是通入一段时间的氯气,将装置中的空气排尽再进行实验,否则Cu会被氧化为CuO;②在大试管发生反应:Cu+ Cl2 CuCl2,盛粗铜粉的试管中的现象是产生大量棕黄色的烟;(5)A.将Y稀释,即加入水,若存在上述平衡,则增大了水的浓度,平衡逆向移动,产生更多的蓝色的Cu(H2O)42+(aq)。正确。 B.在Y中加入CuCl2晶体,即增大了c(Cl-)的浓度,平衡正向移动,绿色的CuCl42-(aq)的浓度增大。溶液变为绿色。正确。C.在Y中加入NaCl固体,c(Cl-)的浓度增大,平衡正向移动,绿色的CuCl42-(aq)的浓度增大,溶液变为绿色。正确。D.取Y进行电解,溶液颜色最终消失,这与是哪种结合方式无关。错误。
CuCl2,盛粗铜粉的试管中的现象是产生大量棕黄色的烟;(5)A.将Y稀释,即加入水,若存在上述平衡,则增大了水的浓度,平衡逆向移动,产生更多的蓝色的Cu(H2O)42+(aq)。正确。 B.在Y中加入CuCl2晶体,即增大了c(Cl-)的浓度,平衡正向移动,绿色的CuCl42-(aq)的浓度增大。溶液变为绿色。正确。C.在Y中加入NaCl固体,c(Cl-)的浓度增大,平衡正向移动,绿色的CuCl42-(aq)的浓度增大,溶液变为绿色。正确。D.取Y进行电解,溶液颜色最终消失,这与是哪种结合方式无关。错误。
考点:考查混合物的分离、有气体参加的化学反应的所以步骤、盐的水解、离子方程式的书写等知识。


科目:高中化学 来源: 题型:单选题
下列反应的离子方程式中,书写正确的是
| A.氯气溶于水:H2O + C12=2H+ + ClO- + Cl- |
| B.将铝粉投入氢氧化钠溶液中:2Al + 2OH-=2AlO2- + H2↑ |
| C.铁粉与氯化铁溶液反应:Fe + Fe3+=2Fe2+ |
| D.过氧化钠与水反应:2Na 2O2+ 2H2O=4Na+ + 4OH-+ O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(11分)含有下列离子的五种溶液①Ag+②Mg2+③Fe2+④Al3+⑤Fe3+试回答下列问题:
(1)既能被氧化又能被还原的离子是____________(填离子符号,下同)
(2)向③中加入NaOH溶液,现象是 有关反应的离子方程式或化学方程式为 。
(3)加入过量NaOH溶液无沉淀的是_____________
(4)加铁粉溶液质量增重的是_________,溶液质量减轻的___________
(5)遇KSCN溶液呈红色的是_________________________
(6)能用来鉴别Cl–存在的离子是___________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(15分)实验探究是学习化学的一个重要方法,某实验小组的同学利用下列装置完成一些常见气体制备以及相关物质性质探究(夹持装置及连接橡胶管已省略,其中装置E有多个供使用)。
可供选择的液体试剂及固体药品:
| 液体试剂 | 固体药品 |
| 稀硫酸、稀盐酸、稀硝酸、NaOH溶液、浓氨水、5%H2O2溶液、浓盐酸、饱和食盐水 | CaCO3、CaO、MnO2、KMnO4、CaC2、 碱石灰、Cu、Zn、Na2S |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
废旧锂离子池的正极材料(主要含有LiCoO2及少量的Al、Fe等)可用于回收钴、锂,工艺流程如下:
(1)在上述溶解过程中,S2O32-被氧化成SO42-,LiCoO2在溶解过程中发生反应的化学方程式为 ,还原产物是 。
(2)在上述除杂过程中,通入空气的作用是 废渣的主要成分是 。
(3)“沉淀钴”和“沉淀锂”的离子方程式分别为 。
(4)除了废渣可以回收利用外,本工艺还可回收的副产品是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
电镀厂镀铜废水中含有CN-和Cr2O72-离子,需要处理达标后才能排放。该厂拟定下列流程进行废水处理, 回答下列问题:
(1)上述处理废水流程中主要使用的方法是 。
(2)②中反应后无气体放出,该反应的离子方程式为 。
(3)步骤③中,每处理0.4mol Cr2O72-时转移电子2.4mol,该反应离子方程式为 。
(4)取少量待测水样于试管中,加入NaOH溶液,观察到有蓝色沉淀生成,再加Na2S溶液, 蓝色沉淀转化成黑色沉淀,请使用化学用语和文字解释产生该现象的原因 。
(5)目前处理酸性Cr2O72-废水多采用铁氧磁体法。该法是向废水中加入FeSO4·7H2O将Cr2O72-还原成Cr3+,调节pH,Fe、Cr转化成相当于 (铁氧磁体,罗马数字表示元素价态)的沉淀。处理1mol Cr2O72-,需加入a mol FeSO4?7H2O,下列结论正确的是 。
(铁氧磁体,罗马数字表示元素价态)的沉淀。处理1mol Cr2O72-,需加入a mol FeSO4?7H2O,下列结论正确的是 。
| A.x ="0.5" ,a =8 | B.x ="0.5" ,a = 10 | C.x =" 1.5" ,a =8 | D.x =" 1.5" ,a = 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
消毒剂在生产生活中有极其重要的作用,开发具有广普、高效、低毒的杀菌剂和消毒剂是今后发展的趋势。
(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是________(填序号)。
| A.Cl2 | B.H2O2 | C.ClO2 | D.O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
钛有强度高和质地轻的优点,广泛应用于飞机制造业等。工业上利用钛铁矿,其主要成分为钛酸亚铁(FeTiO3)制备钛金属,工业流程如下: 已知:Ti与TiO2化学性质稳定,不溶于稀硫酸、稀盐酸等。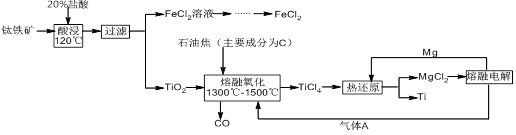
(1)请写出FeTiO3与稀盐酸反应的离子方程式: 。
(2)请写出“熔融氧化”的化学方程式: 。
(3)电解氯化镁的阴极反应式为: ,可循环利用的物质为: (填化学式)。
(4)热还原法中能否改用钠代替镁作还原剂: (填“能”或“不能”);原因为: 。
(5)用此方法制备得到的Ti金属常混有MgCl2和Mg,除杂试剂是 (填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某无色溶液只可能含有以下几种离子:①Mg2+、②Al3+、③Fe2+、④H+、⑤ 、⑥Cl-、⑦OH-。向其中缓慢地滴入NaOH溶液至过量,产生沉淀的质量与加入NaOH溶液的体积的关系如图所示,由此可确定原溶液中一定含有的离子是
、⑥Cl-、⑦OH-。向其中缓慢地滴入NaOH溶液至过量,产生沉淀的质量与加入NaOH溶液的体积的关系如图所示,由此可确定原溶液中一定含有的离子是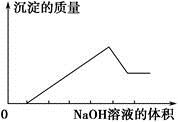
| A.①②⑤ | B.①③④ | C.②⑥⑦ | D.①②④⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com