
| A. | 增加N2的浓度能加快反应速率 | |
| B. | 降低体系温度能加快反应速率 | |
| C. | 使用催化剂不影响反应速率 | |
| D. | 若反应在密闭容器中进行,N2和H2能100%转化为NH3 |
科目:高中化学 来源: 题型:解答题
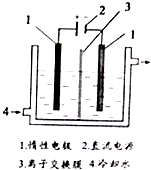 碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.请回答下列问题:
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应中物质变化的实质是旧化学键的断裂和新化学键的形成 | |
| B. | 离子化合物中一定有金属元素和非金属元素 | |
| C. | 全部由非金属元素形成的化合物一定是共价化合物 | |
| D. | 共价化合物中各原子都一定满足最外层8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
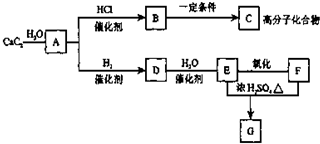 根据如图,回答问题.
根据如图,回答问题. ,GCH3COOCH2CH3
,GCH3COOCH2CH3查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
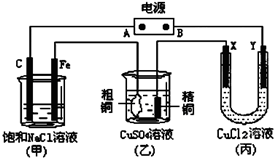 如图所示的装置,X、Y都是惰性电极.将电源接通后,向(甲)中滴入酚酞溶液,在Fe极附近显红色.试回答下列问题:
如图所示的装置,X、Y都是惰性电极.将电源接通后,向(甲)中滴入酚酞溶液,在Fe极附近显红色.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在pH=1的无色溶液中:SO42-、Cu2+、Na+、Cl- | |
| B. | 使pH试纸呈红色的溶液中:Fe2+、NO3-、SO42-、Na+ | |
| C. | 加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、SO42- | |
| D. | 在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×1013的溶液中:NH4+、Ca2+、C1-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
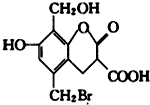 某有机物的结构简式如图,取足量的Na、NaOH 溶液和NaHCO3溶液分别和等物质的量的该有机物在一定的条件下反应(必要时可以加热),完全反应后消耗Na、NaOH和 NaHCO3三种物质的物质的量之比为( )
某有机物的结构简式如图,取足量的Na、NaOH 溶液和NaHCO3溶液分别和等物质的量的该有机物在一定的条件下反应(必要时可以加热),完全反应后消耗Na、NaOH和 NaHCO3三种物质的物质的量之比为( )| A. | 3:4:2 | B. | 3:5:2 | C. | 3:5:1 | D. | 3:4:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com