
【题目】[化学—选修22:化学生活与技术]氯碱工业过程中产生了大量的盐泥。某氯碱工厂的盐泥组成如下:
成分 | NaCl | Mg(OH)2 | CaCO3 | BaSO4 | SiO2等不溶于酸的物质 |
质量分数(%) | 15~20 | 15~20 | 5~10 | 30~40 | 10~15 |
该工厂进一步利用盐泥生产了七水硫酸镁,设计了工艺流程如图:

回答下列问题:
(1)反应器中加入酸溶解,反应液控制pH为5左右,反应温度在50℃左右,写出有关化学反应方程式 。
(2)在滤饼中检测到硫酸钙的成分,其原因是 。
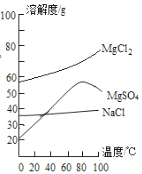
(3)已知一些盐的溶解度如下图。在滤液I中通入高温水蒸气进行蒸发结晶,为了析出晶体I,应控制温度在__________℃。
(4)步骤II操作是_______________,
(5)步骤III在工业上常用的设备是______________(填字母)。
A.加压干燥器 B.蒸馏塔 C.离心机 D.真空干燥器
(6)准确称取制备产品ag,将其加入到盛有V1mL c1mol/L的NaOH溶液的锥形瓶中,溶解后,加入酚酞溶液2滴,溶液变红色,再用c2mol/L的盐酸进行滴定,消耗盐酸V2mL,则样品MgSO4·7H2O的质量分数是 。
【答案】(1)Mg(OH)2+H2SO4===MgSO4+2H2O;CaCO3+H2SO4![]() CaSO4+H2O+CO2↑(2分)。
CaSO4+H2O+CO2↑(2分)。
(2)因为CaCO3+H2SO4![]() CaSO4+H2CO3,加热有H2CO3
CaSO4+H2CO3,加热有H2CO3![]() H2O+CO2↑,降低c(H2CO3),所以平衡不断向右移动,最终CaCO3生成了CaSO4(3分);
H2O+CO2↑,降低c(H2CO3),所以平衡不断向右移动,最终CaCO3生成了CaSO4(3分);
(3)80 (2分);
(4)冷却结晶、洗涤 (2分);
(5)D(2分);
(6)![]() %。(2分)
%。(2分)
【解析】
试题分析:
(1)根据盐泥成分可知,能溶于酸的只有Mg(OH)2和CaCO3两种,又因该流程的目的是制备七水硫酸镁,则加入的酸为硫酸,则反应方程式为:Mg(OH)2+H2SO4===MgSO4+2H2O;CaCO3+H2SO4![]() CaSO4+H2O+CO2↑。
CaSO4+H2O+CO2↑。
(2)因为CaCO3+H2SO4![]() CaSO4+H2CO3,加热有H2CO3
CaSO4+H2CO3,加热有H2CO3![]() H2O+CO2↑,降低c(H2CO3),所以平衡不断向右移动,最终CaCO3生成了CaSO4,导致在滤饼中检测到硫酸钙的成分。
H2O+CO2↑,降低c(H2CO3),所以平衡不断向右移动,最终CaCO3生成了CaSO4,导致在滤饼中检测到硫酸钙的成分。
(3)观察溶解度图象,当温度大于80℃,随着温度的升高,氯化镁的溶解度逐渐增大,而硫酸镁的溶解度反而下降,氯化钠的溶解度一直比较低。故在滤液I中通入高温水蒸气进行蒸发结晶析出的晶体为氯化钠,为避免硫酸镁结晶析出,应控制温度在80℃。
(4)步骤II操作是冷却结晶、洗涤。
(5)步骤III在工业上常用的设备是真空干燥器。
(6)NaOH溶液总物质的量为c1V1×10-3mol,与盐酸反应的NaOH物质的量为c2V2×10-3mol,则与MgSO4·7H2O反应的NaOH物质的量为(c1V1-c2V2)×10-3mol,可得MgSO4·7H2O的质量为(c1V1-c2V2)×10-3××246 g。则样品MgSO4·7H2O的质量分数是![]() %。
%。


科目:高中化学 来源: 题型:
【题目】2015年2月16日李克强总理到东北调研经济情况,重点走访了钢铁厂,鼓励钢铁厂提高钢铁质量和产量,铁及其化合物在日常生活中应用广泛。
(1)利用Fe 2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理。已知含SO2的废气通入含Fe2+、Fe 3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4 H+ =4Fe3+ +2H2O,则另一反应的离子方程式为_________________;
(2)草酸亚铁为黄色固体,作为一种化工原料, 可广泛用于涂料、染料、陶瓷、玻璃器皿等的着色剂以及新型电池材料、感光材料的生产。合成草酸亚铁的流程如下:

①配制(NH4) 2Fe(SO4)2溶液时,需加入少量稀硫酸,目的是___________________。
②得到的草酸亚铁沉淀需充分洗涤,洗涤操作的具体方法为_________________________________,检验是否洗涤干净的方法是___________________________。
(3)将制得的产品(FeC2O4·2H2O)在氩气气氛中进行加热分解,结果如下图(TG%表示残留固体质量占原样品总质量的百分数)。
① 则A→B发生反应的化学方程式为:__________________________________。
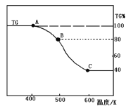
②已知 B→C过程中有等物质的量的两种气态氧化物生成,写出B→C的化学方程式____________;
(4)某草酸亚铁样品中含有少量草酸铵。为了测定不纯产品中草酸根的含量,某同学做了如下分析实验:
Ⅰ.准确称量m g 样品,溶于少量2mol/L 硫酸中并用 100mL 容量瓶定容。
Ⅱ.取上述溶液20mL,用c mol/L高锰酸钾标准溶液滴定,溶液变为淡紫色,消耗高锰酸钾溶液的体积为V 1 mL。
Ⅲ.向上述溶液中加入足量 Zn 粉,使溶液中的 Fe3+恰好全部还原为 Fe2+。
Ⅳ.过滤,洗涤剩余的锌粉和锥形瓶,洗涤液并入滤液
Ⅴ.用c mol/L KMnO4溶液滴定该滤液至溶液出现淡紫色,消耗KMnO4溶液的体积V 2 mL。
已知:2MnO4- +5H2C2O 4+6H+=2Mn2+ +10CO2+8H2O
MnO4- +8H++5Fe2+ =5Fe3+ + Mn2+ +4H2O
回答下列问题:
①若省略步骤Ⅳ,则测定的草酸根离子含量(填―偏大‖、―偏小‖或―不变‖)。
②mg样品中草酸根离子的物质的量为(用 c,V1,V2的式子表示,不必化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己二酸是合成尼龙-66的主要原料之一。实验室合成己二酸的原理、有关数据及装置示意图如下:3![]() +8HNO3—→3
+8HNO3—→3![]() +8NO↑+7H2O
+8NO↑+7H2O

实验步骤如下:
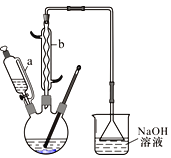
Ⅰ.在三口烧瓶中加入16 mL 50%的硝酸(密度为1.31g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4 mL环己醇。
Ⅱ.水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间。
Ⅲ.当环己醇全部加入后,将混合物用80℃~90℃水浴加热约10 min(注意控制温度),直至无红棕色气体生成为止。
Ⅳ.趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤、干燥、称重。
请回答下列问题:
(1)装置b的名称为 ,使用时要从 (填“上口”或“下口”)通入冷水;滴液漏斗的细支管a的作用是
(2)本实验所用50%的硝酸的物质的量浓度为 ;实验中,氮氧化物废
气(主要成分为N02和NO)可以用NaOH溶液来吸收,其主要反应为:
2N02+2NaOH=NaN02+NaN03+H20和NO+N02+2NaOH=2NaN02+H20
其中NaOH溶液可以用Na2C03溶液来替代,请模仿上述反应,写出Na2C03溶液吸收的两个方程式:
;
(3)向三口烧瓶中滴加环己醇时,反应温度迅速上升,为使反应温度不致过高,必要时可采取的措施是 。
(4)为了除去可能的杂质和减少产品损失,可分别用 和 洗涤晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W 四种短周期元素在周期表中位于连续的四个主族,相对位置如图所示。Z元
素原子核外K层与M层电子数相等。下列说法正确的是
![]()
A. 原子半径由小到大的顺序为Y<X<W<Z
B. Y的单质和Z的单质能够发生反应
C. X的单质都是熔点高、硬度大的物质
D. 工业上利用电解Z、W的熔融氯化物的方法制备对应的单质
查看答案和解析>>
科目:高中化学 来源: 题型:
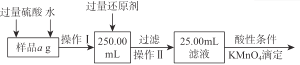
【题目】某氯化铁与氯化亚铁的混合物。现要测定其中铁元素的质量分数,实验按以下步骤进行:

请根据上面流程,回答以下问题:
(1)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有 、 。 (填仪器名称)
(2)请写出加入溴水发生的离子反应方程式 。
(3)将沉淀物加热,冷却至室温,用天平称量其质量为b1g。再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3g,则接下来还应进行的操作是 。若蒸发皿质量是 W1 g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是 。有同学提出,还可以采用以下方法来测定:
①溶解样品改用了硫酸,而不用盐酸,为什么 。
②选择的还原剂是否能用铁 (填“是”或“否”),原因是: 。
③若滴定用掉c mol/ L KMnO4溶液bmL,则样品中铁元素的质量分数是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某科研小组研究:在恒温、恒容(容器容积为2L,)下N2(g)+3H2(g)![]() 2NH3(g)反应的变化。初始条件n (H2)= 3mol 、n (N2)=1mol,反应达到平衡时H2的转化率为60%,NH3的体积分数约为43%
2NH3(g)反应的变化。初始条件n (H2)= 3mol 、n (N2)=1mol,反应达到平衡时H2的转化率为60%,NH3的体积分数约为43%
①此条件下反应的平衡常数K= 。
②若初始条件n (NH3)= 2mol,反应达到平衡时NH3的转化率为 ,
③若初始条件n (H2)= 6mol 、n (N2) =2mol,反应达到平衡时NH3的体积分数 43%,此时移除0.5 mol NH3 ,再次达到平衡时NH3的体积分数 43% (填 “>、<、=”)
(2)N2O5是一种新型硝化剂,其性质和制备受到人们的关注。
一定温度下,在恒容密闭容器中N2O5可发生下列反应:
2N2O5(g)![]() 4NO2(g)+O2(g),ΔH>0
4NO2(g)+O2(g),ΔH>0
①下表为该反应在T1温度下的部分实验数据
t/s | 0 | 500 | 1000 |
c(N2O5)/mol·L—1 | 5.00 | 3.52 | 2.48 |
则500s内NO2的平均生成速率为 。
②现以NO2、O2、N2O5、熔融盐NaNO3组成的燃料电池,采用电解法制备N2O5,装置如图所示。
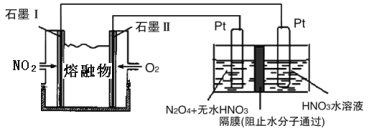
写出石墨I电极上发生反应的电极反应式 。
在电解池中生成N2O5的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粗铜精炼后的阳极泥含有Cu、Au(金)和PbSO4等杂质,湿法处理阳极泥进行综合利用的流程如下:

(1)用CuSO4做电解液电解含铜、金、铅的粗铜,阳极的电极反应式有: 和Cu-2e-= Cu2+。
(2)焙烧阳极泥时,为了提高焙烧效率,采取的合理措施是 。
(3)操作I的主要步骤为 。
(4)写出用SO2还原AuCl4-的离子方程式 。
(5)为了减少废液排放、充分利用有用资源,工业上将滤液1并入硫酸铜溶液进行循环操作,请指出流程图中另一处类似的做法 。
(6)已知298K时,Ksp(PbCO3)=1.46×10-13,Ksp(PbSO4)= 1.82×10-8,用离子方程式表示加入碳酸钠溶液的作用 。m]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种“光敏性高分子”材料在荧光屏及大规模集成电路中应用广泛。其结构如下,对该“光敏性高分子”,下列叙述正确的是( )
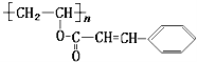
A.化学式为(C11H11O2)n
B.它能发生加成反应,不能发生水解反应
C.它可以和FeCl3溶液发生显色反应
D.1mol该分子最多能和4n mol H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1mol分子式为CmHn的有机化合物在氧气中完全燃烧,且生成CO2和H2O的物质的量相等,并消耗168L氧气。(体积均在标准状况下测定);
(1)该有机化合物的分子式。
(2)若分子中只有两个甲基且属于不饱和烃,写出其结构简式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com