
【题目】化合物A(C12H16O2)经碱性水解、酸化后得到B和C(C8H8O2)。C的核磁共振氢谱表明含有苯环,且苯环上有2种氢原子。B经过下列反应后得到环状化合物G,G的实验式为C2H3O,相对分子质量为172,核磁共振氢谱显示只有一个吸收峰。
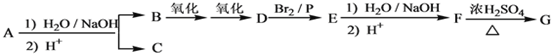
已知:
请回答下列问题:![]()
(1)写出G的分子式:_______________。
(2)写出A的结构简式:______________________。
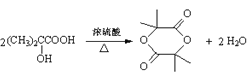
(3)写出F→G反应的化学方程式: ____________,该反应属于________(填反应类型)。
(4)C的同分异构体有多种。
①属于芳香族化合物,且能发生水解反应的有_____种;
(5)F可以发生下列变化:
![]()
J的结构简式是_________________,由F可以直接生成H,设计反应①和②的目的是________________。
【答案】![]()
![]()
 取代反应(或酯化反应)6种
取代反应(或酯化反应)6种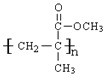
![]()
【解析】
化合物A经碱性水解、酸化后得到B和C(C8H8O2),B能二次氧化生成D,说明A是酯,B是醇,则C是羧酸,C(C8H8O2)的核磁共振氢谱表明含有苯环,且苯环上有2种氢原子,则说明苯环上有2个取代基,且两个取代基处于对位,根据C的分子式知,C是![]() .B经过一系列反应后得到环状化合物G,G的实验式为C2H3O,令分子式为(C2H3O)x,相对分子质量为172,则(24+3+16)x=172,解得x=4,故G的分子式为C8H12O4,核磁共振氢谱显示只有一个峰,说明G只有一种氢原子;B经过两次氧化生成D,D是羧酸,D和溴、P反应生成E,根据题给信息知,E是含有溴原子的羧酸,E经过水解和酸化后生成F,F是含有羟基的羧酸,由于G分子中只有1种H原子,故应是2分子F自身发生酯化反应生成G为环酯,F应含有2个甲基,故F为
.B经过一系列反应后得到环状化合物G,G的实验式为C2H3O,令分子式为(C2H3O)x,相对分子质量为172,则(24+3+16)x=172,解得x=4,故G的分子式为C8H12O4,核磁共振氢谱显示只有一个峰,说明G只有一种氢原子;B经过两次氧化生成D,D是羧酸,D和溴、P反应生成E,根据题给信息知,E是含有溴原子的羧酸,E经过水解和酸化后生成F,F是含有羟基的羧酸,由于G分子中只有1种H原子,故应是2分子F自身发生酯化反应生成G为环酯,F应含有2个甲基,故F为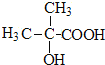 、G为
、G为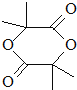 ,逆推可得,E为
,逆推可得,E为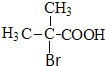 、D为
、D为![]() 、B为
、B为![]() ,故A为
,故A为![]() ,
,
(1)由上述分析可知,G的分子式为:C8H12O4;
(2)由上述分析可知,A的结构简式为:![]() ;
;
(3)F→G反应的化学方程式: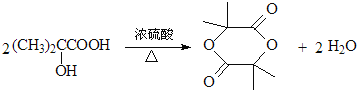 ,属于酯化反应;
,属于酯化反应;
(4)属于芳香族化合物,且能发生水解反应,含有酯基,只有一个侧链时,有乙酸苯酚酯、甲酸苯甲酯、苯甲酸甲酯,若侧链为甲基、-OOCH,有邻、间、对三种位置,故共有6种;
(5)中F与HBr发生取代反应生成K为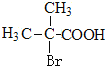 ,K发生消去反应生成H为CH2=C(CH3)COOH,H与甲醇发生酯化反应生成I为CH2=C(CH3)COOCH3,I发生加聚反应生成高聚物J为
,K发生消去反应生成H为CH2=C(CH3)COOH,H与甲醇发生酯化反应生成I为CH2=C(CH3)COOCH3,I发生加聚反应生成高聚物J为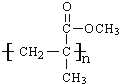 ,由F可以直接生成H,可以发生酯化反应、成醚等副反应,设计反应①和②的目的是减少如酯化、成醚等副反应的发生,故答案为:
,由F可以直接生成H,可以发生酯化反应、成醚等副反应,设计反应①和②的目的是减少如酯化、成醚等副反应的发生,故答案为: ;减少如酯化、成醚等副反应的发。
;减少如酯化、成醚等副反应的发。


科目:高中化学 来源: 题型:
【题目】将碘水中的碘萃取出来的实验中,下列说法不正确的是( )
A.分液漏斗使用前要检验它是否漏水
B.萃取剂要求不溶于水,且比水更容易使碘溶解
C.用CCl4作萃取剂,萃取后液体分层且下层无色
D.分液时,打开旋塞,使下层液体流出,上层液体从上口倒出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】既不能与氢气发生加成反应又不能使酸性高锰酸钾褪色的是:
①甲苯 ②苯酚 ③聚丙烯 ④聚乙炔 ⑤天然橡胶 ⑥苯甲醛 ⑦油脂 ⑧ 直馏汽油 ⑨葡萄糖 ⑩脲醛树脂
A. ③⑧ B. ①⑧⑩ C. ④⑤⑦⑨ D. ①②③⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,CH3COOH:K=1.75×10-5,H2S:K1=1.3×10-7、K2=7.1×10-15。物质的量浓度均为0.1 mol/L的①CH3COONa溶液 ②Na2S溶液 ③NaHS溶液,三种溶液的pH由小到大的顺序是
A. ①③② B. ③①②
C. ③②① D. ②①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】120℃时1体积某气态烃和4体积O2混合,完全燃烧后恢复到原来的温度和压强时,体积不变,该分子式中所含的碳原子数不可能是
A. 1 B. 2 C. 3 D. 7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期金属元素甲~戊在元素周期表中的相对位置如图所示,下列判断正确的是( )
甲 | 乙 | |
丙 | 丁 | 戊 |
A.原子半径:丙<丁<戊
B.金属性:甲>乙
C.最外层电子数:甲>乙
D.最高价氧化物的水化物的碱性:丙>丁>戊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组欲制备漂白剂亚氯酸钠(NaClO2)。甲同学通过查阅文献发现:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出晶体的是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
实验I 乙同学利用下图所示装置制取NaClO2晶体
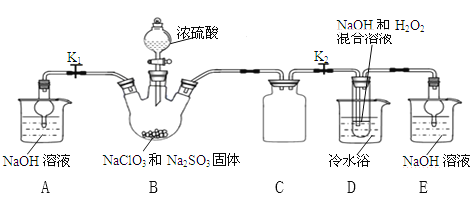
(l)装置B中使浓硫酸顺利滴下的操作是______,该装置中生成了ClO2,反应的化学方程式为_____________。
(2)装置A和E的作用是__________。
(3)装置D中发生反应的化学方程式为____________。
(4)反应结束后,先将装置D反应后的溶液在55℃条件下减压蒸发结晶,然后进行的操作是_______,再用38℃~60℃的温水洗涤,最后在低于60℃条件下干燥,得到NaClO2晶体。
实验Ⅱ 丙同学设计实验测定制得NaClO2样品的纯度
其实验步骤如下:
① 称取所得亚氯酸钠样品ag于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应后,配成100mL混合液。
② 取25.00 mL待测液于锥形瓶中,用bmol/LNa2S2O3标准液滴定,消耗标准液体积的平均值为VmL(已知:I2+2S2O32-=2I-+S4O62-)。
(5)步骤① 反应的离子方程式为______________。
(6)步骤② 滴定中使用的指示剂是_________。
(7)样品中NaClO2的质最分数为_______(用含a、b、V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知反应2H2 + O2 ![]() 2H2O为放热反应,破坏1mol的化学键消耗的能量称为化学键的键能。有关物质中化学键的键能如下表,则生成1mol水可以放出热量 __________kJ
2H2O为放热反应,破坏1mol的化学键消耗的能量称为化学键的键能。有关物质中化学键的键能如下表,则生成1mol水可以放出热量 __________kJ
化学键 | H—H | O=O | H—O |
键能kJ/mol | 436 | 496 | 463 |
(2)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如下图所示,A、B两个电极均由多孔的碳块组成。

①B作_____极材料(填“正”或“负”),电解质溶液中SO42- 移向_____极(填“A”或“B”)。
②写出A极的电极反应式_______,一段时间后,溶液的PH______(填“升高”“降低”“不变”),
③如果将上述装置中通入的H2改成CH4气体,也可以组成一个原电池装置,当有标准状况下11.2L CH4完全反应时,导线中通过的电子的数目__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com