
在一个U形管里盛有CuCl2溶液,并插入两块锌片作电极,按如图连接。
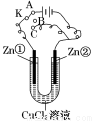
(1)如果把电键K接A,该装置应是电解装置,Zn①极是 极,电极反应式为 ,Zn②极是 极,电极反应式为 。
(2)上述反应进行5 min后,转换电键K到C,则这个装置是原电池装置,Zn①极是 极,电极反应式为 。
(3)上述装置进行2 min后,再转换电键K到B,则Zn①极发生的化学反应为 ,Zn②极发生的有关电化学的反应为 。
(1)阳 Zn-2e-=Zn2+ 阴 Cu2++2e-=Cu
(2)负 Zn-2e-=Zn2+
(3)Zn+CuCl2=ZnCl2+Cu
负极:Zn-2e-=Zn2+,
正极:Cu2++2e-=Cu
【解析】当电键K接触A点时,构成一个有外接直流电源的电解池装置,与电源正极相连的Zn①极是阳极,与电源负极相连的Zn②极是阴极。当工作5 min后,Zn②极上析出了Cu,此时,将电键K接触C点,构成一个原电池装置,表面覆盖铜的Zn②极是原电池的正极,Zn①极是原电池的负极。当把电键K接触B点时,形成断路,Zn①极发生Zn与CuCl2的置换反应,Zn②极由于在锌的表面有铜,又浸在CuCl2溶液中,发生电化学腐蚀。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014年高中化学苏教版选修四专题3 溶液中的离子反应练习卷(解析版) 题型:填空题
现有浓度均为0.1 mol/L的下列溶液:①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵
请回答下列问题:
(1)①②③④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)________。
(2)将③和④等体积混合后,混合液中各离子浓度由大到小的顺序是____________。
(3)已知t°C,KW=1×10-13,则t°C______(填“>”、“<”或“=”)25°C。
(4)25°C时,有pH=x的盐酸和pH=y的氢氧化钠溶液(x≤6,y≥8),取a L该盐酸与b L该氢氧化钠溶液反应,恰好完全中和。两溶液的pH(x、y)的关系式为________________(填表达式)。
查看答案和解析>>
科目:高中化学 来源:2014年高中化学苏教版选修四专题2 反应速率与化学平衡练习卷(解析版) 题型:选择题
[双选题]实验室用锌粒与2 mol·L-1硫酸溶液制取氢气,下列措施不能增大化学反应速率的是( )
A.向该硫酸溶液中加入等体积的水
B.改用3 mol·L-1盐酸
C.改用热的2 mol·L-1硫酸溶液
D.用锌粉代替锌粒
查看答案和解析>>
科目:高中化学 来源:2014年高中化学苏教版选修四专题1 化学反应与能量变化练习卷(解析版) 题型:选择题
沼气是一种能源,它的主要成分是CH4,0.5 mol CH4完全燃烧生成CO2和H2O(l)时,放出445 kJ热量,则下列热化学方程式中正确的是( )
A.2CH4(g)+4O2(g)=2CO2(g)+4H2O(l)ΔH=+890 kJ/mol
B.CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH=+890 kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH=-890 kJ/mol
D. CH4(g)+O2(g)=
CH4(g)+O2(g)= CO2(g)+H2O(l)ΔH=-890 kJ/mol
CO2(g)+H2O(l)ΔH=-890 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四第四章 电化学基础练习卷(解析版) 题型:填空题
如图所示,p、q为直流电源的两极,A由金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D上产生气泡,试回答:
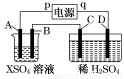
(1)p为 极,A极发生了 反应。
(2)C为 极,可收集到 ;D为 极,可收集到 。
(3)C极的电极反应式为 。
(4)在电解过程中,测C、D两极上产生气体的体积,实验数据如下表:
时间(min) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
阴极产生气体 的体积(cm3) | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 | 79 | 89 |
阳极产生气体 的体积(cm3) | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
仔细分析以上实验数据,请说出变化的可能原因是
。
(5)当反应进行一段时间后,A、B电极附近溶液的pH (填“增大”“减小”或“不变”)。
(6)当电路中通过0.004 mol电子时,B极上沉积的金属X为0.128 g,则此金属的摩尔质量为 。
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四第四章 电化学基础练习卷(解析版) 题型:选择题
1 L某溶液中含有的离子如下表:
离子 | Cu2+ | Al3+ | NO | Cl- |
物质的量浓度(mol/L) | 1 | 1 | a | 1 |
用惰性电极电解该溶液,当电路中有3 mol e-通过时(忽略电解时溶液体积的变化及电极产物可能存在的溶解现象),下列说法正确的是( )
A.电解后溶液的pH=0 B.a=3
C.阳极生成1.5 mol Cl2 D.阴极析出的金属是铜与铝
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四第四章 电化学基础练习卷(解析版) 题型:选择题
下列说法正确的是( )
A.铅蓄电池放电时铅电极发生还原反应
B.电解饱和食盐水在阳极得到氯气,阴极得到金属钠
C.给铁钉镀铜可采用CuSO4作电镀液
D.生铁浸泡在食盐水中发生析氢腐蚀
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四第二章 化学反应速率与化学平衡练习卷(解析版) 题型:选择题
反应A(g)+B(g)  C(g)+D(g)过程中的能量变化如图所示,下列说法正确的是( )
C(g)+D(g)过程中的能量变化如图所示,下列说法正确的是( )
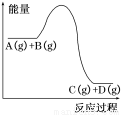
A.该反应的正反应为放热反应
B.升高温度,利于A的转化率增大
C.加入催化剂时,该反应的反应热发生改变
D.增大压强,能够加快反应达到平衡状态的速率
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四第一章 化学反应与能量练习卷(解析版) 题型:选择题
含1 mol Ba(OH)2的稀溶液与足量稀盐酸反应,放出热量114.6 kJ。下列热化学方程式中正确的是( )
A.Ba(OH)2(aq)+2HCl(aq)=BaCl2(aq)+2H2O(l) ΔH=+114.6 kJ/mol
B.Ba(OH)2(aq)+2HCl(aq)=BaCl2(aq)+2H2O(l) ΔH=-114.6 kJ/mol
C.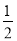 Ba(OH)2(aq)+HCl(aq)=
Ba(OH)2(aq)+HCl(aq)= 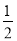 BaCl2(aq)+H2O(l) ΔH=-57.3 kJ/mol
BaCl2(aq)+H2O(l) ΔH=-57.3 kJ/mol
D.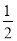 Ba(OH)2(aq)+HCl(aq)=
Ba(OH)2(aq)+HCl(aq)= 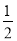 BaCl2(aq)+H2O(l) ΔH=+57.3 kJ/mol
BaCl2(aq)+H2O(l) ΔH=+57.3 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com