
��O2��HClת��ΪCl2�������Ч�棬������Ⱦ��
��1����ͳ�ϸ�ת��ͨ������ͼ��ʾ�Ĵ���ѭ��ʵ�֣�

���У���Ӧ��Ϊ��2HCl(g) + CuO(s) 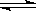 H2O(g)+CuCl2(g) ��H1
H2O(g)+CuCl2(g) ��H1
��Ӧ������1molCl2(g)�ķ�Ӧ��Ϊ��H2�����ܷ�Ӧ���Ȼ�ѧ����ʽΪ , (��Ӧ���á�H1�͡�H2��ʾ)��
��2������RuO2����������HClת��ΪCl2���ܷ�Ӧ���и��õĴ����ԣ�
��ʵ������һ��ѹǿ�£��ܷ�Ӧ��HClƽ��ת�������¶ȱ仯��aHCl��T������ͼ12�����ܷ�Ӧ�ġ�H 0 ,�����������������������A��B�����ƽ�ⳣ��K(A)��K(B)�нϴ���� ��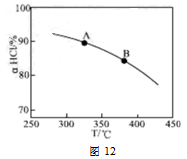
��������ʵ������ѹ�����ʹѹǿ��������ӦaHCl��T���ߵ�ʾ��ͼ������Ҫ˵�����ɣ� ��
�����д�ʩ�����������aHCl����  ��
��
A������n(HCl) B������n(O2) C��ʹ�ø��õĴ��� D����ȥH2O
��3��һ�������²�÷�Ӧ������n(Cl2)���������£�
| t(min) | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| n(Cl2)/10-3mol | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
����2.0��6.0min����HCl�����ʵ����仯��ʾ�ķ�Ӧ���ʣ���mol��min-1Ϊ��λ��д��������̣���
��4��Cl2��;�㷺��д����Cl2�Ʊ�Ư�۵Ļ�ѧ����ʽ��
���𰸡�(1) 2HCl(g) + 1/2O2(g) H2O(g)+Cl2(g) ��H=��H1+��H2
H2O(g)+Cl2(g) ��H=��H1+��H2
(2) �٣� ��K(A)���ڼ���ͼ 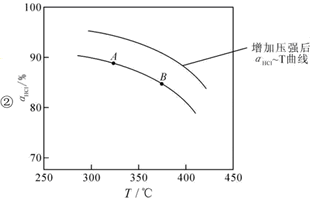
����ѹǿ��ƽ�����ƣ���HCl������ͬ�¶��£�HCl��ƽ��ת���ʱ�֮ǰʵ��Ĵ� ��B��D
(3)�⣺��2.0��6.0minʱ���ڣ�HClת�������ʵ���Ϊn����
2HCl(g) + 1/2O2(g) == H2O(g)+Cl2(g)
2 1
n (5.4-1.8)��10-3mol
��� n=7.2��10-3mol������v(HCl)= 7.2��10-3mol/(6.0-2.0)min==1.8��10-3mol/min
(4)2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O
������������ͼ����Ϣ����ͷָ������������д����Ӧ�ڵ��Ȼ�ѧ����ʽ��CuCl2(g)+1/2O2(g) CuO(s) +Cl2(g) ��H2�����+�ڿɵ��ܷ�Ӧ����2���ٸ���ͼ12��֪�����¶ȵ����ߣ�aHCl��С��˵�������¶ȣ�ƽ���������ƶ������֪�淴Ӧ���ȷ�Ӧ����������Ӧ�Ƿ��ȷ�Ӧ���ʡ�H��0��ͬʱ���������¶ȣ�ƽ�����ƣ�����������٣��¶���B�����A�㣬����ƽ�ⳣ��K(A) ��K(B)����ͬʱ���ڸ��ܷ�Ӧ������ϵ����С�ķ�Ӧ�����ԣ�ѹ�����ʹѹǿ����һ���¶��£�ƽ��Ӧ�����ƶ�����HClӦ����Ŀʵ��״̬��Ϊ�����Կɵ�����ͼ:
CuO(s) +Cl2(g) ��H2�����+�ڿɵ��ܷ�Ӧ����2���ٸ���ͼ12��֪�����¶ȵ����ߣ�aHCl��С��˵�������¶ȣ�ƽ���������ƶ������֪�淴Ӧ���ȷ�Ӧ����������Ӧ�Ƿ��ȷ�Ӧ���ʡ�H��0��ͬʱ���������¶ȣ�ƽ�����ƣ�����������٣��¶���B�����A�㣬����ƽ�ⳣ��K(A) ��K(B)����ͬʱ���ڸ��ܷ�Ӧ������ϵ����С�ķ�Ӧ�����ԣ�ѹ�����ʹѹǿ����һ���¶��£�ƽ��Ӧ�����ƶ�����HClӦ����Ŀʵ��״̬��Ϊ�����Կɵ�����ͼ:  ��
��
��A������n(HCl) ��ƽ�������ƶ�������ƽ���ƶ�ʹHCl���ٵ�����С������HClʹ��������ƣ�����HCl��ת���ʼ�С������B������n(O2) ����Ӧ���Ũ������ƽ���������ƶ���HClת�������ԣ�C��ʹ�ø��õĴ���������ʹ��ѧƽ�ⷢ���ƶ���ʵ��HCl��ת���ʲ��䣬���� D����ȥH2O������С���������Ũ�ȣ�ƽ��������Ӧ�����ƶ���HClת�������ԡ��ʴ���ѡ��B��D����3����Ŀ�и�������n(Cl2)�����ݣ�Ҫ�������HCl�����ʵ����仯��ʾ�ķ�Ӧ���ʣ����Ը��ݷ���ʽ���м��㣬ע����2.0��6.0min�ڵ����ʣ���λ��mol��min-1����2.0��6.0min�ڣ�HClת�������ʵ���Ϊn����
2HCl(g) + 1/2O2(g)��H2O(g)+Cl2(g)
2 1
n (5.4-1.8)��10-3mol
��� n=7.2��10-3mol������v(HCl)= 7.2��10-3mol/(6.0-2.0)min==1.8��10-3mol/min
��4��Cl2��ʯ���鷢����Ӧ��ȡƯ�ۣ���Ӧ�Ļ�ѧ����ʽΪ��2Cl2+2Ca(OH)2��CaCl2+Ca(ClO)2+2H2O��
�����㶨λ��������Ҫ�����˸�˹���ɵ�Ӧ�á���ѧƽ���ƶ�����ѧƽ�ⳣ���Ĵ�С�Ƚϡ���ѧͼ��Ļ����Լ���ѧ��Ӧ���ʵļ��㡣
����ʦ�㾦�����ø�˹���ɽ����Ȼ�ѧ����ʽ����ʱ��Ҫ�۲�ַ�Ӧ���������ܷ�Ӧ��λ�ã����á�ͬ�����������ķ������ַ�Ӧת��Ϊ�ܷ�Ӧ����ѧ��Ӧ���ʵļ���ʱŪ�������Ũ�ȵĸı䣬�����ù�ʽ���м��㡣��ѧƽ�������ͨ���漰��ƽ��״̬���жϡ�ƽ����ƶ���ƽ����йؼ���ȣ�ƽ����ж�ץס����������־�������ʵ�Ũ�Ȳ��ٱ仯��ͬ�����ʵ��������ʺ�����������ȡ�ƽ���ƶ��ж�ʱ���������Ӧ���������ϵ����С����Ӧʱ���Ȼ��Ƿ��ȵȡ��йػ�ѧƽ��ļ�����һ��Ҫ�á�����ʽ�����ڻ���ͼ��ʱͨ����Ŀ���вο������ߣ��ڷ����µ�������ԭ���ߵĹ�ϵ�Ļ����Ͻ��л��ơ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʳƷ��ѧ֪ʶ����������ȷ����(����)
A��ʳ�ο�����ζ����Ҳ����ʳƷ������
B�������߲����������ά����C��������ʧ
C����ά���������ڿ�ˮ��Ϊ�����ǣ��ʿ��������Ӫ������
D�������еĻ������ڼ��Ի���������ɫ���ʿ����մ�ۼ���ٺ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£���0.05 mol Na2CO3��������ˮ���100mL��Һ������Һ�м����������ʡ��йؽ�����ȷ���ǣ� ��
| ��������� | ���� | |
| A | 50mL 1 mol��L��1H2SO4 | ��Ӧ������c(Na+)=c(SO42��) |
| B | 0.05molCaO | ��Һ�� |
| C | 50mL H2O | ��ˮ�������c(H+)��c(OH��)���� |
| D | 0.1molNaHSO4���� | ��Ӧ��ȫ����ҺpH��С��c(Na+)���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵������ȷ���ǣ� ��
A��Na��H2O�ķ�Ӧ�������ķ��ȷ�Ӧ���÷�Ӧ���Է�����
B������Na2SO4��Һ��Ũ�������ʹ��������Һ������������ԭ����ͬ
C��FeCl3��MnO2���ɼӿ�H2O2�ֽ⣬ͬ�������¶��߶�H2O2�ֽ����ʵĸı���ͬ
 D��Mg(OH)2��������Һ�д���ƽ�⣺Mg(OH)2(s)
D��Mg(OH)2��������Һ�д���ƽ�⣺Mg(OH)2(s) Mg2+(aq)+2OH��(aq)���ù��������NH4Cl��Һ
Mg2+(aq)+2OH��(aq)���ù��������NH4Cl��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ںϳɰ���Ӧ���ﵽƽ������·�����ȷ����( )
A�������¶ȣ�������Ӧ�ķ�Ӧ����Ӱ�����
B������ѹǿ��������Ӧ�ķ�Ӧ����Ӱ�����
C����С��Ӧ��Ũ�ȣ����淴Ӧ�ķ�Ӧ����Ӱ�����
D��������������淴Ӧ�ķ�Ӧ����Ӱ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�⼰�仯�����ںϳ�ɱ������ҩ��ȷ�����й㷺��;���ش��������⣺
��1�������ĵ⸻���ں����У���ˮ��ȡ��Ũ��������Ũ��Һ�м�MnO2��H2SO4�����ɵõ�I2���÷�Ӧ�Ļ�ԭ����Ϊ____________��
��2������Ũ��Һ�к���I-��Cl-�����ӣ�ȡһ������Ũ��Һ�������еμ�AgNO3��Һ����AgCl��ʼ����ʱ����Һ��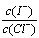 Ϊ��_____________����֪Ksp��AgCl��=1.8��10-10��Ksp��AgI��=8.5��10-17��
Ϊ��_____________����֪Ksp��AgCl��=1.8��10-10��Ksp��AgI��=8.5��10-17��
��3����֪��Ӧ2HI(g) ===H2(g) + I2(g)�Ħ�H= +11kJ��mol��1��1mol H2(g)��1mol I2(g)�����л�ѧ������ʱ�ֱ���Ҫ����436kJ��151kJ����������1molHI(g)�����л�ѧ������ʱ�����յ�����Ϊ______________kJ��
��4��Bodensteins�о������з�Ӧ��
2HI(g) H2(g) + I2(g)
H2(g) + I2(g)
��716Kʱ�����������е⻯������ʵ�������x(HI)�뷴Ӧʱ��t�Ĺ�ϵ���±���
| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0. | 0.773 | 0.780 | 0.784 |
�� ��������ʵ�������÷�Ӧ��ƽ�ⳣ��K�ļ���ʽΪ��___________��
�� ������Ӧ�У�����Ӧ����Ϊv��= k����x2(HI)���淴Ӧ����Ϊv��=k����x(H2)��x(I2)������k����k��Ϊ���ʳ�������k��Ϊ________(��K��k����ʾ)����k�� = 0.0027min-1����t=40minʱ��v��=__________min-1
�� ������ʵ�����ݼ���õ�v��~x(HI)��v��~x(H2)�Ĺ�ϵ������ͼ��ʾ�������ߵ�ijһ�¶�ʱ����Ӧ���´ﵽƽ�⣬��Ӧ�ĵ�ֱ�Ϊ_________________������ĸ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ˮ��Ӧʱ���� �����Ƶ����������ص��ǣ���
�����Ƶ����������ص��ǣ���
| A�� | �Ƶ��ܶ�С | B�� | �Ƶ��۵�� | C�� | �Ƶ�Ӳ��С | D�� | ����ǿ��ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ͼ�е������仯�����������ȷ����(����)
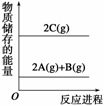
A��2A��B===2C����H<0 B��2C===2A��B����H<0
C��2A(g)��B(g)===2C(g)����H<0 D��2A(g)��B(g)===2C(g)����H>0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����й��л����˵����ȷ����(����)
A�����顢��ϩ��������������ԭ�Ӷ���ͬһƽ����
B�����ۺ���ά�صĻ�ѧʽ����(C6H10O5)n��������ǻ�Ϊͬ���칹��
C��ú���е���˹���ͼ�ͥʹ�õ�Һ��ʯ��������Ҫ�ɷֶ��Ǽ���
D���Ҵ�������������������ñ���Na2CO3��Һ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com