
���� ��1�����崵��������X�������Ҳ����巴Ӧ��
��2����������Һ���嵥�ʺ������٣���Ҫ��������ȡ��
��3���ռ�������������ƿ�ڹ�װ���嵥�ʲ���Ӧ����Һ�������������ܷ⼴�ɵõ���
��4���嵥�ʺ�̼������Һ��Ӧ�����廯�ơ������ƺͶ�����̼���嵥�ʺ������������������Һ�з������з�Ӧ�����嵥�ʣ�
��� �⣺��1�����崵��������X�������Ҳ����巴Ӧ���������嵥����̼������Һ���գ�������̼�غ�̼������Һ��Ӧ����ϩ���巢���ӳɷ�Ӧ����������ɱ��ߣ����Թ�ҵ��������ѡ�ÿ�������ѡB��
�ʴ�Ϊ��B��
��2��������X���崵����ֱ�������л��ܼ�������ȡ����������֮ǰ�庬���ϵͣ���Ҫ������ȡ�������һ�����嵥����ʧ������ȡ��������ȡ��Ч�ʵ��³ɱ��ߣ�
�ʴ�Ϊ������֮ǰ�庬���ϵͣ�����ȡ��������ȡ��Ч�ʵ��£�
��3���ռ������Ŀ�������Ҫ��װ������NaBr��Һ���Լ�ƿ����������������Һ������Ȼ���ܷ��Լ�ƿ�õ�һƿ�����ڵĿ�����
�ʴ�Ϊ����װ������NaBr��Һ���Լ�ƿ����������������Һ������Ȼ���ܷ��Լ�ƿ�õ�һƿ�����ڵĿ�����
��4���嵥�ʺ�̼������Һ��Ӧ�����廯�ơ������ƺͶ�����̼������Ӧ�����ӷ���ʽΪ��3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2�����嵥�ʺ������������������Һ�з������з�Ӧ�����嵥�ʣ���Ӧ�����ӷ���ʽΪ��5Br-+BrO3-+6H+=3Br2+3H2O��
�ʴ�Ϊ��3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2����5Br-+BrO3-+6H+=3Br2+3H2O��
���� ���⿼���˺�ˮ��ȡ�嵥�ʵĹ��̷�����ʵ�������������Ҫ���������ʵ�����Ӧ�ã�ע��������ԭ��Ӧ�IJ����жϣ���Ŀ�Ѷ��еȣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��NaOH��Һ�ζ�CH3COOH��Һ����ѡ�ü�����ָʾ�� | |
| B�� | ����Ͳ��20mL0.5000mol•L-1H2SO4��Һ���ձ��У���ˮ80mL�����Ƴ�0.1000mol•L-1H2SO4��Һ | |
| C�� | �����£����ʵ���Ũ�Ⱦ�Ϊ0.1mol•L-1�����ᡢ������Һ���ֱ���ˮϡ��100����pH�Ĺ�ϵΪ��������� | |
| D�� | ʵ���ҳ����Ȼ������������ᣬ�ټ�ˮϡ������������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������̽�Ϳ���ʯ�� | |
| B�� | ��������Ȼ����ʹ��ʯ�� | |
| C�� | ��Ϊú�Ĵ�����ʯ�ͷḻ��Ӧ��ʹ��ú����Դ | |
| D�� | ������չ���ܡ����ܲ��������̫���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | CH3OH | B�� | C2H5OH | C�� | CH3CH2C��CH3��2OH | D�� | ��CH3��3CCH2OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe3O4�׳����죬������ɫ�����Ϳ�� | |
| B�� | ��������̼���ƵĻ�����������ĭ����� | |
| C�� | �����������������ơ�̼���ƶ��dz�����θ���кͼ� | |
| D�� | ����ũ����ո���ȡ�Ҵ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �����£�pH=6��NaHSO3��Һ�У�c��SO32-��-c��H2SO3��=9.9��10-7mol•L-1 | |
| B�� | 0.1mol•L-1��NH4Cl��Һ�У�c��Cl-����c��NH4+����c��OH-����c��H+�� | |
| C�� | 0.1mol•L-1pH=4��NaHC2O4��Һ��c��H2C2O4����c��C2O42-�� | |
| D�� | ��1.0L0.1mol•L-1�Ĵ�������Һ�м���1.0L0.1mol•L-1���c��Na+����c��CH3COO-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �٢� | D�� | �٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ŵ�ʱ��������ӦΪ��PbO2+4H++2e-=Pb2++2H2O | |
| B�� | ���ʱ����������������23.9gʱת��0.4mol���� | |
| C�� | �ŵ�ʱ���������������Һ��pH���� | |
| D�� | ���ʱ��Pb�缫���Դ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| I���Լ� | II���Լ� | Ŀ�� | װ�� | |
| A | ����ʯ��ˮ | ��������KMnO4��Һ | ����SO2���Ƿ�����CO2 | 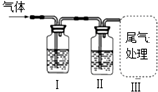 |
| B | ��ˮ | NaOH��Һ | ��ȥCH4�л��е�C2H4���� | |
| C | ����Na2CO3��Һ | Ũ���� | ��ȥCO2�л���HCl���� | |
| D | ����ʯ��ˮ | CuSO4��Һ | ֤����������к���CO2��H2O���壮 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com