
【题目】H 是一种免疫调节剂,其合成流程如下:

问答下列问题:
(1)H所含官能团有氨基、羟基和______________。
(2)X的化学式为_______________,③的反应类型是_____________。
(3)设计反应①和⑤的目的是__________________。
(4)反应①为取代反应,其化学方程式为________________。
(5)R的同分异构体M同时满足下列条件:
①M 能与氯化铁溶液发生显色反应
②1molM 最多能和4molNaOH 发生反应
③在核磁共振氢谱上有四组峰且峰的面积之为3:3:2:2
M 的结构简式可能为________________。
(6)已知: ,结合上述相关信息,以
,结合上述相关信息,以 为原料设计合成路线合成
为原料设计合成路线合成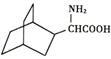 _________(其他试剂自选)。
_________(其他试剂自选)。
【答案】 羧基 C12H14O4 氧化反应 保护羟基,避免羟基在反应③中被氧化 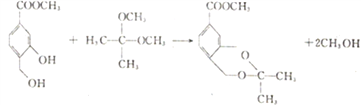

【解析】(1)H为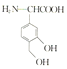 ,所含官能团有氨基、羟基和羧基;(2)X为
,所含官能团有氨基、羟基和羧基;(2)X为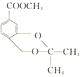 ,化学式为C12H14O4,根据Y的分子式及X、Z的结构简式可推断Y为
,化学式为C12H14O4,根据Y的分子式及X、Z的结构简式可推断Y为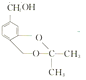 ,③是
,③是 在铜的催化下发生氧化反应生成
在铜的催化下发生氧化反应生成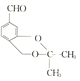 ,反应类型是氧化反应;(3)设计反应①和⑤的目的是保护羟基,避免羟基在反应③中被氧化;(4)反应①为取代反应,为R与反应生成X与甲醇,反应的化学方程式为
,反应类型是氧化反应;(3)设计反应①和⑤的目的是保护羟基,避免羟基在反应③中被氧化;(4)反应①为取代反应,为R与反应生成X与甲醇,反应的化学方程式为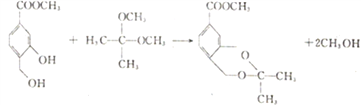 ;(5)R的同分异构体M同时满足条件:①M能与氯化铁溶液发生显色反应,则含有酚羟基;②1molM最多能和4molNaOH发生反应,则含有酚羟基或羧基可能为4个,或酯基酚羟基3个;③在核磁共振氢谱上有四组峰且峰的面积之为3:3:2:2,则高度对称。
;(5)R的同分异构体M同时满足条件:①M能与氯化铁溶液发生显色反应,则含有酚羟基;②1molM最多能和4molNaOH发生反应,则含有酚羟基或羧基可能为4个,或酯基酚羟基3个;③在核磁共振氢谱上有四组峰且峰的面积之为3:3:2:2,则高度对称。
M的结构简式可能为 ;(6)结合上述相关信息,
;(6)结合上述相关信息, 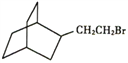 在氢氧化钠的乙醇溶液中加热发生消去反应生成
在氢氧化钠的乙醇溶液中加热发生消去反应生成 ,
, 氧化转化为
氧化转化为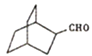 ,
, 与氰化钠、氨气反应生成
与氰化钠、氨气反应生成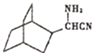 ,
, 在硫酸作用下控制pH得到
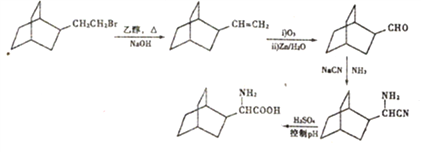
在硫酸作用下控制pH得到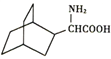 ,合成路线如下:
,合成路线如下:  。
。


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
【题目】下列物质中,不能与CO2发生反应的是( )。
①Na2O ②Na2O2 ③NaCl ④NaOH ⑤NaHCO3
A.①④B.②③C.③⑤D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途具有对应关系的是
A.明矾易溶于水,可用作净水剂
B.Al2O3熔点高,可用于制作耐火材料
C.HClO具有弱酸性,可用于漂白、消毒
D.Al(OH)3高温会分解,可用于治疗胃酸过多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于密闭容器中进行的可逆反应:2SO2(g)+O2(g) ![]() 2SO3(g),下列能判断该反应已经达到化学平衡状态的是( )
2SO3(g),下列能判断该反应已经达到化学平衡状态的是( )
A.SO2、O2、SO3的浓度相等
B.SO2、O2、SO3的浓度不再发生变化
C.SO2、O2、SO3在密闭容器中共存
D.反应停止,正、逆反应速率都等于零
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关人体细胞组成元素的叙述,正确的是
A.人体不同细胞的元素种类和含量都大致相同
B.构成细胞的微量元素的含量少,生理作用也小
C.组成人体的元素在非生物界中都能找到
D.C是最基本元素,也是细胞鲜重中含量最多的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NiS 可用作陶瓷和搪瓷的着色剂。NiS 在有水存在时能被氧气氧化成Ni(OH)S。将H2S通入稀硫酸酸化的NiSO4溶液中,经过过滤,制得NiS 沉淀,装置如图所示:

下列对实验的叙述正确的是
A. 在装置A中滴加蒸馏水前通入N2,是为了将H2S赶入C 装置中与NiSO4溶液反应
B. 装置B 中盛放浓硫酸
C. 装置D 中的洗涤液应用煮沸过的蒸馏水
D. 反应结束后继续通入N2 可将C装置中产生的沉淀压入过滤沉淀漏斗中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)对眼和上呼吸道黏膜有强烈的刺激性,但其在工业上有重要作用。其与硫酸的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其他性质 |
SO2Cl2 | -54.1 | 69.1 | ①遇水易水解,产生大量白雾,生成两种强酸 ②易分解:SO2Cl2 |
H2SO4 | 10.4 | 338 | 强吸水性、稳定不易分解 |
实验室用干燥纯净的氯气和过量的二氧化硫在活性炭的催化作用下合成硫酰氯,反应方程式为:SO2(g)+Cl2(g)=SO2Cl2(1)H<0,其实验装置如图所示(夹持仪器已省略):

(1)仪器A的名称为____________,冷却水应该从______(填“a”或“b”)口进入。
(2)仪器B中盛放的药品是__________。
(3)实验时,装置戊中发生反应的化学方程式为____________。
(4)若缺少装置乙和丁,则硫酰氯会水解,硫酰氯水解的化学方程式为___________。
(5)反应一段时间后,需在丙装置的三颈瓶外面加上冷水浴装置,其原因是__________。
(6)实验开始时,戊中开始加入12.25gKC1O3,假设KC1O3在过量盐酸作用下完全转化为Cl2,实验结束后得到32.4g纯净的硫酰氯,则硫酰氯的产率为______。
(7)少量硫酰氯也可用氙磺酸(ClSO2OH)直接分解获得,反应方程式为:2ClSO2OH=H2SO4+SO2Cl2。
①在分解产物中分离出硫酰氯的实验操作名称是_____,现实验室提供的玻璃仪器有漏斗、烧杯、蒸发皿、酒精灯、接液管、锥形瓶,该分离操作中还需要补充的玻璃仪器是_____、_____、_____。
②分离出的产品中往往含有少量的H2SO4,请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、紫色石蕊试液):___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光催化技术是一种在能源和环境领域有着重要应用前景的绿色技术。Ti的某种晶型的氧化物M可用作光催化材料。
(1)基态Ti原子的价层电子排布图为________。
(2)在第四周期d区元素中,与Ti 原子未成对电子数相同的元素名称是________。
(3)金属钛的原子堆积方式如图1所示,则金属钛晶胞俯视图为_____。

(4)生活环境中的臭气源有氨气、甲硫醇(CH3-SH) 等,M 可以作为高效除臭剂。与氨气互为等电子体的阳离子为_____,甲硫醇中硫原子采取的杂化方式为_____,与S位于同一周期,且第一电离能小于S 的非金属元素符号为______,已知甲硫醇熔沸点小于甲醇(CH3OH),试解释此差异的主要原因___________。
(5)M 的晶胞结构如图2,M 化学式为______。
(6)石墨烯是单个原子厚度的二维碳纳米材料( 如图3),其比表面积大( 比表面积指单位质量物料所具有的总面积)。石墨烯与M 的结合使用,极大地提高了M 的光催化效果。在石墨烯晶体中,每个最小的六元环占有____个C 原子。已知石墨烯中C-C 键长为a pm,则单层石墨烯的比表面积为_____m2/g(NA表示阿伏伽德罗常数的数值,忽略碳原子的厚度)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用工业炼铅产生的锌灰(主要成分为ZnO、PbO、FeO、MnO2、CuO)可回收制备ZnCl2,工艺流程如下:
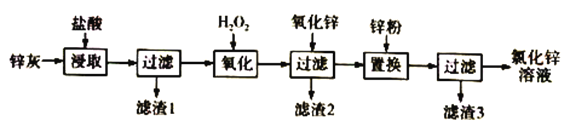
回答下列问题
(1)“浸取”实验中,反应体系的温度、反应时间对锰脱除效果的影响如下表,则适合的温度和反应时间分别是________________、____________________。

(2)“滤渣1”的主要成分是_____________。
(3)H2O2溶液的作用是____________________________________,已知“滤渣2”的主要成分是Fe(OH)3,则氧化锌的作用是_______________________________。“置换”实验中发生的反应的离子方程式有Zn+Pb2+=Ph+Zn2+、___________________________________。
(4)由锌灰制取金属锌可采用碱溶解,然后电解浸取液,已知:ZnO溶于NaOH溶液中生成[Zn(OH)4]2-,则阴极的电极反应为___________________________________。
(5)ZnCl2晶体溶解于饱和Na2CO3溶液中,得到6.46g的碱式碳酸锌[Znx(CO3)y(OH)z,为了测定其组成,充分加热分解,产生的气体依次通入浓硫酸和碱石灰,质量分别增重了0.72g和0.88g,则该碱式碳酸锌的化学式为______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com