
| A. | NaOH溶液可保存在玻璃塞的试剂瓶中 | |
| B. | 液溴应盛放在用水密封且用玻璃塞塞紧的棕色试剂瓶中 | |
| C. | 一学生用广泛pH试纸测得某浓度的稀盐酸pH为2.3 | |
| D. | 配制硫酸亚铁溶液,是将绿矾晶体溶于蒸馏水再加入一定量的铁粉 |
分析 A.玻璃中含有SiO2能与碱反应有黏性的Na2SiO3;
B.溴水见光易分解,用棕色瓶盛装;
C.广泛pH试纸精确到1;
D.配制完后,要加铁粉和稀硫酸,铁粉是还原被氧化的二价铁,稀硫酸是抑制硫酸亚铁的水解.
解答 解:A.因玻璃中含有SiO2,SiO2能与碱反应SiO2+2NaOH═Na2SiO3 +H2O,生成有黏性的Na2SiO3,会导致玻璃塞打不开,所以装浓NaOH溶液的试剂瓶不能用玻璃塞密封,故A错误;
B.液溴应盛放在用水密封且用玻璃塞塞紧的棕色试剂瓶中液溴容易挥发,所以要密封保存,且会加入少量的水密封.在水中有:Br2+H2O?HBr+HBrO,加热或光照,都会促进反应.所以,要避光,用棕色的瓶子.但是由于溴水溶液呈酸性,会腐蚀橡胶塞,所以,只能用玻璃塞,故B正确;
C.广泛pH试纸精确到1,无法测得pH为2.3,故C错误;
D.应该加要加铁粉和稀硫酸,铁粉可以还原被氧化的二价铁,硫酸亚铁易水解,需要增大氢离子浓度,防止水解,故D错误.
故选B.
点评 本题考查化学试剂的存放、PH试纸的使用、溶液的配制,难度不大,注意配制硫酸亚铁溶液要加铁粉和稀硫酸,铁粉是还原被氧化的二价铁,稀硫酸是抑制硫酸亚铁的水解.


科目:高中化学 来源: 题型:解答题
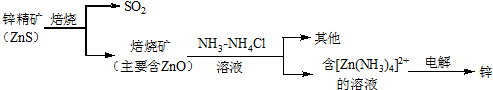
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
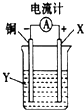
| A. | X可以是银或石墨 | B. | Y是硫酸铜溶液 | ||
| C. | 电子从铜电极经外电路流向X电极 | D. | X极发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②③④① | C. | ④③②① | D. | ②③①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氟氯代烷是一类含氟和含氯的卤代烃 | |
| B. | 氟氯代烷化学性质稳定,有毒 | |
| C. | 氟氯代烷大多无色、无臭、无毒 | |
| D. | 在平流层中,氟氯代烷在紫外线照射下,分解产生的氯原子可引发损耗臭氧层的循环反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
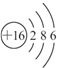 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室配置氯化铁溶液,将氯化铁固体溶于水,加盐酸抑制水解 | |
| B. | 取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ | |
| C. | 室温下向苯和少量苯酚的混合溶液中加入适量NaOH溶液,振荡、静置后分液,可除去苯中少量苯酚 | |
| D. | 已知I3-?I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳与浓硫酸加热 | B. | 浓硫酸与NaCl固体加热 | ||
| C. | 浓硫酸中加入铜片 | D. | 蔗糖与浓硫酸混合后炭化发黑 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com