
【题目】氯碱工业是以电解食盐水为基础的基本化学工业,电解食盐水同时得到两种气体(一种是所有气体中密度最小的气体,一种是黄绿色气体)和一种易溶、易电离的碱。
(1)试写出电解食盐水的化学方程式:_______________________________
(2)上述产物彼此之间或与其它物质可以发生有重要工业价值的反应,写出你能想到的其中一个化学方程式________________________________________________________
(3)把Cl2通入NaBr溶液中,并向其中加入少量四氯化碳,振荡后静置,液体分为两层,下层为______色。其中涉及的离子方程式为_____________________________。
【答案】 2NaCl+ 2H2O![]() 2NaOH + H2↑ + Cl2↑ H2 + Cl2
2NaOH + H2↑ + Cl2↑ H2 + Cl2![]() 2HCl 或 2NaOH + Cl2=NaCl + NaClO + H2O 橙红色 Cl2 + 2Br- =Br2 +2Cl-
2HCl 或 2NaOH + Cl2=NaCl + NaClO + H2O 橙红色 Cl2 + 2Br- =Br2 +2Cl-
【解析】(1)电解饱和食盐水生成是氢气、氯气和氢氧化钠;
(2)氯气与氢气化合制备盐酸,与氢氧化钠反应制备漂白液;
(3)氯气与溴化钠反应生成氯化钠和溴。
(1)电解食盐水同时得到两种气体,一种是所有气体中密度最小的气体,应该是氢气。一种是黄绿色气体,是氯气。另一种是易溶、易电离的碱,应该是氢氧化钠,则电解食盐水的化学方程式为2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑;
(2)上述产物彼此之间或与其它物质可以发生有重要工业价值的反应,例如制备盐酸或制备漂白液,方程式分别是H2+Cl2![]() 2HCl或2NaOH+Cl2=NaCl+NaClO+H2O;
2HCl或2NaOH+Cl2=NaCl+NaClO+H2O;
(3)氯气氧化性强于溴,把Cl2通入NaBr溶液中生成氯化钠和单质溴,反应的离子方程式为Cl2+2Br-=Br2+2Cl-;溴易溶在有机溶剂中,则向其中加入少量四氯化碳,振荡后静置,液体分为两层,四氯化碳密度大于水,下层为橙红色。


科目:高中化学 来源: 题型:
【题目】下面有关氧化还原反应的叙述正确的是( )
A.在反应中不一定所有元素的化合价都发生变化
B.肯定有一种元素被氧化,另一种元素被还原
C.非金属单质在反应中只做氧化剂
D.某元素从化合物变为单质时,该元素一定被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸(HNO2)在反应中既可作氧化剂,又可作还原剂。当它作氧化剂时,其还原产物可能是( )
①NO ②NO2 ③HNO3 ④N2 ⑤NH3
A.②③B.①②③C.①④⑤D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的分类正确的是( )
A.氯化钡、四氯化碳、硫酸、碘酒都属于化合物
B.硝酸、纯碱、磷酸钠、二氧化碳分别属于酸、碱、盐、氧化物
C.溶液、浊液、胶体、空气都属于混合物
D.CO2、SO2、P2O5、CO都属于酸性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.向Ba(OH)2溶液中加稀硫酸:Ba2++OH﹣+H++SO42-═BaSO4↓+H2O
B.用惰性电极电解MgCl2溶液:2Cl﹣+2H2O ![]() Cl2↑+H2↑+2OH﹣
Cl2↑+H2↑+2OH﹣
C.向小苏打溶液中加入少量的澄清石灰水:2HCO3﹣+Ca2++2OH﹣═CaCO3↓+2H2O+CO32﹣
D.足量CO2通入NaOH溶液:CO2+2 OH﹣═CO32﹣+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烃1体积最多能与2体积HBr发生加成反应,所得产物1mol可与6mol Cl2发生完全取代反应,则该烃的结构简式为
A. CH2=CH—CH3 B. CH3—CH=CH—CH3
C. CH2=CH-CH=CH2 D. CH3-C≡CH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是自来水表的常见安装方式.下列有关说法不正确的是( ) 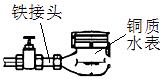
A.发生腐蚀过程中,电子从接头流向水表
B.腐蚀时,铁接头发生的是还原反应
C.腐蚀时铜质水表发生的电极反应为:2H2O+O2+4e﹣═4OH﹣
D.腐蚀过程还涉及到反应:4Fe(OH)2+2H2O+O2═4Fe(OH)3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com