
分析 (1)根据溶质的质量分数ω=$\frac{{m}_{溶质}}{{m}_{溶液}}$×100%计算;
(2)根据Na2SO3•7H2O晶体和原溶液中溶质的质量求出10℃是饱和溶液中溶质的质量和溶剂的质量,再求出10℃时Na2SO3在水中的溶解度,即100g水中溶解 Na2SO3的质量.
解答 解:(1)30℃时Na2SO3饱和溶液中Na2SO3的质量分数ω=$\frac{{m}_{溶质}}{{m}_{溶液}}$×100%=$\frac{35.5g}{35.5g+100g}$×100%=26.20%,
答:30℃时Na2SO3饱和溶液中Na2SO3的质量分数为26.20%.
(2)冷却溶液后,析出晶体79.5g,根据其晶体Na2SO3•7H2O的组成,其中含有水和亚硫酸钠为:
m(Na2SO3)=79.5g×$\frac{126}{126+126}$=39.75g,
m(H2O)=79.5g-39.75g=39.75g,
10℃时Na2SO3的质量为271-200-39.75=31.25g,
10℃时H2O的质量为200-39.75=160.25g,
假设10℃时Na2SO3的溶解度为S,则
$\frac{S}{100g}=\frac{31.25g}{160.25g}$,
解得S=19.5g;
答:10℃时Na2SO3在水中的溶解度为19.50g/100g水.
点评 本题考查了溶液的质量分数的和溶解度的数理关系,难度中等,侧重于基本概念以及数理分析能力和计算能力的培养.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
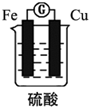
| A. | 该电池工作时电能转变为化学能 | B. | 铁片的质量变轻 | ||
| C. | 铜片上发生的反应2H++2e-=H2↑ | D. | SO42-向铁片移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水泥、玻璃、水晶饰物都是硅酸盐制品 | |
| B. | 用澄清石灰水鉴别SO2 和CO2 | |
| C. | 将Fe(NO3)2 溶于稀盐酸,滴加KSCN 溶液没有颜色变化 | |
| D. | 透闪石的化学成分为Ca2Mg5Si8O22(OH)2 写成氧化物的形式为:2CaO•5MgO•8SiO2•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已溶解的溶质和未溶解的溶质质量相等 | |
| B. | 溶质不再溶解,因此从表面看溶质不再减少,也不再增加 | |
| C. | 升高温度,饱和溶液将变为不饱和溶液 | |
| D. | 溶质的溶解和结晶继续进行,且速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 压强p/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/mol•L-1 | 0.08 | 0.20 | 0.44 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在五水硫酸铜中滴加少量浓硫酸,固体颜色由蓝变白,说明浓硫酸具有吸水性 | |
| B. | 在未知试液中滴加BaCl2溶液得白色沉淀,取该白色沉淀加稀盐酸不溶解,说明原未知试液中含有SO42- | |
| C. | 在铜片上滴加少量稀硫酸,无明显现象,说明稀硫酸没有氧化性 | |
| D. | 某未知气体通入品红溶液中,品红溶液褪色,则原气体一定是 SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
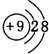
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | +4、-2 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.102 | 0.110 | 0.143 | 0.160 | 0.186 |
 .
.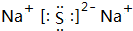 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com