
| m |
| M |
| V |
| Vm |
| 3.6g |
| 18g/mol |
| 3.36L |
| 22.4L/mol |
| 3.0g-2.2g |
| 16g/mol |
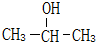 ,
,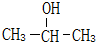 .
.


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、5.4 kJ |
| B、350 kJ |
| C、3.5 kJ |
| D、8.5 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 碳氧化物的转化有重大用途,回答关于CO和CO2的问题.
碳氧化物的转化有重大用途,回答关于CO和CO2的问题.| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石油裂化主要得到乙烯 |
| B、石油分馏是化学变化,可得到汽油、煤油 |
| C、煤干馏主要得到焦炭、煤焦油、粗氨水和焦炉气 |
| D、石油的裂解可提高汽油等轻质油的质量和产量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O |
| B、CuO+2HNO3 (稀)=Cu(NO3)2+H2O |
| C、C+4HNO3 (浓)=CO2↑+4NO2↑+2H2O |
| D、3Ag+4HNO3 (稀)=3 AgNO3+NO↑+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com