
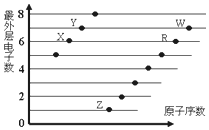
| A. | X与W形成的化合物中只有共价键 | B. | X与Z形成的化合物中只有离子键 | ||
| C. | 元素的非金属性:X>R>W | D. | 简单离子的半径:W>R>X |
分析 都是短周期元素,由最外层电子数与原子序数关系可知,X、Y处于第二周期,X的最外层电子数为6,故X为O元素,Y的最外层电子数为7,故Y为F元素;Z、R、W处于第三周期,最外层电子数分别为1、6、7,故Z为Na元素、R为S元素、W为Cl元素,结合对应单质、化合物的性质以及元素周期律知识解答该题.
解答 解:X为O元素,Y为F元素,Z为Na元素、R为S元素、W为Cl元素,
A.X为O元素,W为Cl元素,形成的化合物为共价化合物,只有共价键,故A正确;
B.X与Z形成的化合物过氧化钠中既有共价键也有离子键,故B错误;
C.元素的非金属性Cl>S,故C错误;
D.核外电子排布相同的离子,核电荷数越大离子半径越小,则X>R,故D错误.
故选A.
点评 本题考查原子结构与元素周期律知识,为高考常见题型和高频考点,侧重于学生的分析能力的考查,根据最外层电子数及原子序数的关系确定元素是解题的关键,注意整体把握元素周期表的结构,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 体现浓硫酸的吸水性 | |
| B. | 体现了浓硫酸的脱水性 | |
| C. | 体现了浓硫酸的吸水性和脱水性 | |
| D. | 体现了浓硫酸的吸水性、脱水性和强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 实验内容 | 实验目的 |
| A | 测定相同物质的量浓度的KOH和氨水的pH | 证明氨水中存在电离平衡 |
| B | 向混有NaCl的NaOH溶液中滴入已知浓度的盐酸(用酚酞作指示剂) | 滴定其中NaOH含量 |
| C | 将Mg、Al和NaOH溶液设计为原电池 | 比较Mg、Al活泼性强弱 |
| D | 用惰性电极电解饱和食盐水,阴极附近滴加酚酞 | 验证阴极有碱生成 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H4=△H3+△H2+△H1 | B. | △H4=△H3+2△H2+2△H1 | ||
| C. | △H4=△H3+2△H2-2△H1 | D. | △H4=△H3+2△H2-△H1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
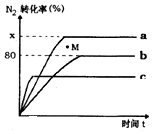 氢气是一种高能燃料,也广范应用在工业合成中.
氢气是一种高能燃料,也广范应用在工业合成中.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 医疗上常用75%的酒精进行消毒 | B. | 光导纤维的主要成份是二氧化硅 | ||
| C. | 食品行业用小苏打制作发酵粉 | D. | SO2可以随意排放,对环境没有污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高纯度的硅单质广泛用于制作光导纤维 | |
| B. | 液氨可用作制冷剂 | |
| C. | 常温下可用铝制容器盛装浓硫酸 | |
| D. | 明矾常用于水的净化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=5的溶液中c(H+)=1.0×10-5 mol•L-1 | |
| B. | pH=7的溶液呈中性 | |
| C. | pH值为0的溶液中c(H+)=0 mol/L | |
| D. | pH=5的溶液中c(OH-)=1.0×10-9 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com