
反应A+B→C分两步进行: ①A+B→X, ②X→C, 反应过程中能量变化如图所示, E1表示反应A+B→X的活化能。下列有关叙述不正确的是( )
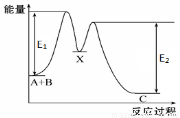
A.反应A+B→X的△H >0
B.反应A+B→C的△H = E1-E2
C.E2表示反应C→X的活化能
D.X是反应A+B→C的中间产物
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源:2017届北京市高三12月月考化学试卷(解析版) 题型:选择题
关于溶液的酸碱性说法正确的是 ( )
)
A.C(H+)很小的溶液一定呈碱性
B.PH=7的溶液一定呈中性
C.C(OH-)=C(H+)的溶液一定呈中性
D.不能使酚酞试液变红的溶液一定呈酸性
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上学期阶段考二化学试卷(解析版) 题型:选择题
常温下,有KOH和Ca(OH)2的混合溶液,测得其pH=13。取此溶液300 mL,向其中通入CO2,通入CO2的体积(V)和生成沉淀的物质的量(n)的关系如图所示,图中V1为224 mL(标准状况),则图中V2、V3的数值(单位为mL)分别是( )
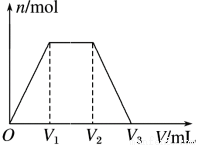
A.336、672 B.448、672
C.1120、1176 D.296、352
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省湖州市高二上期中化学试卷(解析版) 题型:填空题
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:
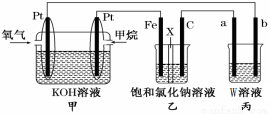
(1)石墨电极(C)作 极,甲中甲烷燃料电池的负极反应式为 。
(2)若消耗2.24 L(标况)氧气,则乙装置中铁电极上生成的气体体积(标况)为 L。
(3)丙中以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是________。
A.a电极为纯铜
B.粗铜接电源正极,发生还原反应
C.CuSO4溶液的浓度保持不变
D.利用阳极泥可回收Ag、Pt、Au等金属
(4)若丙中以稀H2SO4为电解质溶液,电极材料b为铝,则能使铝表面 生成一层致密的氧化膜,该电极反应式为 。
生成一层致密的氧化膜,该电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省湖州市高二上期中化学试卷(解析版) 题型:选择题
一定条件下,反应4NH3(g)+5O2(g)  4NO(g)+6H2O(g) △H =-a kJ·mol-1,在5 L密闭容器中进行,10 s时达到平衡,水蒸气的物质的量增加了0.6 mol,则下列说法正确的是( )
4NO(g)+6H2O(g) △H =-a kJ·mol-1,在5 L密闭容器中进行,10 s时达到平衡,水蒸气的物质的量增加了0.6 mol,则下列说法正确的是( )
A.第10s时,H2O的反应速率为0.012 mol·Lˉ1·sˉ1
B.10s内,NH3的平均反应速率为0.48 mol·Lˉ1·minˉ1
C.10s内,反应放出的热量为a kJ
D.这10s内,O2的反应速率逐渐减小,NO的反应速率逐渐增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省湖州市高二上期中化学试卷(解析版) 题型:选择题
关于反应CaCO3(s) = CaO (s)+CO2(g),下列说法中正确的是( )
A.△H < 0 B.△S < 0 C.高温下自发进行 D.一定不能自发进行
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省慈溪市高二上学期期中化学试卷(解析版) 题型:选择题
某温度时,可逆反应:X(g)+Y(g) Z(g)的平衡常数K=1.0,若反应物的初始浓度c(X)=4 mol·L-1,c(Y)=a mol·L-1,达到平衡后c(Z)=2 mol·L-1。则a为( )
Z(g)的平衡常数K=1.0,若反应物的初始浓度c(X)=4 mol·L-1,c(Y)=a mol·L-1,达到平衡后c(Z)=2 mol·L-1。则a为( )
A.1 B.2 C.3 D.4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省慈溪市高二上学期期中化学试卷(解析版) 题型:选择题
下列措施或事实不能用勒沙特列原理解释的是( )
A.新制的氯水在光照下颜色变浅
B.H2、I2、HI平衡混合气加压后颜色变深
C.工业上生产硫酸的过程中,使用过量的空气以提高SO2的利用率
D.在合成氨的反应中,加压有利于氨的合成
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二上期中化学试卷(解析版) 题型:选择题
将4mol A气体和2mol B气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)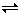 2C(g)。若经2s后测得C的浓度为0.6mol/L,现有几种说法:
2C(g)。若经2s后测得C的浓度为0.6mol/L,现有几种说法:
①用物质A表示的反应的平均速率为0.3 mol/(L·s)
②用物质B表示的反应的平均速率为0.6 mol/(L·s )
③2s时物质A的转化率为70%
④2s时B物质的浓度为0.7 mol/L
其中正确的是( )
A.①③ B.①④ C.②③ D.③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com