
【题目】根据能量变化示意图,下列热化学方程式正确的是( )
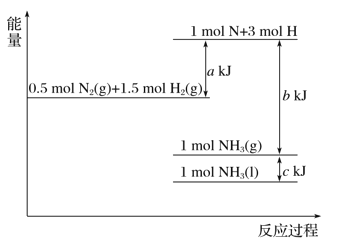
A. N2(g)+3H2(g)===2NH3(g) ΔH=-(b-a) kJ·mol-1
B. N2(g)+3H2(g)===2NH3(g) ΔH=-(a-b) kJ·mol-1
C. 2NH3(l)===N2(g)+3H2(g) ΔH=2(a+b-c) kJ·mol-1
D. 2NH3(l)===N2(g)+3H2(g) ΔH=2(b+c-a) kJ·mol-1
【答案】D
【解析】由图可知,![]() N2(g)+
N2(g)+![]() H2(g)=NH3(g)△H=(a-b)kJmol-1,
H2(g)=NH3(g)△H=(a-b)kJmol-1,![]() N2(g)+
N2(g)+![]() H2(g)=NH3(l)△H=(a-b-c)kJmol-1。A.N2(g)+3H2(g)=2NH3(g)△H=-2(b-a)kJmol-1,故A错误;B.N2(g)+3H2(g)=2NH3(g)△H═-2(b-a)kJmol-1,故B错误;C.物质的量与热量成正比、互为可逆反应的焓变的数值相同而符号相反,则2NH3(1)=N2(g)+3H2(g)△H=2(-a+b+c)kJmol-1,故C错误;D.结合选项C可知,2NH3(1)=N2(g)+3H2(g)△H=2(b+c-a)kJmol-1,故D正确;故选D。
H2(g)=NH3(l)△H=(a-b-c)kJmol-1。A.N2(g)+3H2(g)=2NH3(g)△H=-2(b-a)kJmol-1,故A错误;B.N2(g)+3H2(g)=2NH3(g)△H═-2(b-a)kJmol-1,故B错误;C.物质的量与热量成正比、互为可逆反应的焓变的数值相同而符号相反,则2NH3(1)=N2(g)+3H2(g)△H=2(-a+b+c)kJmol-1,故C错误;D.结合选项C可知,2NH3(1)=N2(g)+3H2(g)△H=2(b+c-a)kJmol-1,故D正确;故选D。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ.如图所示,已知有机物A的相对分子质量是28,它的产量是衡量一个国家石油化工水平的标志,B和D都是日常生活食品中常见的有机物,E是具有浓郁香味、不易溶于水的油状液体,F是一种高聚物,生活中用于制造食物保鲜膜。
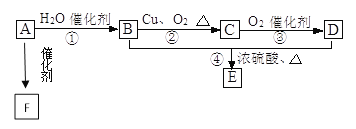
(1)请写出A的结构简式________、C的结构式__________;
(2)请写出B中官能团的电子式__________、D中官能团的名称__________;
(3)请写出下列反应的类型:①__________,②________,④__________。
(4)请写出下列物质转化的化学方程式:A→F ____________; B→C _______;B+D→E __________。
Ⅱ.在实验室可以用如图所示的装置进行B与D的反应,请回答下列问题:
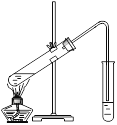
(1)装置中通蒸气的导管要插在_______溶液的液面上方,而不能插入溶液中的原因是为了________,该溶液的作用是____________________________________。
(2)若要把制得的乙酸乙酯分离出来,应采用的实验操作是______。
Ⅲ. 苹果醋是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等药效。苹果酸是苹果醋的主要成分,其结构简式如图所示,请回答下列问题:
![]()
(1)苹果酸的分子式为__________。
(2)1 mol苹果酸与足量金属钠反应,能生成标准状况下的氢气____L。
(3)在一定条件下,苹果酸可能与下列哪些物质发生反应?_________
A.氢氧化钠溶液 B.乙酸 C.碳酸氢钠溶液 D.乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列转化关系中,A是一种日常生活中最常见的溶剂,G气体溶于水显碱性,Y 是胃酸的主要成分,K是不溶于稀硝酸的白色沉淀,反应⑤是工业制X的主要反应之一。1mol B通过反应②得到1mol F,B中F的质量分数为72%。
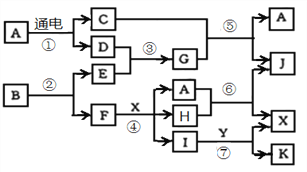
请按要求填空:
(1)B和G含有的共同元素在周期表中的位置是___________________。
(2)过量气体G与氯气反应可以生成一种单质和一种盐,该盐的电子式为 ________________________。
(3)写出反应④的离子方程式,并用单线桥标出电子转移情况__________________________。
(4)反应⑤的化学方程式为___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中不是氧化还原反应的是
A. 3Cl2+6KOH===5KCl+KClO3+3H2O
B. CuO+H2![]() Cu+H2O
Cu+H2O
C. 2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
D. 2AgNO3+BaCl2===2AgCl↓+Ba(NO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据要求填空:
(1)化学反应过程中,不仅有物质的变化,还伴随有能量的变化。根据下图写出反应的热化学方程式:_________________________________。

(2)化学反应速率和化学平衡是化学反应原理的重要组成部分。
将4.0mol PCl3和2.0 mol Cl2充入10 L恒容密闭容器中,在一定条件下发生反应PCl3(g)+Cl2(g)![]() PCl5(g),经2 min达到平衡时,PCl5为0.40 mol。
PCl5(g),经2 min达到平衡时,PCl5为0.40 mol。
①在0~2 min 内,用Cl2 表示的反应速率为:v(Cl2)=_____ mol·L-l·min-1;
②达到平衡时,PCl3的转化率为___________________。
③如果再通入1.0 mol Cl2,相同温度下重新达到平衡时,PCl5的物质的量________________。(填标号)
A.增大 B.减小 C.不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A是一种重要的化工原料。已知A在标准状况下的密度为1.25 g·L-1,B可发生银镜反应。它们之间的转化关系如图:
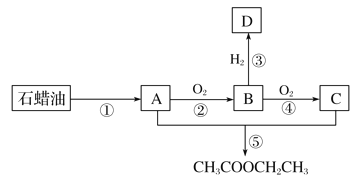
请回答:
(1)有机物B中含有的官能团名称是_______________________________________________。
(2)第⑤步发生加成反应,该反应的化学方程式是_________________________________。
(3)将金属钠与有机物D反应所得的少量产物溶于水,滴加2滴酚酞溶液,水溶液显红色,其原因是__________________(用化学方程式表示)。
(4)下列说法正确的是________。
A.有机物A与D在一定条件下可反应生成乙醚[(CH3CH2)2O]
B.用新制碱性氢氧化铜悬浊液无法区分有机物B、C和D
C.通过直接蒸馏乙酸乙酯和有机物C的混合物,可分离得到纯的乙酸乙酯
D.相同条件下乙酸乙酯在氢氧化钠溶液中水解较在稀硫酸中更完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用浓度为0.100 mol·L-1的NaOH溶液分别逐滴加入到20.00 mL 0.100 0 mol·L-1的HX、HY溶液中,pH随NaOH溶液体积的变化如图。下列说法正确的是( )
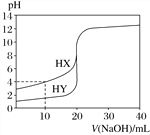
A. V(NaOH)=10.00 mL时,两份溶液中c(X-)>c(Y-)
B. V(NaOH)=10.00 mL时,c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-)
C. V(NaOH)=20.00 mL时,c(OH-)>c(H+)>c(Na+)>c(X-)
D. pH=7时,两份溶液中c(X-)=c(Na+)=c(Y-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资料显示:“氨气可在纯氧中安静燃烧……”。某校化学兴趣小组学生设计如下装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验对比。
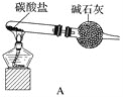
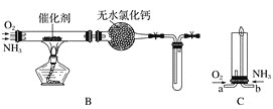
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是____________________;碱石灰的作用是__________________________。
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:
①氨催化氧化的化学方程式__________________;试管内气体变为红棕色,该反应的化学方程式是_______________________。
②停止反应后,立即关闭B中两个活塞。一段时间后,将试管浸入冰水中,试管内气体颜色变浅,请说明可能的原因________________________。
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气生成氮气和水:
①两气体通入的先后顺序是_____________,其理由是______________________。
②氨气燃烧的化学方程式是_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验:
①向Fe2(SO4)3和CuSO4的混合液中加入过量铁粉,充分反应,有红色固体析出,过滤。
②取①中滤液,向其中滴加KSCN溶液,观察现象。
判断下列说法正确的是
A. 氧化性Cu2+>Fe3+
B. ①中所得固体只含铜
C. ①中滤液含有Cu2+和Fe2+
D. ②中不会观察到溶液变红
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com