
科目:高中化学 来源:2016-2017学年江苏省盐城市高二学业水平模拟(一)化学试卷(解析版) 题型:选择题
X、Y、Z、W是原子序数依次增大的短周期主族元素。Y与W同主族,Z所在的族序数等于周期数,X、Y最外层电子数之和为7;X、Z原子的电子数总和与Y、W原子的电子数总和之比为7:12。下列说法正确的是( )
A. 原子半径:r(X)<r(Y)<r(Z)<r(W)
B. Y的简单气态氢化物的热稳定性比W的弱
C. 由X、Y组成的物质与由Y、W组成的物质化合,可能发生氧化还原反应
D. 常温下,Z的单质一定易溶于由X、Y、W三种元素组成的化合物的溶液
查看答案和解析>>
科目:高中化学 来源:2017届河南省南阳、信阳等六市高三第一次联考理综化学试卷(解析版) 题型:选择题
下列离子组在一定条件下能大量共存,且加入相应试剂后所对应的离子方程式正确的是
选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
A | Fe2+、NO3-、K+ | 稀硫酸 | 3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O |
B | Fe3+、I-、ClO- | 氢氧化钠溶液 | Fe3++3OH-=Fe(OH)3↓ |
C | Ba2+、HCO3-、Cl- | 氢氧化钠溶液 | HCO3-+ OH-=CO32-+H2O |
D | Al3+、Cl-、NO3- | 过量氢氧化钠液 | Al3++3OH-=Al(OH)3↓ |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2017届江苏省常州市高三第一次模拟考试化学试卷(解析版) 题型:简答题
铁是最常见的金属材料。铁能形成[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(III)〕 和Fe(CO)x等多种配合物。
(1)基态Fe3+的核外电子排布式为_____,与NO3-互为等电子体的分子是__________。
(2)尿素(H2NCONH2)分子中C、N原子的杂化方式依次为______。C、N、O三种元素的第一电离能由大到小的顺序是______。
(3)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=______。Fe(CO)x常温下呈液态,熔点为-20 .5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于_______(填晶体类型)。
(4)铁有δ、γ、a三种同素异形体,δ、γ、a三种晶胞中铁原子的配位数之比为_______。
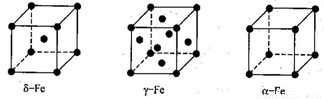
查看答案和解析>>
科目:高中化学 来源:2017届江苏省常州市高三第一次模拟考试化学试卷(解析版) 题型:选择题
已知H2C2O4是二元弱酸,NaHC2O4溶液显酸性。25℃时,将amol/L H2C2O4溶液与b mol/LNaOH 溶液等体积混合(0<a≤0.1, 0<b≤0.1),下列有关溶液中微粒的物质的量浓度关系正确的是
A. a=b时,c(H2C2O4)+c(H+)=c(C2O42-)+c(OH-)
B. 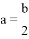 时,c(C2O42-)>c(HC2O4-)>c(H2C2O4)>c(OH-)
时,c(C2O42-)>c(HC2O4-)>c(H2C2O4)>c(OH-)
C. a=2b时,2c(Na+)=c(H2C2O4)+ c(HC2O4-)+ c(C2O42-)
D. a=3b时,c(Na+)+ c(H+)= c(HC2O4-)+ c(C2O42-)+ c(OH-)
查看答案和解析>>
科目:高中化学 来源:2017届江苏省常州市高三第一次模拟考试化学试卷(解析版) 题型:选择题
用H2O2溶液处理含NaCN的废水的反应原理为NaCN+H2O2+H2O=NaHCO3+NH3,已知:HCN酸性比H2CO3弱。下列有关说法正确的是( )
A. 该反应中氮元素被氧化
B. 该反应中H2O2作还原剂
C. 实验室配制NaCN溶液时,需加入适量的NaOH溶液
D. 0.lmol/LNaCN溶液中含HCN和CN-总数目为0.1×6.02×1023
查看答案和解析>>
科目:高中化学 来源:2017届山东省临沂市高三上学期期末考试化学试卷(解析版) 题型:实验题
亚硝酞氯(NOCl,熔点:-64.5℃,沸点:-5.5℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如下图所示:

为制备纯净干燥的气体,下表中缺少的药品是:
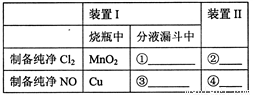
①_______ ②_________③_______④_______
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:

①装置连接顺序为a→________________(按气流自左向右方向,用小写字母表示)。
②装置IV、V除可进一步干燥NO、Cl2外,另一个作用是___________________。
③装置VII的作用是______________________。
④装置VIII中吸收尾气时,NOCl发生反应的化学方程式为____________________。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酞氯和氯气,该反应的化学方程式为________________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省济南市高一下学期开学考试化学试卷(解析版) 题型:实验题
(1)如图所示的装置在实验室中用途比较广泛:
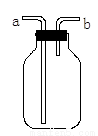
①排空气法收集气体,若收集CO2气体,进气口为_______ (填“a”或“b”)。
②若瓶中装满水,可用于收集下列气体中的_________(选填编号)。
A、NO B、NO2 C、NH3 D、HCl
此时进气口为____________(填“a”或“b”)。
③如果广口瓶中盛放浓硫酸,可用作气体干燥装置,则该装置不可以干燥的气体有____________(选填编号)。
A、HCl B、NH3 C、H2 D、CO
④此装置还可用于除去气体中的杂质气体。若要用此装置除去CO2中混有的少量SO2气体,则装置中应盛放的液体可能是____________(选填编号)。
A、NaOH溶液 B、饱和Na2CO3溶液 C、饱和NaHCO3溶液 D、浓H2SO4
(2)下面是中学化学实验中常见的几种仪器:
A.量筒 B.容量瓶 C.试管 D.圆底烧瓶 E.托盘天平
①其中仪器上要标出使用温度的是_____________(填选项)
②可用作反应容器并能进行加热的是___________(填选项)
③下列操作,使得实验结果偏小的是____________(填选项)
A.称取5.2 gNaCl固体时,将砝码放在左盘,NaCl固体放在右盘
B.配制一定物质的量浓度的NaCl溶液,转移NaCl溶液前,容量瓶中已有少许蒸馏水
C. 配制一定物质的量浓度的NaCl溶液,定容时俯视读数。
D.用量筒量取一定体积的浓硫酸,浓硫酸倒入烧杯后,用蒸馏水继续冲洗量筒内壁并将洗涤液倒入烧杯。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二下学期学业水平模拟化学试卷(解析版) 题型:填空题
A.《化学与生活》
(1)南通是“世界长寿之都”。合理饮食,正确使用药物对人体健康至关重要。
①下列途径不属于补充人体必需的微量元素的是__________(填字母)。
a.乳制品补钙 b.海产品补碘 c.肉制品补硒
②某品牌饼干的配料标签如图所示,下列法正确的是 _________(填字母)。

a.苯甲酸钠是一种着色剂
b.小麦粉中的主要营养物质是葡萄糖
C.食用植物油在人体内水解生成高级脂肪酸和甘油
③“是药三分毒”说明药物在人体内可能产生不良反应,下列药物可能引起的不良反应叙述错误的是__________(填字母)。
a.青霉素一一过敏反应 b.阿司匹林——胃肠道反应
c.复方氢氧化铝——肠胃穿孔
(2)南通地铁2017年底开工建设,工程建设需要大量水泥、钢铁等材料。
①工业上生产水泥的主要原料是黏土和__________,地铁信息传输系统中使用的光导纤维主要成分是 __________。
②钢铁在潮湿的空气中易发生吸氧腐蚀(如右图), 正极电极反应式为_____________。
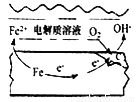
③复合材料“钙塑板”质轻、消声、隔热,以高压聚乙烯、轻质碳酸钙及少量助剂为原料压制而成,聚乙烯的结构简式为__________。
(3)环境友好型城市建设是南通城市规划(2011〜2020年)重点之一。
①2016年,南通市机动车保有量超过200万辆,在机动车尾气系统中装置催化转化器,可将尾气中的NO、CO转化为无害的CO2和__________。
②锌锰电池含有的微量汞单质可用KMnO4吸收液处理。常温下,汞的吸收率及主要反应产物与吸收液的pH的关系如下图。为降低吸收后溶液中Hg2+的浓度,吸收过程中pH> __________。当吸收液的pH<6时,Hg与KMnO4溶液反应的离子方程式为________________。
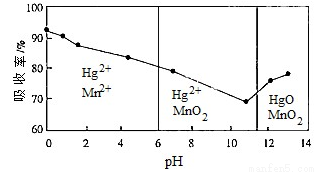
③脱硫、脫碳是指将燃煤中产生的SO2、CO2去除,减少其排放的过程。向煤中加入适量生石灰,可大大减少SO2的排放,并可回收得到_______________;CO2和H2在催化剂及髙温、高压条件下可以合成乙醇,该反应的化学方程式为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com