
| A. | 光伏发电是将太阳能转变为电能 | |
| B. | Ga与N在元素周期表中不处于同一主族 | |
| C. | YAG中钇显+3价 | |
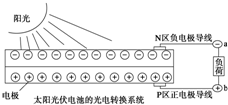
| D. | 上图中N区半导体为负极,P区半导体为正极,电流从a流向b |
分析 A.根据图知,该装置中是将光能先转化为电能,然后电能转化为热能、光能等;
B.Ga元素位于第四周期第IIIA族,N元素位于第二周期第VA族;
C.该化合物中Al元素为+3价、O元素为-2价,根据化合物中各元素化合价代数和为0确定Y元素化合价;
D.电路中的电流从正极沿导线流向负极.
解答 解:A.根据图知,该装置中是将光能先转化为电能,然后电能转化为热能、光能等,所以光伏发电是将太阳能转变为电能,故A正确;
B.Ga元素位于第四周期第IIIA族,N元素位于第二周期第VA族,所以二者不位于同一主族,故B正确;
C.该化合物中Al元素为+3价、O元素为-2价,根据化合物中各元素化合价代数和为0确定Y元素化合价为+$\frac{12×2-5×3}{3}$=+3,故C正确;
D.电路中的电流从正极沿导线流向负极,根据图知,N为负极、P为正极,则电流从b流向a,故D错误;
故选D.
点评 本题考查化学电源新型电池、元素化合价判断、原子周期表等知识点,为高频考点,明确原电池原理、元素周期表结构、原子结构等知识点是解本题关键,侧重考查学生分析判断能力,熟练掌握1-36号元素在周期表中的位置,题目难度不大.


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 陶瓷餐具 | B. | 石英钟表 | C. | 计算机芯片 | D. | 光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2OCH3 | B. | CH3CH(OH)CH3 | C. | CH3CH2COOH | D. | CH3CH2CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 反应物的总键能量低于生成物的总键能 | |
| B. | 该反应是放热反应 | |
| C. | 当A的正反应速率与C的逆反应速率相同时处于平衡状态 | |
| D. | 当A、B、C、D的浓度相同时,反应处于平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸和乙醇的酯化反应 | |
| B. | 乙醇与Na反应 | |
| C. | 乙醇与氧气在Cu作催化剂条件下反应 | |
| D. | 在镍作催化剂的条件下,苯与氢气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “水乳交融,火上浇油”前者包含物理变化,而后者包含化学变化 | |
| B. | “曾青得铁化为铜”发生了化学变化 | |
| C. | “滴水石穿、绳锯木断”不包含化学变化 | |
| D. | “卤水点豆腐,一物降一物”的前半句话与胶体知识有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com