

| A、色氨酸不能与双缩脲试剂发生显色反应 |
| B、色氨酸分子中存在氨基和羧基,可形成内盐,具有较高的熔点 |
| C、色氨酸具有两性,而褪黑素不能与盐酸反应 |
| D、在色氨酸水溶液中,可通过调节溶液的pH使其形成晶体析出 |
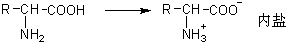 ,该盐是离子化合物,熔点较高,故B正确;
,该盐是离子化合物,熔点较高,故B正确;

科目:高中化学 来源: 题型:
| A、原子半径:Na<Mg<Al |
| B、热稳定性:HCl>H2S>PH3 |
| C、酸性强弱:H4SiO4<H2CO3<CH3COOH |
| D、熔点:金刚石>食盐>干冰 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲烷是最简单的烃,也是含H的质量分数最大的烃 |
| B、通式相同、组成上相差一个或若干个“CH2”原子团的化合物,一定互为同系物 |
| C、有机物一定含C和H两种元素,可能含有O元素 |
| D、含有5个碳原子的有机物,每个分子中最多可形成4个C-C单键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
131 53 |
131 53 |
| A、质量数为131 |
| B、中子数为53 |
| C、质子数为78 |
| D、核外电子数为131 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 可简写为
可简写为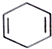 .现有某化合物X的分子结构可表示为
.现有某化合物X的分子结构可表示为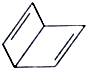 .
.查看答案和解析>>
科目:高中化学 来源: 题型:

| A、浓H2SO4 |
| B、NaCl溶液 |
| C、Ba(OH)2溶液 |
| D、NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
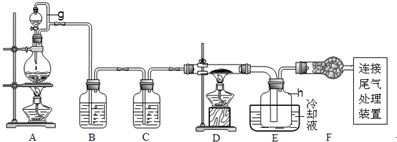
| 物质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸点/℃ | 57.7 | 12.8 | - | 315 | - |
| 熔点/℃ | -70.0 | -107.2 | - | - | - |
| 升华温度/℃ | - | - | 180 | 300 | 162 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、荧光素的分子式为C20H14O5 |
| B、1molX最多能与9mol氢气反应 |
| C、1molX与足量的浓溴水反应,最多消耗4molBr2 |
| D、X能与甲醛发生缩聚反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com