
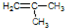 .
. .
. 分析 (1)这种有机物蒸气的质量是同温同压下同体积N2的2倍,则该有机物的相对分子质量为2×28=56,计算2.8g有机物的物质的量,结合生成水和二氧化碳的质量可计算有机物的分子式;
(2)根据分子式和官能团写出结构简式;
(3)若在核磁共振氢谱中只有一个信号峰,说明有机物中一种H.
解答 解:(1)这种有机物蒸气的质量是同温同压下同体积N2的2倍,则该有机物的相对分子质量为2×28=56;
n(A)=$\frac{2.8g}{2×28g/mol}$=0.05mol,
n(C)=n(CO2)=$\frac{8.8g}{44g/mol}$=0.2mol,
n(H)=2n(H2O)=2×$\frac{3.6g}{18g/mol}$=0.4mol,
故有机物分子中含有C原子数目为$\frac{0.2mol}{0.05mol}$=4,含有H原子数目为$\frac{0.4mol}{0.05mol}$=8,
因为12×4+1×8=56=M(A),所以没有O元素;
∴分子式为C4H8,
故答案为:C4H8;
(2)已知分子式为C4H8,如果分子中有一个C=C,则结构简式为:CH2=CHCH2CH3,CH3CH=CH2CH3 ,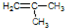 ;
;
故答案为:CH2=CHCH2CH3,CH3CH=CH2CH3 ,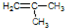 ;
;
(3)在核磁共振氢谱中只有一个信号峰,说明有机物中一种H,则不可能为烯烃,应为环丁烷,结构简式为: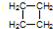 ;其键线式为:
;其键线式为: ;
;
故答案为: .
.
点评 本题考查有机物的推断,侧重考查学生的分析、计算能力,题目难度不大,本题注意根据有机物生成的二氧化碳和水的质量结合相对分子质量可判断有机物的分子式,注意有机物的结构特点.


科目:高中化学 来源: 题型:填空题
 CaCl2
CaCl2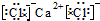 Na2O2
Na2O2 OH-
OH- CH3-
CH3- NaOH
NaOH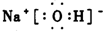
 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
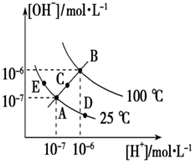 已知水的电离平衡曲线如图所示,试回答下列问题:
已知水的电离平衡曲线如图所示,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某有机物的结构简式如图,取Na、NaOH、新制Cu(OH)2分别与等物质的量的该物质恰好反应(反应时可加热煮沸)则Na、NaOH、新制Cu(OH)2三种物质的物质的量之比为( )
某有机物的结构简式如图,取Na、NaOH、新制Cu(OH)2分别与等物质的量的该物质恰好反应(反应时可加热煮沸)则Na、NaOH、新制Cu(OH)2三种物质的物质的量之比为( )| A. | 6:4:5 | B. | 4:6:5 | C. | 2:3:2 | D. | 2:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.02mol/(L•s) | B. | 1.8mol(L•s) | C. | 1.2mol/(L•s) | D. | 0.18mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
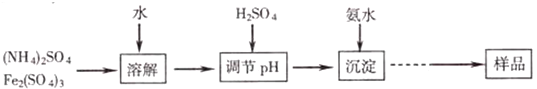
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com