
| A. | 原子半径:X>W>Z>Y | |
| B. | 化合物ZW3溶于水时水解生成一种弱碱和一种强酸 | |
| C. | X的最高价氧化物能与Z的最高价氧化物对应的水化物反应 | |
| D. | 甲、乙混合时生成的白烟为离子化合物,且该化合物只含有离子键 |
分析 Z的最简单氢化物为甲,W的最简单氢化物为乙,乙是双原子分子且甲、乙混合时有白烟生成,则乙为HCl,甲为NH3,所以Z为N元素,W为Cl元素;X与W、Y与Z分别位于同一周期,则X在第三周期、Y在第二周期,Cl的最外层电子数是X与Y的最外层电子数之和,而且X、Y、Z的最外层电子数依次增大,所以X、Y最外层电子数少于5,则X、Y最外层电子数分别为3、4,所以X为Al元素,Y为C元素,据此结合元素化合物的性质与元素周期律分析解答.
解答 解:Z的最简单氢化物为甲,W的最简单氢化物为乙,乙是双原子分子且甲、乙混合时有白烟生成,则乙为HCl,甲为NH3,所以Z为N元素,W为Cl元素;X与W、Y与Z分别位于同一周期,则X在第三周期、Y在第二周期,Cl的最外层电子数是X与Y的最外层电子数之和,而且X、Y、Z的最外层电子数依次增大,所以X、Y最外层电子数少于5,则X、Y最外层电子数分别为3、4,所以X为Al元素,Y为C元素,
A.电子层越多,原子半径越大,电子层数相同时,原子序数越大,半径越小,则原子半径:X>W>Y>Z,故A错误;
B.NCl3水解的化学方程式为NCl3+3H2O=NH3+3HClO,HClO为弱酸,故B错误;
C.X为Al元素,Z为N元素,氧化铝能与硝酸反应生成硝酸铝和水,故C正确;
D.甲为NH3,乙为HCl,二者混合生成氯化铵,氯化铵为离子化合物,含有离子键和共价键,故D错误.
故选C.
点评 本题考查原子结构和元素周期律的关系,涉及化学键判断、元素周期律应用等知识点,正确判断元素是解本题关键,知道原子半径的比较方法,题目难度中等.


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:选择题
| A. | 早在1 000多年前,我国就已采用加热胆矾(CuSO4•5H2O)或绿矾(FeSO4•7H2O) 的方法制硫酸,尽管硫酸的生产工艺几经改进,此方法仍然是工业生产硫酸的主要方法 | |
| B. | 氢能是未来能源结构中最具发展潜力的清洁能源之一.目前已有专家研究出用淀粉或纤维素与水在酶作用下转变为二氧化碳和氢气的方法制氢气.从整个循环来看,利用该方法得到的氢能来源于太阳能 | |
| C. | 在现代化学工业中催化剂的应用十分普遍,对于给定条件下反应物之间能够同时发生多个反应时,理想催化剂还可以大幅度提高目标产物在最终产物中的比率 | |
| D. | 有机反应中的加聚反应符合绿色化学的原则 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 火箭用偏二甲肼(C2H8N2)作燃料,N2O4作还原剂,反应产生巨大能量 | |
| B. | 铝制品由于表面有致密的氧化膜,可以稳定存在于空气中 | |
| C. | 硫是一种生命元素,自然界中的石膏矿、硫铁矿、赤铁矿等都是含“硫”为主的矿石 | |
| D. | 高纯度的SiO2对光有很好的折射和全反射作用,可以制成光电池将光能直接转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最外层电子构型为ns2(n≠1),次外层电子数为8 | |
| B. | 外围电子构型为3d104s2 | |
| C. | 外围电子排布式为ns2np4 | |
| D. | 外围电子排布式为(n-1)d5ns2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 试剂甲 | 试剂乙 | 实验目的 | 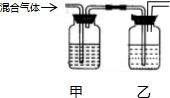 |
| A | NaOH溶液 | 浓硫酸 | 从等体积NO、NH3和NO2中分离出NO | |
| B | KMnO4溶液 | 浓硫酸 | 除去Cl2中的SO2、HCl得干燥Cl2 | |
| C | 溴水 | 浓H2SO4 | 除去乙炔中的H2S和H2O(g) | |
| D | 品红溶液 | 石灰水 | 检验混合气体HCl、SO2、CO2中的SO2和CO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
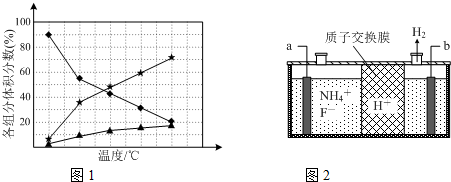
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
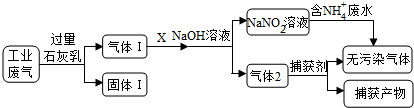
| A. | 固体Ⅰ中主要含有Ca(OH)2、CaCO3、CaSO3 | |
| B. | X可以是空气,且需过量 | |
| C. | 捕获剂所捕获的气体主要是CO | |
| D. | 处理含NH4+废水时,发生反应的离子方程式为:NH4++NO2-=N2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
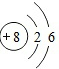 ;
; ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com