

| A. | 该硫酸的物质的量浓度为18.4 mol/L | |
| B. | 该硫酸常用做干燥剂 | |
| C. | 配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL | |
| D. | 该硫酸与等质量的水混合后所得溶液的浓度大于9.2 mol/L |
分析 A、根据c=$\frac{1000ρω}{M}$计算该浓硫酸的物质的量浓度;
B、由A该硫酸是浓硫酸,可以做干燥剂;
C、根据稀释定律,稀释前后溶质硫酸的物质的量不变,据此计算需要浓硫酸的体积;
D.浓硫酸密度大于水,所以等质量混合时硫酸浓度小于原来一半.
解答 解:A、该浓硫酸物质的量浓度为$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L,故A正确;
B、由A该硫酸是浓硫酸,可以做干燥剂,故B正确;
C、令需浓硫酸的体积为V,根据稀释定律,稀释前后溶质硫酸的物质的量不变,则200mL×4.6 mol/L=V×18.4mol/L,解得V=50mL,故C正确;
D.浓硫酸密度大于水,所以等质量的浓硫酸和水混合体积大于浓硫酸的2倍,所以混合时硫酸浓度小于原来一半,故D错误;
故选D.
点评 本题考查物质的量浓度、质量分数的有关计算,难度中等,注意公式的灵活运用,注意D选项中浓度影响物质性质关系.


科目:高中化学 来源: 题型:选择题
| A. | Cu2+、Fe3+、Fe2+、Zn2+ | B. | Fe3+、Fe2+、Zn2+ | ||
| C. | Cu2+、Fe3+、Zn2+ | D. | Cu2+、Fe2+、Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1molSO3的气体体积为22.4L | |
| B. | 1mol铁粉与过量Cl2反应时,转移电子数为2NA | |
| C. | 含有2NA个氧原子的D2O质量为40g | |
| D. | 16gO2分子中含有的氧原子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
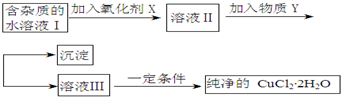
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn为负极,MnO2为正极 | |
| B. | Zn为正极,MnO2为负极 | |
| C. | 工作时电子由MnO2经外电路流向Zn极 | |
| D. | Zn电极发生还原反应,MnO2电极发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽马鞍山二中高一10月阶段测化学卷(解析版) 题型:推断题
为了除去KCl溶液中少量的MgCl2、MgSO4,可选用Ba(OH)2、HCl和K2CO3三种试剂,按下图步骤操作:

(1)写出三种试剂的化学式:A_____ ___,B_ _______,C_ _______。
(2)加过量A的原因是:__________________,
有关反应的化学方程式为:__________________,_________________。
(3)加过量B的原因是:__________________________,
有关反应的化学方程式为:_________________________。
查看答案和解析>>
科目:高中化学 来源:2017届云南省高三上第二次周考化学试卷(解析版) 题型:选择题
科学的假设与猜想是科学探究的先导和价值所在.在下列假设或猜想引导下的探究肯定没有意义的是
A.探究SO2和Na2O2反应可能有Na2SO4生成
B.探究NO和N2O可能化合生成NO2
C.探究NO2可能被NaOH溶液完全吸收生成NaNO2和NaNO3
D.探究向滴有酚酞试液的NaOH 溶液中通入Cl2,酚酞红色褪去的原因是溶液的酸碱性改变还是HCIO的漂白作用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com