
某小组同学以碳棒为电极电解CuCl2溶液时,发现阴极碳棒上除了有红色物质析出外,还有少量白色物质析出。为探究阴极碳棒上的产物,同学们设计了如下实验过程。
(1)对比实验(以碳棒为电极电解下列溶液)
| 电解质溶液 | 阴极析出物质 | |
| 实验1 | CuSO4溶液 | 红色固体 |
| 实验2 | CuSO4和NaCl的混合溶液 | 红色固体和少量白色固体 |
(2)提出假设
①红色物质一定有铜,还可能有Cu2O;
②白色物质为铜的化合物,其化学式可能为________。
(3)实验验证
取电解CuCl2溶液后的阴极碳棒,洗涤、干燥。连接下列装置进行实验,验证阴极产物。
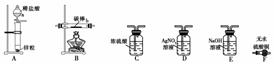
仪器a的名称为________,各装置从左至右的连接顺序为________。
(4)观察现象,得出结论
实验结束后,碳棒上的白色物质变为红色,F中物质不变色,D中出现白色沉淀。
根据现象写出装置B中发生反应的化学方程式:
________________________________________________________________________。
(5)问题讨论
①欲洗去碳棒上的红色和白色物质,可将碳棒插入稀硝酸中,则红色物质消失的离子方程式为______________________;白色物质消失的离子方程式为_________________
______________________。
②实验过程中,若装置B中的空气没有排净就开始加热,可能对实验造成的影响是________________。
解析 (2)对比(1)中实验1和实验2,实验1中没有白色固体物质生成;该白色物质为铜的化合物,而铜的化合物多为黑色、红色,再结合实验2的电解质溶液增加了NaCl,故该白色固体只能是CuCl(氯化亚铜)。(3)漏斗种类较多,包括普通漏斗、分液漏斗、长颈漏斗,解题时要注意区分。用装置A制备氢气,但用稀盐酸制备的氢气中含有HCl和水蒸气两种杂质,前者可用碱液除去(E装置),后者用浓硫酸除去(C装置),但干燥装置应该放后,故装置的连接顺序是A→E→C→B;如果红色物质含有Cu2O,则装置B中会有水生成,可以用装置F中的无水硫酸铜检验,装置D中的AgNO3溶液用于检验Cl-。(4)无水硫酸铜不变色,说明没有Cu2O,AgNO3溶液中出现白色沉淀,说明生成物中含有HCl,故装置B中的反应为CuCl被氢气还原,生成Cu和HCl。(5)①由(4)可知红色物质为Cu,故红色物质消失的反应是铜与稀硝酸反应生成NO;白色物质消失的反应是CuCl被稀硝酸氧化为+2价铜的反应,硝酸被还原为NO。②可燃性气体受热前必须排除装置中的空气,防止发生爆炸;上述装置B中若有空气,则其中的水蒸气会使后续检验水的装置F中的物质出现变色,从而干扰Cu2O是否存在的判断。
答案 (2)②CuCl
(3)分液漏斗 AECBFD(若多选装置,只要合理均可给分)
(4)2CuCl+H2 2Cu+2HCl
2Cu+2HCl
(5)①3Cu+8H++2NO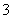 ===3Cu2++2NO↑+4H2O
===3Cu2++2NO↑+4H2O
3CuCl+4H++NO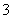 ===3Cu2++3Cl-+NO↑+2H2O
===3Cu2++3Cl-+NO↑+2H2O
②氢气和氧气混合加热可能发生爆炸;空气中的水蒸气会干扰Cu2O是否存在的判断


科目:高中化学 来源: 题型:
新型净水剂高铁酸钾(K2FeO4)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定。
工业上制备K2FeO4的常用方法有两种。
方法Ⅰ:次氯酸盐氧化法。
工艺流程如图所示。
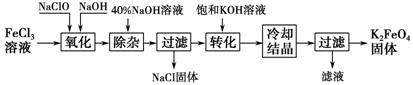
(1)完成“氧化”过程中反应的化学方程式:
FeCl3+____NaOH+____NaClO→____Na2FeO4+____+____。其中氧化剂是____(填化学式)。
(2)“转化”过程中发生反应的化学方程式为________________________________________________________________________
________________________________________________________________________。
(3)上述工艺得到的高铁酸钾常含有杂质,可用重结晶法提纯,操作是:将粗产品用________________溶解,然后________________。
方法Ⅱ:电解法。
以铁为阳极电解氢氧化钠溶液,然后在阳极液中加入KOH。
(4)电解时阳极发生反应生成FeO,该电极反应方程式为________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F六种元素的原子序数依次递增。已知:
①F的原子序数为29,其余的均为短周期主族元素;②E原子价电子(外围电子)排布为msnmpn-1;③D原子最外层电子数为偶数;④A、C原子p轨道的电子数分别为2和4。
请回答下列问题:
(1)下列叙述正确的是________(填序号)。
A.金属键的强弱:D>E
B.基态原子第一电离能:D>E
C.五种元素中,电负性最大的元素是E
D.晶格能:NaCl<DCl2
(2)F基态原子的核外电子排布式为________;与F同一周期的副族元素的基态原子中最外层电子数与F原子相同的元素为________(填元素符号)。
(3)A与C形成的非极性分子中,σ键与π键的个数之比为________;该分子与过量强碱反应生成的酸根离子的空间构型为________。
(4)已知原子数和价电子数相同的分子或离子为等电子体,互为等电子体的微粒结构相同,B 中心原子的杂化轨道类型为________。
中心原子的杂化轨道类型为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用下列实验或实验装置进行的实验中,能达到相应实验目的的是( )
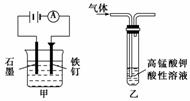
A.装置甲:防止铁钉生锈
B.测定同温同浓度的NaCl和NaF溶液的pH,确定F、Cl两元素的非金属性的强弱
C.装置乙:除去乙烷中混有的乙烯
D.用Ca(OH)2溶液来鉴别Na2CO3溶液和NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列实验事实得出的结论正确的是 ( )。
A.气体 品红溶液褪色
品红溶液褪色
结论:原气体一定是SO2
B.气体 气体
气体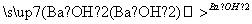 白色沉淀
白色沉淀
结论:原气体一定是烃
C.某溶液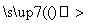 冒白雾
冒白雾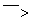 白烟
白烟
结论:原溶液一定是浓盐酸
D.某有色溶液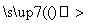 紫色
紫色
结论:原溶液中一定含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室可用如图所示的装置进行CO和CO2混合气体的分离和干燥。已知a为止水夹,b为分液漏斗丙的活塞,可供选用的试剂有NaHCO3溶液、NaOH溶液、NaHS溶液、浓硫酸、无水氯化钙、稀硫酸。试填空回答:

(1)广口瓶甲中应放的试剂为________,广口瓶乙中应放的试剂为________,分液漏斗丙中应放的试剂为________。
(2)第一步应先分离出________,分离时应先关闭________。打开________,发生反应的离子方程式为___________________________________________
__________________。
(3)第二步分离出________时,先关闭________,打开________,发生反应的离子方程式为_____________________________________________________
___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
被称为万能还原剂的NaBH4溶于水并和水反应:NaBH4+2H2O===NaBO2+4H2↑,下列说法中正确的是(NaBH4中H为-1价)( )
A.NaBH4既是氧化剂又是还原剂
B.NaBH4是氧化剂,H2O是还原剂
C.硼元素被氧化,氢元素被还原
D.被氧化的元素与被还原的元素质量之比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
根据FeS2+O2—→Fe2O3+SO2,回答下列问题:
(1)氧化剂________,还原剂________,氧化产物________,还原产物________。
(2)元素化合价升高的元素为________,元素化合价降低的元素为________。
(3)1“分子”还原剂化合价升高总数为________,1“分子”氧化剂化合价降低总数为________。
(4)配平后各物质的系数依次为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com