
| 实 验 操 作 | 现 象 和 结 论 |
| 步骤一:取萃取后的上层清液滴加2滴K4[Fe(CN)6] | 若产生①蓝色沉淀, 则②猜想一不成立; |
| 步骤二:往探究Ⅲ所得溶液中加入少量乙醚,充分振荡、静置分层 | 若③乙醚层呈血红色, 则④猜想二成立; |
分析 (1)根据KI和FeCl3和发生反应:2KI+FeCl3=I2+2KCl+FeCl2,液体呈棕黄色;碘单质易溶于四氯化碳,混合液分层,四氯化碳层呈紫红色;
(2)①根据题目中的信息一和信息二进行解答反应的现象和结论;
②Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀,据此写出反应的离子方程式.
解答 解:(1)活动(Ⅰ)中发生反应:2KI+FeCl3=I2+2KCl+FeCl2,碘溶于水呈棕黄色;碘单质易溶于有机溶剂四氯化碳,所以CCl4能萃取水中的碘,溶液呈紫红色,由于CCl4的密度比水大,所以在混合液的下层,
故答案为:溶液呈棕黄色;溶液分层,下层CCl4层呈紫红色;
(2)ⅰ.因为Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀,所以取萃取后的上层清液滴加2滴K4[Fe(CN)6],若产生蓝色沉淀,说明清夜中含有Fe3+,则猜想一:Fe3+全部转化为Fe2+不成立;步骤二:往探究Ⅲ所得溶液中加入少量乙醚,充分振荡、静置分层,根据Fe(SCN)3在乙醚中的溶解度比在水中大,Fe(SCN)3在乙醚中与在水中呈现的颜色相同,所以乙醚层呈血红色,说明猜想二:生成的Fe(SCN)3浓度极小,其颜色肉眼无法观察成立.
由信息信息一可得:取萃取后的上层清液滴加2-3滴K4[Fe(CN)6]溶液,产生蓝色沉淀,
由信息二可得:往探究活动III溶液中加入乙醚,充分振荡,乙醚层呈血红色,
| 实 验 操 作 | 现 象 和 结 论 |
| 步骤一:取萃取后的上层清液滴加2滴K4[Fe(CN)6] | 若产生蓝色沉淀,则 猜想一不成立 |
| 步骤二:往探究Ⅲ所得溶液中加入少量乙醚,充分振荡、静置分层 | 若乙醚层呈血红色,则 猜想二成立 |
| 实 验 操 作 | 现 象 和 结 论 |
| 若产生蓝色沉淀,则 猜想一不成立 | |
| 若乙醚层呈血红色,则 猜想二成立 |
点评 本题考查了铁离子和亚铁离子的检验、化学反应的限度等,题目难度中等,注意掌握检验铁离子和亚铁离子的方法.


科目:高中化学 来源: 题型:选择题
| A. | 2-甲基丁烷也称为异戊烷 | B. | C4H9Cl有3种同分异构体 | ||
| C. | 由乙烯生成乙醇属于加成反应 | D. | 油脂和蛋白质都属于高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,17g甲基(-14CH3)所含的中子数为8NA | |
| B. | 0.1molFe与0.1molCl2充分反应,转移的电子数为0.2NA | |
| C. | 标准状况下,44.8LNO与22.4LO2混合后气体的分子总数为2NA | |
| D. | 1molNa2O和Na2O2混合物中含有的阴、阳离子总数是3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同周期元素含氧酸的酸性随核电荷数的增加而增强 | |
| B. | 核外电子排布相同的微粒,化学性质也相同 | |
| C. | 原子核都是由质子和中子构成的 | |
| D. | ${\;}_{17}^{35}$Cl与${\;}_{37}^{17}$Cl得电子能力相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它是副族元素 | |
| B. | 它是第七周期元素 | |
| C. | 它的原子核内有97个质子 | |
| D. | 它的一种同位素的核内有108个中子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12g金刚石含有的共价键数为4NA | |
| B. | 1.00molNaCl中约含有6.02×1023个NaCl分子 | |
| C. | 常温下,23g NO2和N2O4的混合物含有1.5NA个原子 | |
| D. | agC2H4和C3H6的混合物所含共用电子对数目为($\frac{a}{7}$+1)NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题




| A. | ①②③④ | B. | ①②③ | C. | ②③④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某有机物燃烧只生成CO2和H2O,且二者的物质的量相等,则此有机物的组成为CnH2n | |
| B. | 相同质量的烃,完全燃烧时,含氢元素质量分数越高的烃,消耗O2量越多 | |
| C. | 常温下分子中氢原子数为4的气态烃,与足量O2完全燃烧时,反应前后气体总体积不变 | |
| D. | 烃在足量的氧气中燃烧并通过浓H2SO4,减少的体积就是生成的水蒸气的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
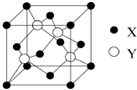 元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1;元素Y基态原子的3p轨道上有5个电子;元素Z的原子最外层电子数是其内层的3倍;元素W基态原子的核外电子共有16种运动状态.
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1;元素Y基态原子的3p轨道上有5个电子;元素Z的原子最外层电子数是其内层的3倍;元素W基态原子的核外电子共有16种运动状态.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com