
【题目】中和滴定是高中化学重要的定量实验。请回答下列问题:
(1)用标准盐酸滴定未知浓度的NaOH溶液,下列情况会造成测定结果偏高的是____(填选项字母)。
A.滴定终点读数时,俯视滴定管刻度
B.盛装NaOH溶液的锥形瓶用蒸馏水洗过,未用NaOH溶液润洗
C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D.滴定前,滴定管尖嘴有气泡,滴定后气泡消失
(2)取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.02mol·L-1的高锰酸钾溶液滴定,发生反应的离子方程式为:____。
(3)一滴定数据如下:
滴定次数 | 待测液体积(mL) | 标准KMnO4溶液体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 3.00 | 23.00 |
第三次 | 25.00 | 4.00 | 24.10 |
①滴定时,该反应速率开始十分缓慢,一段时间后突然加快,这是因为____(填离子)对该反应具有催化作用,KMnO4溶液应装在____(填“酸”或“碱”)式滴定管中;滴定终点的现象是____。
②该草酸溶液的物质的量浓度为_____。
【答案】CD 2MnO4-+5H2C2O4+6H+=10CO2↑+2Mn2++8H2O Mn2+ 酸 当加入最后一滴KMnO4后,锥形瓶中溶液由无色变为红色,且半分钟内不褪色 0.04mol·L-1
【解析】
(1)A.滴定终点读数时,俯视滴定管刻度,其他操作正确,导致V(标准)偏小,根据c(待测)= 分析,测定结果偏低,故A错误;
分析,测定结果偏低,故A错误;
B.盛装NaOH溶液的锥形瓶用蒸馏水洗过,未用NaOH溶液润洗,此操作正确,不影响测定结果,故B错误;
C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗,导致标准液浓度减小,导致V(标准)增大,根据c(待测)= 分析,测定结果偏高,故C正确;
分析,测定结果偏高,故C正确;
D.滴定前,滴定管尖嘴有气泡,滴定后气泡消失,导致V(标准)增大,根据c(待测)= 分析,测定结果偏高,故D正确;
分析,测定结果偏高,故D正确;
故选CD;
(2)在硫酸提供的酸性条件下高锰酸钾与草酸发生反应生成二氧化碳、硫酸锰和水,离子方程式为2MnO4-+5H2C2O4+6H+=10CO2↑+2Mn2++8H2O。
答案为:2MnO4-+5H2C2O4+6H+=10CO2↑+2Mn2++8H2O;
(3)①滴定刚开始时,只有酸性高锰酸钾和草酸反应,反应较慢,随着反应的进行生成Mn2+,一段时间后突然加快,说明反应的产物Mn2+对该反应具有催化作用,加快了反应速率;高锰酸钾溶液具有强氧化性,能够氧化碱式滴定管的橡胶管,所以应该使用酸式滴定管盛装高锰酸钾溶液;滴定结束前混合液为无色,滴定结束时混合液变成了紫红色,所以滴定终点现象为:当加入最后一滴KMnO4后,锥形瓶中溶液由无色变为紫红色,且半分钟内不褪色;
故答案为:Mn2+;酸;当加入最后一滴KMnO4后,锥形瓶中溶液由无色变为紫红色,且半分钟内不褪色。
②三次滴定消耗标准液体积为19.90mL,20.00mL,20.10mL,三次数据均有效,消耗标准液的平均体积为:![]() =20.00mL,高锰酸钾的物质的量为:0.02mol/L×0.020L=0.0004mol,由2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8
=20.00mL,高锰酸钾的物质的量为:0.02mol/L×0.020L=0.0004mol,由2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8
H2O可知,n(H2C2O4)=![]() n(KMnO4)=0.001mol,待测液草酸的物质的量浓度为:
n(KMnO4)=0.001mol,待测液草酸的物质的量浓度为:![]() =0.04 molL-1;
=0.04 molL-1;
故答案为:0.04 molL-1;


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】按要求回答问题:
(1)石灰法是目前应用最广泛的工业废气脱硫方法,过程如下:通过煅烧石灰石得到生石灰,以生石灰为脱硫剂,在吸收塔中与废气中的SO2反应而将硫固定,其产物可作建筑材料。有关反应的化学方程式____________,_____________,___________。
(2)汽车燃料中一般不含氮元素,尾气中所含的NO是如何产生的?说明原因并写出有关方程式___________________________________________________。
(3)治理汽车尾气中NO和CO的一种方法是,在汽车的排气管上装一个催化转化装置,使NO和CO反应,生成无毒的物质。反应的化学方程式是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予了锂离子电池开发的三位科学家。一种锂离子电池的反应式为LixC6+Li1﹣xCoO2![]() 6C+LiCoO2(x<1)其工作原理如图所示。下列说法不正确的是( )
6C+LiCoO2(x<1)其工作原理如图所示。下列说法不正确的是( )

A.放电时A极电极式为:LixC6–xe-=6C+xLi+
B.放电时,若转移0.3mol电子,石墨电极将减重2.1g
C.充电时,A极接外电源的正极
D.该废旧电池进行“放电处理”有利于锂在B极回收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,以硼氢化合物NaBH4(B元素的化合价为+3)和H2O2作原料的燃料电池可用作空军通信卫星电源,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示。下列说法正确的是( )
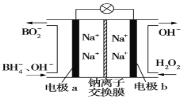
A.电池放电时Na+从b极区移向a极区
B.电极b采用MnO2,MnO2既作电极材料又有催化作用
C.每消耗1molH2O2,转移的电子为1mol
D.该电池的正极反应为:BH4-+8OH--8e-=BO2-+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2 L的密闭容器中,加入1mol X(g)和2 mol Y(g)发生反应:X(g)+mY(g)![]() 3Z(g) ΔH<0,平衡时,X和Y的转化率都是10%。下列叙述不正确的是
3Z(g) ΔH<0,平衡时,X和Y的转化率都是10%。下列叙述不正确的是
A.m=2
B.达平衡时,Z的体积分数为10%
C.达平衡后,保持容器体积不变,加热,容器内压强将增大
D.将平衡后的容器体积压缩至1L,X的浓度为0.45mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴乙烷是无色油状液体沸点为38.4℃,难溶于水,能溶于多种有机溶剂.以NaBr固体、C2H5OH、浓H2SO4、水为原料,对反应后的混合液微热可在烧杯中得到粗产品(溴乙烷),反应装置如图(已略去夹持和加热装置),反应原理:①NaBr+H2SO4(浓)=NaHSO4+HBr;②CH3CH2OH+HBr![]() CH3CH2Br+H2O。下列有关说法正确的是( )
CH3CH2Br+H2O。下列有关说法正确的是( )
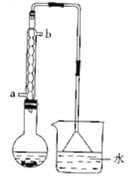
A.烧瓶中试剂加入的先后顺序:浓硫酸、水、溴化钠、乙醇
B.可用 装置代替倒置漏斗装置
装置代替倒置漏斗装置
C.冷凝水从b口进a口出
D.粗产品经水洗涤、蒸发结晶得到纯净的溴乙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含(NH4)2SO4和K2SO4的混合溶液100mL,向其中滴加足量的Ba(OH)2溶液,加热,充分反应,生成的气体在标准状况下体积为448 mL,将反应后的溶液过滤得白色沉淀4.66 g。求原混合溶液中K2SO4的物质的量浓度________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 1L水中溶解了40.0 g NaOH,该溶液的物质的量浓度为1 mol/L
B. 从1L2mol/L的NaCl液中取出0.5L,取出的该溶液的浓度为1mol/L
C. 中和100 mL 1mol/L的H2SO4溶液,需NaOH8.0g
D. 配制500mL0.5mol/L的CuSO4溶液,需40.0g胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)利用如图装置,进行NH3与金属氧化物MxOy反应生成M、N2、H2O,通过测量生成水的质量来测定M的相对原子质量。a中试剂是浓氨水。

①仪器a的名称为_________,仪器b中装入的试剂可以是___________。
②按气流方向正确的装置连接顺序为_________(填字母,装置可重复使用)。
(2)亚硝酸钠是一种工业盐,在生产、生活中应用广泛。现用下图所示装置(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物成分。
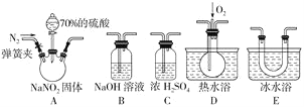
已知:ⅰ.NO+NO2+2OH-=2NO2-+H2O
ⅱ.气体液化的温度:NO2(21℃)、NO(-152℃)
①反应前应打开弹簧夹,先通入一段时间氮气,目的是________________。
②为了检验装置A中生成的气体产物,仪器的连接顺序(从左向右连接):A→_________;组装好仪器后,接下来进行的操作是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com