
| A. | Na投入到足量的盐酸中:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 向碳酸氢钠溶液中加入过量氢氧化钙溶液:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| C. | 三氯化铁溶液中加入铜粉:Fe3++Cu═Fe2++Cu2+ | |
| D. | 将氯气通入冷的氢氧化钠溶液中:Cl2+2OH-═Cl-+ClO-+H2O |
分析 A.Na投入到足量的盐酸中反应生成氯化钠和氢气;
B.氢氧化钙过量,反应生成碳酸钙和氢氧化钠和水;
C.电荷不守恒;
D.二者反应生成氯化钠和次氯酸和水.
解答 解:A.Na投入到足量的盐酸中,离子方程式:2Na+2H+═2Na++H2↑,故A错误;
B.向碳酸氢钠溶液中加入过量氢氧化钙溶液,离子方程式:HCO3-+Ca2++OH-═CaCO3↓+H2O,故B错误;
C.三氯化铁溶液中加入铜粉,离子方程式:2Fe3++Cu═2Fe2++Cu2+,故C错误;
D.将氯气通入冷的氢氧化钠溶液中,离子方程式:Cl2+2OH-═Cl-+ClO-+H2O,故D正确;
故选:D.
点评 本题考查离子方程式的书写,本题注意水、氨水、次氯酸都为弱电解质,应写成化学式,书写离子方程式时要注意电荷守恒、质量守恒,注意反应遵循客观事实,题目难度不大.


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源: 题型:选择题
| A. | 甲烷的燃烧热为890.3 kJmor-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+202 (g)═C02 (g)+2H20(g)△H=-890.3kJ mol-1 | |
| B. | 500 V、30MPa下,将0.5molN2和1.5 molH2置于密闭的容器中充分反应生成 NH3(g),放热19.3kJ,其热化学方程式为 N2(g)+3H2 (g)$?_{500℃、30Mp}^{催化剂}$2NH3(g)△H=-38.6 kJmol-1 | |
| C. | 同温同压下,等物质的量的H2与足量的C12在光照和点燃条件下充分反应,所产生的热量相同 | |
| D. | 已知中和热为57.3 kJ/mol,则稀硫酸与氢氧化钡溶液反应的热化学方程式为 2H+(aq)+SO42-(aq)+Ba2+(aq)+20H-(aq)=BaS04 (s)+2H20(l)△H=-57.3kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
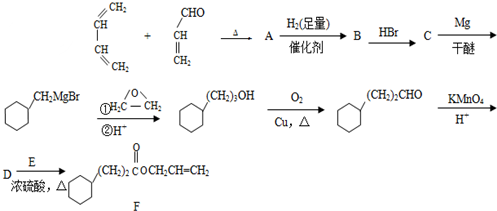

 ,A中所含官能团的名称是醛基、碳碳双键;
,A中所含官能团的名称是醛基、碳碳双键; ;
; ;
;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
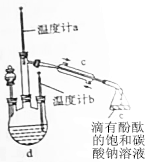 乙酸丁酯沸点、溶解性如下表.
乙酸丁酯沸点、溶解性如下表.| 物质 | 乙酸 | 1-丁醇 | 乙酸丁酯 | 90%浓硫酸 |
| 沸点 | 117.9℃ | 117.2℃ | 126.3℃ | 338.0℃ |
| 溶解性 | 溶于水和有机溶剂 | 溶于水和有机溶剂 | 微溶于水,溶于有机溶剂 | 与水混溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝酸的摩尔质量是63 g | |
| B. | 1 mol CO的质量是28 g | |
| C. | 4 g氢气对应的摩尔质量是2 g氢气对应的摩尔质量的2倍 | |
| D. | 铁的摩尔质量在数值上等于铁原子的相对原子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钠水溶液在电流的作用下电离出Na+和Cl- | |
| B. | 硫酸钡难溶于水,但硫酸钡属于强电解质 | |
| C. | 二氧化碳溶于水能部分电离,故二氧化碳属于弱电解质 | |
| D. | 硫酸氢钠在水中的电离方程式可表示为NaHSO4═Na++HSO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量N2和CO2中,共用电子对的个数比为3:4 | |
| B. | 该反应中化合价变化的有N和C元素 | |
| C. | 氧化剂与还原剂的物质的量之比为1:1时,NOx中氮元素的化合价为+2价 | |
| D. | 当x=2时,每生成1mol N2,转移电子数为4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaNO2发生的是氧化反应 | B. | 生成1molN2时转移的电子数为3mol | ||
| C. | NH4Cl中的N元素被还原 | D. | N2既是氧化剂有事还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 植树造林,加强绿化 | B. | 合理使用化肥和农药 | ||
| C. | 工业“三废”经处理后再排放 | D. | 矿物产品的综合开发和利用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com