
| A. | 镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料 | |
| B. | 石英玻璃、陶瓷都属于硅酸盐产品 | |
| C. | 做衣服的棉、麻、蚕丝的成分都是纤维素 | |
| D. | 牛油和花生油在碱性条件下水解产物相同 |
分析 A、镧镍合金是金属金属和金属形成的合金材料,能大量吸收H2形成金属氢化物,目前可以解决氢气的储存和运输问题;
B、石英玻璃的主要成分是二氧化硅,不属于硅酸盐产品;
C、蚕丝则主要成分是蛋白质;
D、牛油是饱和高级脂肪酸甘油酯,花生油含不饱和高级脂肪酸甘油酯;
解答 解:A、储氢材料是一类能可逆地吸收和释放氢气的材料,镧镍合金能大量吸收H2形成金属氢化物,是目前解决氢气的储存和运输问题的材料,故A正确;
B、含有硅酸根离子的盐属于硅酸盐,传统硅酸盐产品包括:普通玻璃、陶瓷、水泥,石英玻璃的主要成分是二氧化硅是氧化物,不属于硅酸盐产品,故B错误;
C、因棉花的成分是纤维素,羊毛、蚕丝的成分是蛋白质,故C错误;
D、牛油是饱和高级脂肪酸甘油酯,花生油含不饱和高级脂肪酸甘油酯,故产物不同,故D错误.
故选A.
点评 本题考查油脂、糖类和蛋白质的性质以及醋酸盐产品,题目难度不大,掌握物质性质和相关概念是解题的关键.


科目:高中化学 来源: 题型:选择题
| 酸 | CH3COOH | HCN | HF | H2CO3 |
| 电离常数 | 1.8×10-5 | 4.9×10-10 | 6.6×10-4 | Ka1=4.3×10-2Ka2=5.6×10-11 |
| A. | 5种钠盐溶液pH大小关系pH(Na2CO3)>pH(NaCN)>pH(NaHCO3)>pH(CH3COONa)>pH(NaF) | |
| B. | 2mol•L-1HCN与1mol•L-1NaOH溶液等体积混合后的溶液中:c(CN-)<c(Na+)<c(HCN) | |
| C. | 向Na2CO3溶液中滴加过量的HCN溶液;2HCN+Na2CO3=2NaCN+CO2↑+H2O | |
| D. | 含等物质的量的Na2CO3、NaHCO3的混合液中:2c(Na+)=3c(CO32-)+3C(HCO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 白磷、硅 | B. | 碳化硅、硫酸钠 | C. | 水晶、金刚石 | D. | 碘、汞 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
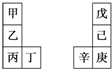 甲~辛等元素在周期表中的相对位置如表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )
甲~辛等元素在周期表中的相对位置如表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )| A. | 丙与庚的原子序数相差3 | |
| B. | 气态氢化物的热稳定性:戊>己>庚 | |
| C. | 乙所在周期元素中,其简单离子的半径最大 | |
| D. | 乙的单质在空气中燃烧生成的化合物只含离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
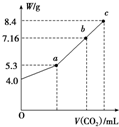 钠有多种化合物,如氧化钠、过氧化钠、氢氧化钠、碳酸钠、碳酸氢钠等等,这些物质在实际生活中有广泛的应用,一定条件下相互间能进行转化.完成下列计算:
钠有多种化合物,如氧化钠、过氧化钠、氢氧化钠、碳酸钠、碳酸氢钠等等,这些物质在实际生活中有广泛的应用,一定条件下相互间能进行转化.完成下列计算:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
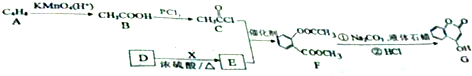
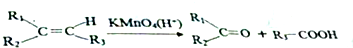
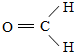 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
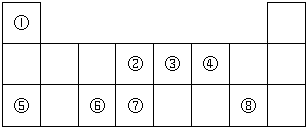
 ,该氢化物中含有的化学键是极性共价键.
,该氢化物中含有的化学键是极性共价键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、CH3COO-、Ca2+、Cl- | B. | Fe3+、Ag+、SO42-、NO3- | ||
| C. | Cu2+、H+、S2-、NO3- | D. | C6H5OH、Fe3+、K+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、M两元素最简单氢化物的稳定性:X<M | |
| B. | Z、W、M的单质均能与稀硫酸反应制取氧气,且反应剧烈程度依次减弱 | |
| C. | Y的最高价含氧酸的化学式为H2YO2 | |
| D. | W和M的氧化物均可作耐高温材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com