
��15�֣��ں� b mol AlCl3����Һ�м��뺬 a mol NaOH����Һ��
��1������a��3b�������ι�����ʱ������Al��OH��3 ���������ʵ���Ϊ mol��
��2������a��4bʱ������Al��OH��3 ���������ʵ���Ϊ mol��
��3������3��a/b��4ʱ�����г������ɣ������в��ֳ����ܽ⣬��ʱAl��OH��3�����ʵ���Ϊ mol��
��4������д��AlCl3��NaOH��Һ��Ӧʱ�����йص����ӷ���ʽ��ѧ����ʽ��
�٣�
�ڣ�
�ۣ�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������ | K+ Na+ Cu2+ Al3+ | ||||||
| ������ | SO
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
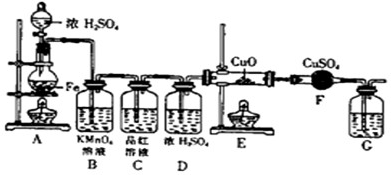
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ���������ʮ���и߶���ѧ�����п��Ի�ѧ���ģ��Ծ� ���ͣ������
��15�֣��ں� b mol AlCl3����Һ�м��뺬 a mol NaOH����Һ��
��1������a��3b�������ι�����ʱ������Al��OH��3 ���������ʵ���Ϊ mol��
��2������a��4bʱ������Al��OH��3 ���������ʵ���Ϊ mol��
��3������3��a/b��4ʱ�����г������ɣ������в��ֳ����ܽ⣬��ʱAl��OH��3�����ʵ���Ϊ mol��
��4������д��AlCl3��NaOH��Һ��Ӧʱ�����йص����ӷ���ʽ��ѧ����ʽ��
�٣�
�ڣ�
�ۣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com