
反应A(g)+2B(g)![]() C(g),按温度每升高10℃,化学反应速率增大到原来的2倍来计算,若某反应由50℃升温到80℃,反应速率增大到原来的:
C(g),按温度每升高10℃,化学反应速率增大到原来的2倍来计算,若某反应由50℃升温到80℃,反应速率增大到原来的:
A.4倍 B.6倍 C.8倍 D.9倍
 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
在一个容积不变的反应器中,要求调节体系的温度使下列反应达到平衡时,保持容器内气体的总物质的量为12 mol。
已知反应A(g)+2B(g) ![]() 2C(g),现向容器中加入6.5 mol A、x mol B、2.0 mol C。
2C(g),现向容器中加入6.5 mol A、x mol B、2.0 mol C。
(1)若x=5.5时,需要降低体系的温度使反应在平衡时达到题设条件,则正反应为_______(填“吸热”或“放热”)反应。
(2)欲使起始反应维持向逆反应方向进行,则x的取值范围为_________。
(3)在一定温度下的上述平衡体系中,另按1∶2 的物质的量之比通入D和E两种气体(此时容器内气体的总物质的量不要求保持12 mol),按下式反应:D(g)+E(g) ![]() 2F(g),当反应达到平衡时,D在这三种物质中的体积分数为p%。若向容器中投入m mol D\,n mol F和一定量的E,在这三种物质新的平衡体系中,D的体积分数仍为p%。则投入E的物质的量为________mol(设A、B、C与D、E、F之间均不反应)。
2F(g),当反应达到平衡时,D在这三种物质中的体积分数为p%。若向容器中投入m mol D\,n mol F和一定量的E,在这三种物质新的平衡体系中,D的体积分数仍为p%。则投入E的物质的量为________mol(设A、B、C与D、E、F之间均不反应)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)Ⅰ、(1)现有浓度均为0.1 mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵,则①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号) 。
(2)已知某温度下,纯水中的C(H+)=5×10-7mol/L,则此时溶液的C(OH-)为 mol/L;若温度不变,将pH=11的NaOH溶液a L与pH=1的H2SO4的溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a∶b= 。
Ⅱ、在一个容积固定的密闭容器中,要求通过调节体系的温度使反应A(g)+2B(g)![]() 2C( g)达到平衡时,保持容器内气体的总物质的量为12mol。现向反应容器中加入6.5molA,xmolB,2.0molC。
2C( g)达到平衡时,保持容器内气体的总物质的量为12mol。现向反应容器中加入6.5molA,xmolB,2.0molC。
⑴若x=5.5时,需要降低体系温度使反应在平衡时达到题设条件,则正反应是 热反应。
⑵欲使反应维持向逆反应方向移动,则x的取值范围为 。
⑶在一定温度下的上述平衡体系中,另按1∶2的物质的量之比充入D、E两种气体(此时容器中的气体的总物质的量不要求保持12mol),按D(g)+E(g) 2F(g)发生反应。当反应达到平衡时,D在这三种物质的混合体系中的体积分数为p%。若向容器中投入m molD,n molF和一定物质的量的E,在这三种物质的新的平衡体系中,D的体积分数仍为p%,则所投入E的物质的量为 (用m、n表示;设A、B、C和D、E、F之间均不发生反应)。
2F(g)发生反应。当反应达到平衡时,D在这三种物质的混合体系中的体积分数为p%。若向容器中投入m molD,n molF和一定物质的量的E,在这三种物质的新的平衡体系中,D的体积分数仍为p%,则所投入E的物质的量为 (用m、n表示;设A、B、C和D、E、F之间均不发生反应)。
查看答案和解析>>
科目:高中化学 来源:2014届云南省高二下学期期中考试化学试卷(本部)(解析版) 题型:填空题
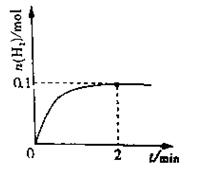
(1)(3分)一定温度下,向4L密闭容器中加入1molHI(g),发生2HI(g) H2(g)+I2(g),H2物质的量随时间的变化如图所示。0~2min内的平均反应速率v(HI)= mol/(L·min)。
H2(g)+I2(g),H2物质的量随时间的变化如图所示。0~2min内的平均反应速率v(HI)= mol/(L·min)。
(2)(3分)①某温度下,反应SO2(g)+ 1/2O2(g)  SO3 (g) 的平衡常数K1=50,在同一温度下,反应2SO3(g)
SO3 (g) 的平衡常数K1=50,在同一温度下,反应2SO3(g)  2SO2(g) + O2(g)的平衡常数K2的值为 。
2SO2(g) + O2(g)的平衡常数K2的值为 。
(3)(3分)某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下反应:3A(g)+2B(g) 4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6 mol C,且反应的前后压强之比为5∶4(相同的温度下测量)。则该反应的化学平衡常数:
4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6 mol C,且反应的前后压强之比为5∶4(相同的温度下测量)。则该反应的化学平衡常数:
K= 。(列出算式,代入数据即可)
(4)(7分)下图表示373K时,反应A(g)  2B(g)在前110s内的反应进程。
2B(g)在前110s内的反应进程。
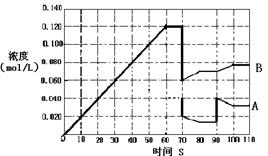
①373K时反应进行到70s时,改变的条件可能是________,反应进行到90s时,改变的条件可能是_____。
A.加入催化剂 B.扩大容器体积 C.升高温度 D.增大A的浓度
②请在图中画出反应物A在0~70秒时的浓度变化曲线。
查看答案和解析>>
科目:高中化学 来源:2012年沪科版高中化学6.1提示化学反应速率和平衡之谜练习卷(解析版) 题型:选择题
在恒温恒容的容器中进行反应
A(g)  2B(g)+C(g);若反应物浓度由0.1mol?L-1降到0.06mol?L-1需20s,那么由0.06mol?L-1降到0.024mol?L-1,需反应的时间为
2B(g)+C(g);若反应物浓度由0.1mol?L-1降到0.06mol?L-1需20s,那么由0.06mol?L-1降到0.024mol?L-1,需反应的时间为
A.等于18s B.等于12s C.大于18s D.小于18s
查看答案和解析>>
科目:高中化学 来源:09-10年台州市高二下学期期末考试化学卷 题型:填空题
(14分) 对于反应A(g) 2B(g) DH>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示。回答下列各题。

(1)根据曲线图,分析下列说法正确的是 ▲ (填字母) 。
A.a、c两点的反应速率:a 〉c
B.由状态b到状态a,可以通过加热的方法
C.b、c两点A气体的转化率相等
(2)上述反应在密闭容器(定容)中进行,达到平衡状态的标志是 ▲ (填字母) 。
A.单位时间内生成n mol A的同时分解2n molB
B.两种气体的体积分数不再改变
C.v正(A)=2v逆(B)
D.混合气体的密度不再发生变化
E.混合气体的压强不再发生变化
(3)若上述反应达平衡时,B气体的平衡浓度为0.1 mol·L-1 ,通过减小体积来增大体系的压强(温度保持不变),重新达平衡后,B气体的平衡浓度 ▲ 0.1 mol·L-1(填“〉”、“〈”或“=”) 。
(4)在100℃时,将0.40mol的B气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表的数据:
|
时间(s) |
0 |
20 |
40 |
60 |
80 |
|
n(B)/mol |
0.40 |
n1 |
0.26 |
n3 |
n4 |
|
n(A)/mol |
0.00 |
0.05 |
n2 |
0.08 |
0.08 |
① 在上述条件下,从反应开始至40s时,以A气体表示的该反应的平均反应速率为 ▲ ;
② 上表中n3 ▲ n4(填“〉”、“〈”或“=”),反应A(g) 2B(g)在100℃时的平衡常数K的值为 ▲ ,升高温度后,反应2B(g) A(g)的平衡常数K的值 ▲ (填“增大”、“减小”或“不变”);
③ 若在相同情况下最初向该容器中充入的是A气体,要达到上述同样的平衡状态,A气体的起始浓度为 ▲ mol·L-1 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com