
下列可逆反应达平衡后,改变反应条件,其变化趋势正确的是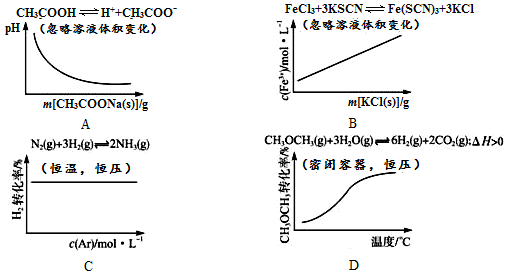
D
解析试题分析:A、醋酸是弱酸,存在电离平衡CH3COOH CH3COO-+H+,加入醋酸钠固体,增大溶液中的CH3COO-浓度,乙醇醋酸的电离,所以溶液的酸性降低,pG增大,A不正确;B、根据离子方程式Fe3++3SCN-=Fe(SCN)3可知,氯离子和钾离子并不参与反应,所以加入氯化钾固体后平衡并不,因此铁离子的浓度不变,B不正确;C、在恒温恒压下充入Ar,则容器的容积增大,物质的浓度降低,所以合成氨反应向逆反应方向移动,反应物的转化率降低,C不正确;D、该反应的正方应是吸热反应,升高温度平衡向正反应方向移动,因此反应物的转化率增大,D正确,答案选D。
CH3COO-+H+,加入醋酸钠固体,增大溶液中的CH3COO-浓度,乙醇醋酸的电离,所以溶液的酸性降低,pG增大,A不正确;B、根据离子方程式Fe3++3SCN-=Fe(SCN)3可知,氯离子和钾离子并不参与反应,所以加入氯化钾固体后平衡并不,因此铁离子的浓度不变,B不正确;C、在恒温恒压下充入Ar,则容器的容积增大,物质的浓度降低,所以合成氨反应向逆反应方向移动,反应物的转化率降低,C不正确;D、该反应的正方应是吸热反应,升高温度平衡向正反应方向移动,因此反应物的转化率增大,D正确,答案选D。
考点:考查外界条件对平衡状态的影响以及图像识别与判断


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:单选题
向四个体积相同的密闭容器中分别充人一定量的SO2和O2,开始反应是,按正反应速率由大到小的顺序排列正确的是
甲:在 500℃时,SO2和O2各 10 mol 反应
乙:在500℃时,用V2O5作催化剂,SO2和O2各10 mol反应
丙:在450℃时,8 mol SO2和5 mol O2反应
丁:在500℃时,8 mol SO2和5 mol O2反应
| A.乙、甲、丁、丙 | B.乙、申、丙、丁 |
| C.甲、乙、丙、丁 | D.丁、丙、乙、甲 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
反应N2+3H2 2NH3刚开始时,N2的浓度为3 mol/L,H2的浓度为5 mol/L,3 min后测得NH3浓度为0.6 mol/L,则此时间内,下列反应速率表示正确的是
2NH3刚开始时,N2的浓度为3 mol/L,H2的浓度为5 mol/L,3 min后测得NH3浓度为0.6 mol/L,则此时间内,下列反应速率表示正确的是
| A.v(NH3)="0.2" mol/(L·s) | B.v(N2)="1.0" mol/(L·min) |
| C.v(H2)="1.67" mol/(L·min) | D.v(H2)="0.3" mol/(L·min) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某实验小组以H2O2分解为例,研究浓度、催化剂对反应速率的影响。在常温下按照如下方案完成实验。实验②的反应物应为
| 实验编号 | 反应物 | 催化剂 |
| ① | 10 mL 2% H2O2溶液 | 无 |
| ② | | 无 |
| ③ | 10 mL 5% H2O2溶液 | MnO2固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
足量的锌与酸反应,欲使制取氢气的反应速率尽可能大,选用的反应条件正确的组合是
①锌粒 ②锌粉 ③加少量的硫酸银的饱和溶液 ④1mol/L的盐酸 ⑤5mol/L的硝酸
⑥1mol/L的硫酸 ⑦加热 ⑧加大量的硫酸铜晶体 ⑨不断振荡 ⑩加大体系的压强
| A.②③⑥⑦⑨ | B.①③⑤⑦⑩ | C.②④⑥⑦⑧⑨ | D.②⑦⑧⑨⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
T℃时在2L刚性密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为Tl和T2时,Y的体积分数 (Y)与时间的关系如图2所示。则下列结论错误的是
(Y)与时间的关系如图2所示。则下列结论错误的是
A.容器中发生的反应可表示为:3X(g)+Y(g) 2Z(g) 2Z(g) |
| B.反应进行的前4min内,用X表示的反应速率v(X)=0.15mo1?(L?min)—1 |
| C.保持其他条件不变,升高温度,反应的化学平衡常数K减小 |
| D.若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列事实不能用勒夏特列原理解释的是
| A.热的纯碱溶液比冷的纯碱溶液洗涤油污效果更好 |
| B.配制FeCl3溶液时,在溶液中加入少量稀盐酸 |
| C.等质量粉末状与块状碳酸钙分别与同浓度的盐酸反应,粉末状比块状的反应快 |
| D.新制的氯水在光照条件下颜色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将 4 mol A 气体和 2 mol B 气体在 2 L 的定容容器中混合并在一定条件下发生如下反应 2A(气)+B(气) 2C(气);△H<0 ,经 2 s(秒)后测得 C 的浓度为0.6 mol·L-1 ,现有下列几种说法:
2C(气);△H<0 ,经 2 s(秒)后测得 C 的浓度为0.6 mol·L-1 ,现有下列几种说法:
① 用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1
② 达到平衡状态时,升高温度,则该化学平衡向左移动,同时化学平衡常数K也减小;
③ 2 s 时物质 A 的转化率为70% ④ 达到平衡状态时,增加A物质的量A和B转化率都提高。⑤当各物质浓度满足c(A)="2c(B)=" c(C)时,该反应达到了平衡状态;其中正确的是( )
A.①③ B. ①② C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一定条件下,在一固定容积的密闭容器中发生如下反应:N2(g)+3H2(g) 2NH3(g),若开始时只充入2a mol NH3,达到平衡时,混合气体的压强比起始时增大了40%。若同条件下开始时充入a mo N2和3a mol H2的混合气体,求:
2NH3(g),若开始时只充入2a mol NH3,达到平衡时,混合气体的压强比起始时增大了40%。若同条件下开始时充入a mo N2和3a mol H2的混合气体,求:
(1)达到平衡时H2的转化率;
(2)平衡时NH3在混合气体中的体积分数。
一定条件下,在一固定容积密闭容器中发生如下反应:N2(g)+3H2(g) 2NH3(g),若开始时只充入2a mol NH3,达到平衡时,混合气体的压强比起始时增大了40%。若开始时充入a mo N2和3a mol H2的混合气体,求:
2NH3(g),若开始时只充入2a mol NH3,达到平衡时,混合气体的压强比起始时增大了40%。若开始时充入a mo N2和3a mol H2的混合气体,求:
(1)达到平衡时H2的转化率;
(2)平衡时NH3在混合气体中的体积分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com