
| A、氢氧化钠可用于治疗胃酸过多 |
| B、O3用于饮用水消毒 |
| C、水玻璃浸泡过的木材既能防腐又能耐火 |
| D、Si用于制造光电池 |


科目:高中化学 来源: 题型:
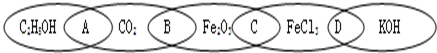
| Fe |
| 气体丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
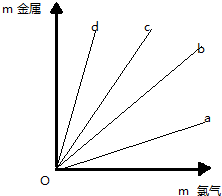 ①舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一.请写出该方法制取氯气的离子方程式:
①舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一.请写出该方法制取氯气的离子方程式:查看答案和解析>>
科目:高中化学 来源: 题型:
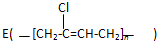 的合成路线如下:
的合成路线如下:
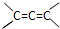 是不稳定结构.
是不稳定结构.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不慎将酸液溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
| B、不慎将浓碱液沾到皮肤上,要立即用大量的稀硫酸冲洗 |
| C、酒精灯着火时可用水扑灭 |
| D、稀释浓硫酸时,可往装有一定体积浓硫酸的量筒中,慢慢加入水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
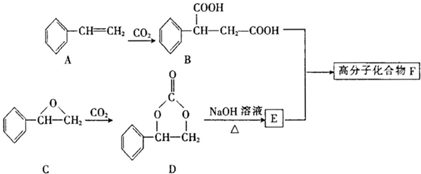
查看答案和解析>>
科目:高中化学 来源: 题型:
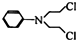
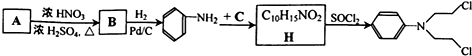
| SOCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
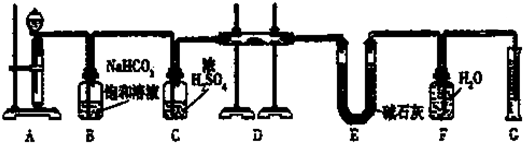
查看答案和解析>>
科目:高中化学 来源: 题型:
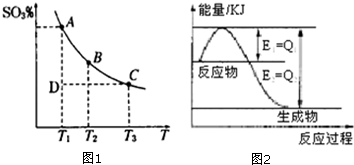 运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义.
运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com