
【题目】下列实验操作能达到目的的是( )
选项 | 实验目的 | 实验操作 |
A | 配制100 g10%的NaOH溶液 | 称取10 gNaOH溶于90 g蒸馏水中 |
B | 验证“84消毒液”呈碱性 | 用pH试纸测量溶液的pH |
C | 检验溶液中是否含有Na+ | 用洁净的玻璃棒蘸取溶液灼烧,观察火焰颜色 |
D | 从溴水中获得溴单质 | 利用SO2将Br2吹出后,富集、还原、分离 |
A.AB.BC.CD.D
【答案】A
【解析】
A. 溶液质量是90 g+10g=100 g,溶质的质量分数为![]() ×100%=10%,A正确;
×100%=10%,A正确;
B. “84消毒液”有效成分是NaClO,该物质具有氧化性,会将pH试纸氧化漂白,因此不能用pH试纸测量该溶液的pH,以验证溶液的碱性,B错误;
C. 玻璃的成分中含有Na2SiO3,含有钠元素,因此用玻璃棒进行焰色反应实验,就会干扰溶液中离子的检验,要使用铂丝或光洁无锈的铁丝进行焰色反应,C错误;
D. 向溴水中加入CCl4充分振荡后,静置,然后分液,就可从溴水中获得溴单质。若向溴水中通入SO2气体,就会发生反应:SO2+Br2+2H2O=H2SO4+2HBr,不能将单质溴吹出,D错误;
故合理选项是A。


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】某学习小组探究SO2与Cu(OH)2悬浊液的反应。
实验Ⅰ:向NaOH溶液中加入浓CuCl2溶液,制得含Cu(OH)2的悬浊液,测溶液pH≈13。向悬浊液中通入SO2,产生大量白色沉淀,测溶液pH≈3。推测白色沉淀中可能含有Cu+、Cu2+、Cl- 、SO42-、SO32-、HSO3-。
已知: i. Cu(NH3)42+(蓝色);Cu+![]() Cu(NH3)2+(无色);Cu+
Cu(NH3)2+(无色);Cu+![]() Cu+Cu2+
Cu+Cu2+
ii. Ag2SO4微溶于水,可溶于一定浓度的硝酸。
实验Ⅱ:

(1)①通过“白色沉淀A”确定一定存在的离子是____________________。
②判断白色沉淀中金属离子仅含有Cu+、不含Cu2+的实验证据是____________________。
③用以证实白色沉淀中无SO42-、SO32-、HSO3-的试剂a是____________________。
④生成CuCl的离子方程式是____________________。
(2)小组同学基于上述实验认为: SO2与Cu(OH)2悬浊液能发生氧化还原反应不仅基于本身的性质,还受到“生成了沉淀促进了氧化还原反应的发生”的影响。设计实验验证了此观点。
①用实验Ⅰ方法制得含Cu(OH)2的悬浊液,过滤、洗涤获取纯净的Cu(OH)2固体。检验Cu(OH)2固体是否洗涤干净的方法是____________________。
编号 | 实验 | 现象 |
III | 向Cu(OH)2固体中加入一定量的水,制得悬浊液(pH≈8),向悬浊液中通入SO2 | a. 底部产生少量浅黄色沉淀,慢慢消失 b. 静置,底部产生少量红色固体 |
IV | 向CuSO4溶液中通入SO2 | 无沉淀产生 |
②经确认浅黄色沉淀是CuOH,红色固体是Cu,证明SO2与Cu(OH)2悬浊液发生了氧化还原反应。最终生成Cu的原因是____________________。
③由实验III、IV可以得出的结论除“生成了沉淀促进了氧化还原反应的发生” 外还有____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,在实验室中通常利用浓硫酸与乙醇混合加热制乙烯,加热一段时间后观察到烧瓶中有黑色物质出现,(Ⅱ)中经稀硫酸酸化的高猛酸钾溶液褪色。甲同学认为酸性高锰酸钾溶液褪色,能证明乙烯被酸性高锰酸钾溶液氧化了;乙同学认为酸性高锰酸钾溶液褪色,不能证明乙烯被酸性高锰酸钾溶液氧化了。
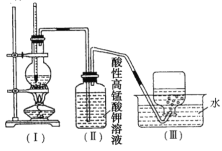
(1)____________(填“甲”或“乙”)同学的观点正确,理由是_________(填序号)。
A.(Ⅱ)中酸性高锰酸钾溶液褪色,能证明乙烯发生了氧化反应
B.(Ⅱ)中酸性高锰酸钾溶液褪色,能证明乙烯发生了加成反应
C.(Ⅱ)中酸性高锰酸钾溶液褪色,不能证明通入的气体是纯净物
D.(Ⅱ)中酸性高锰酸钾溶液褪色,只能证明通入的气体一定具有还原性
(2)丙同学取(Ⅱ)中少量溶液于试管中,加入盐酸和氯化钡溶液,产生白色沉淀,据此他认为乙烯中一定混有二氧化硫,他的结论____(填“合理”或“不合理”),理由是________。若你认为不合理,请改进上述实验方案,验证乙烯中是否含有![]() ______。
______。
(3)丁同学对上述实验方案进行了适当改进,用于验证乙烯能否发生加成反应,则他的改进方法可能是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某高聚物![]() 是一种工业增塑剂,其合成路线如图所示:
是一种工业增塑剂,其合成路线如图所示:
![]()
已知![]() 的苯环上只有一个侧链,且侧链上有两种不同化学环境的氢原子;
的苯环上只有一个侧链,且侧链上有两种不同化学环境的氢原子;![]() 是芳香烃。回答下列问题:
是芳香烃。回答下列问题:
(1)![]() 中含氧官能团的名称为__________,
中含氧官能团的名称为__________,![]() 的分子式为________,
的分子式为________,![]() 的反应条件为________,
的反应条件为________,![]() 的结构简式为_________________。
的结构简式为_________________。
(2)![]() 是与
是与![]() 含有相同官能团的同分异构体,相同条件下也能制得
含有相同官能团的同分异构体,相同条件下也能制得![]() ,写出由
,写出由![]() 生成
生成![]() 的化学方程式:_______。
的化学方程式:_______。
(3)写出![]() 的化学方程式:_______。
的化学方程式:_______。
(4)![]() 的消去产物
的消去产物![]() 是一种药物中间体,下列关于
是一种药物中间体,下列关于![]() 的叙述正确的是________(填序号)。
的叙述正确的是________(填序号)。
a.能发生取代、消去、氧化、加聚反应
b.等物质的量的![]() 与
与![]() 混合,在一定条件下发生酯化反应,生成物可能的分子式为
混合,在一定条件下发生酯化反应,生成物可能的分子式为![]()
c.1molH在一定条件下与![]() 反应,最多消耗
反应,最多消耗![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2,4,6-三硝基甲苯是一种淡黄色的烈性炸药,可由甲苯与浓硝酸和浓硫酸的混合物在加热条件下制取。其结构简式如图所示,下列有关说法不正确的是( )

A.2,4,6-三硝基甲苯的化学式为![]()
B.2,4,6-三硝基甲苯中氮元素的质量分数为18.5%
C.甲苯与浓硝酸和浓硫酸的混合物发生取代发应只可能有2,4,6-三硝基甲苯生成
D.2,4,6-三硝基甲苯的核磁共振氢谱中只有两组峰,且峰面积之比为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列8种物质:①甲烷,②苯,③聚乙烯,④二氧化硫,⑤2-丁炔,⑥环己烷,⑦环已烯,⑧对二甲苯。其中既能使酸性![]() 溶液褪色又能与溴水反应使之褪色的是( )
溶液褪色又能与溴水反应使之褪色的是( )
A.③④⑤⑧B.④⑤⑦⑧C.③④⑤⑦⑧D.④⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案能达到相应实验目的的是( )
选项 | 实验目的 | 实验方案 |
A | 检验溴乙烷中的溴原子 | 加入 |
B | 检验溴乙烷发生了消去反应 | 加 |
C | 除去溴苯中的溴 | 用 |
D | 确定乙醇分子的结构 | 通过质谱仪进行质谱分析 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧是地壳中含量最多的元素,氮是空气中含量最多的元素。
(1)![]() 中的O-H键、分子间的范德华力和氢键由强到弱的顺序依次为__________>__________>__________。
中的O-H键、分子间的范德华力和氢键由强到弱的顺序依次为__________>__________>__________。
(2)![]() 的沸点高于
的沸点高于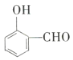 ,其原因是____________________。
,其原因是____________________。
(3)N、P、As都属于第ⅤA族元素,形成简单氢化物的沸点由高到低的顺序为__________(填分子式,下同)>__________>__________。
(4)如图1表示某种含氮有机化合物的结构简式,其分子内4个氮原子分别位于正四面体的4个顶点(见图2)。分子内存在空腔,能嵌入某种离子或分子并形成4个氢键予以识别。

下列分子或离子中,能被该有机化合物识别的是__________(填标号)。
a.![]() b.
b.![]() c.
c.![]() d.
d.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d、e、f为元素周期表前四周期元素,且原子序数依次增大。a原子核内无中子;在考古行业中,元素b的一种核素常用来鉴定一些文物的年代;d原子核外电子有8种不同的运动状态;e为第四周期元素,其基态原子的价电子排布式中成对电子的电子对数与单电子数相等,且每个原子轨道中都有电子;f元素的基态原子最外能层只有1个电子,且其他能层均已充满电子。回答下列问题:
(1)六种元素中电负性最大的是__(填元素符号),其中e原子的价电子排布式为__。
(2)b有多种同素异形体,其中硬度最大的是___(填名称);写出一种属于分子晶体的b的同素异形体的化学式__。
(3)a、c形成的简单分子的化学式为___,分子中c原子的杂化类型为__,分子立体构型为___。
(4)六种元素中其中有两种元素形成的化合物___(填化学式)与c的单质互为等电子体。
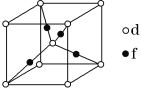
(5)元素d与f形成的一种化合物的晶胞结构如图所示,其中黑球在两个白球连线的中点。该化合物的化学式为__;若相邻d原子和f原子间的距离为acm,阿伏加德罗常数的值为NA,则该晶体的密度为__g·cm-3(用含a、NA的式子表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com