
| A.强酸性溶液中:Na+、、Mg3+、Cl-、AlO2- |
| B.含有0.5 mol·L-1 Al3+的溶液中:K+、Cl-、CO32-、NO-3 |
| C.含有0.5 mol·L-1 Ca2+的溶液中:Na+、K+、HCO3-、Cl- |
| D.室温下,pH=13的溶液中:Na+、K3+、NO-3、HCO3- |
科目:高中化学 来源:不详 题型:填空题
 和
和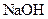 溶液等体积混合,混合前两种溶液的浓度和混合后所得溶液的
溶液等体积混合,混合前两种溶液的浓度和混合后所得溶液的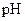 如下表(设混合后溶液体积变化忽略不计):
如下表(设混合后溶液体积变化忽略不计):| 实验编号 |  物质的量浓度 物质的量浓度( 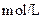 ) ) | 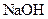 物质的量浓度 物质的量浓度( 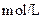 ) ) | 混合溶液的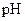 |
| 甲 | 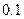 | 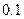 | 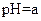 |
| 乙 | 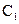 | 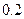 | 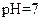 |
| 丙 | 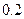 | 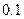 | 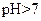 |
| 丁 | 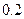 | 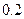 | 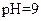 |
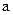 的取值范围为 。
的取值范围为 。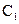 是否一定等于
是否一定等于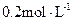 (选填“是”或“否”)。若
(选填“是”或“否”)。若 为弱酸,计算出该混合溶液达平衡时
为弱酸,计算出该混合溶液达平衡时 电离常数
电离常数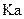 的近似值是 (用含
的近似值是 (用含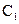 代数式表示)。
代数式表示)。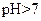 的原因是 ,该组混合溶液中离子浓度的大小关系是 。
的原因是 ,该组混合溶液中离子浓度的大小关系是 。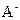 在该条件下的水解度是 ,该溶液中,水电离出的
在该条件下的水解度是 ,该溶液中,水电离出的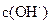 是
是 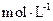 。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
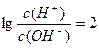 .有关反应后该混合溶液的叙述正确的是
.有关反应后该混合溶液的叙述正确的是| A.上述反应对应的离子方程式为2ClO-+CO2+H2O=2HClO+CO32- |
| B.上述溶液中:c(ClO-)>c(HCO3-)>c(CO32-) |
| C.上述溶液中:c(ClO-)+c(HClO)=c(HCO3-)+c(CO32-)+c(H2CO3) |
| D.上述溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(ClO-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.K+、Na+、OH-、 Cl- | B.Cu2+、Ba2+、NO3-、Cl- |
| C.Na+、Mg2+、OH-、SO42- | D.Ba2+、H+、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
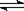 Ca2+(aq)+2OH-(aq),现向其中加入少量CaO粉末,则下列说法错误的是:
Ca2+(aq)+2OH-(aq),现向其中加入少量CaO粉末,则下列说法错误的是:| A.析出固体的质量增加 | B.溶液的pH值不变 |
| C.溶液中的OH-数目减少 | D.溶液中的Ca2+浓度减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下pH=7的溶液中:Fe3+、Na+、Cl-、N03- |
| B.常温下c(OH-)/c(H+)=1014的溶液中:K+、Mg2+、Cl-、Br- |
| C.含有大量HC03-的澄清透明溶液中:K+、C6H5O-、Cl-、Na+ |
| D.能与金属铝反应放出氢气的溶液中:K+、N03-、Cl-、Fe2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入铝粉有大量氢气产生的溶液中:Ca2+、K+、NO3-、C1- |
| B.PH = 0的无色溶液中:Na+、K+、MnO4-、NO3- |
| C.在0.1mol/L的醋酸溶液中:Fe2+、Na+、ClO-、Ca2+ |
| D.在c(OH-)= 1×10-13的溶液中:NH4+、Ca2+、C1-、K+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.无色溶液:Cu2+、K+、MnO4-、SO42- |
| B.能溶解Al2O3的溶液:Na+、Ca2+、HCO3-、NO3- |
| C.c(OH-)=1×10-13mol·L-1的溶液:NH4+、Al3+、SO42-、Cl- |
| D.含0.1 mol·L-1 NO3-的溶液:H+、Fe2+、Mg2+、Br- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将纯水加热至较高温度,水的离子积变大,pH变小,呈中性 |
| B.氨水和盐酸混合后溶液呈酸性,溶液中离子浓度大小关系一定存在:c(NH4+)>c(H+) |
| C.相同温度下,pH=2的醋酸溶液与pH=2的盐酸中c(H+)之比为1:l |
| D.向盛有少量Mg(OH)2沉淀的试管中加入NH4Cl浓溶液,振荡,沉淀会逐渐溶解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com