
| A. | 自然界中含有大量游离态的硅,纯净的硅晶体可用于制作计算机芯片 | |
| B. | Si、P、S、Cl相应的氧化物对应水化物的酸性依次增强 | |
| C. | 工业上通常用电解熔融氧化铝制得金属铝 | |
| D. | 金属铝、铁、铜都有一定的抗腐蚀性能,其抗腐蚀的原因都是表面形成氧化物薄膜,阻止反应的进一步发生 |
分析 A.Si是亲氧元素,极易被氧气氧化生成二氧化硅;
B.元素的非金属性越强,其最高价氧化物的水化物酸性越强;
C.铝属于较活泼金属,工业上采用电解熔融氧化铝的方法冶炼;
D.Fe的金属氧化物较疏松,且Cu、Fe在潮湿的空气中易生锈.
解答 解:A.Si是亲氧元素,极易被氧气氧化生成二氧化硅,在自然界中以二氧化硅和硅酸盐形式存在,故A错误;
B.元素的非金属性越强,其最高价氧化物的水化物酸性越强,但其氧化物的水化物酸性不一定强,如酸性:H2SO3>HClO,故B错误;
C.铝属于较活泼金属,熔融氯化铝不导电,所以工业上采用电解熔融氧化铝的方法冶炼,故C正确;
D.Fe、Cu在潮湿的空气中易生锈,Al属于亲氧元素,易被氧化生成致密的氧化物薄膜氧化铝而阻止进一步被氧化,所以金属铝有一定的抗腐蚀性能,而铁、铜露置于空气中容易与氧气进一步反应,抗腐蚀性能不强,故D错误;
故选C.
点评 本题考查金属冶炼、元素周期律、硅的性质等知识点,侧重考查元素化合物知识,明确物质性质及元素周期律即可解答,知道金属活泼性强弱与冶炼方法的关系,易错选项是BC.


科目:高中化学 来源: 题型:选择题
| A. | 2甲基丙烷的二氯代产物有2种(不考虑立体异构) | |
| B. | C8H10中只有3种属于芳香烃的同分异构体 | |
| C. | 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种 | |
| D. | CH3CH2CH2CH3光照下与氯气反应,只生成1种一氯代烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +4价氧化物都能与氢氧化钠溶液反应 | |
| B. | 单质在加热时都能与氧气反应 | |
| C. | 氧化物都能溶于水生成相应的酸 | |
| D. | 碳和硅两种元素都有能导电的单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某期刊封面上有如下一个分子的球棍模型图,图中“棍”代表单键或双键或三键.不同颜色的球代表不同元素的原子,其中绿球代表( )元素.
某期刊封面上有如下一个分子的球棍模型图,图中“棍”代表单键或双键或三键.不同颜色的球代表不同元素的原子,其中绿球代表( )元素.| A. | 氮 | B. | 氢 | C. | 氧 | D. | 碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=4的NaHSO3溶液中:c(SO32-)<c(H2SO3) | |
| B. | pH=3的氯化铵溶液与pH=3的盐酸中水的电离程度相同 | |
| C. | 将pH=5的醋酸溶液稀释后,所有离子浓度均减小,pH增大 | |
| D. | 向NH4HSO4溶液中加入等物质的量的NaOH形成的溶液中:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸与Fe(OH)3反应:Fe(OH)3+3H+═Fe3++3H2O | |
| B. | 稀硫酸与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO${\;}_{4}^{2-}$═BaSO4↓ | |
| D. | Fe3O4与盐酸反应:Fe3O4+8H+═3Fe3++4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
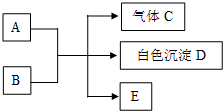
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO32-和HCO3- | B. | CO32-,HCO3-和S2- | ||
| C. | CO32-,HCO3-,S2-,CH3COO- | D. | 全部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com