
 一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )| A. | NaCl是非电解质 | |
| B. | NaCl溶液是电解质 | |
| C. | NaCl在水溶液中电离出了可以自由移动的离子 | |
| D. | 固体NaCl中没有离子 |
分析 根据原电池的工作原理和构成条件:电解质溶液必须含有大量自由移动离子,电解质中阴阳离子的定向移动形成电流,在水溶液里或熔融状态下能导电的化合物是电解质,在水溶液和熔融状态下都不导电的化合物是非电解质,含有自由移动的离子或电子的物质能导电,据此分析解答.
解答 解:A.NaCl晶体中不含自由移动的阴阳离子或电子,所以不导电,但NaCl在熔融状态下能导电,所以属于电解质,故A错误;
B.氯化钠溶液含有自由移动的离子,所以能得电子,但NaCl溶液是混合物,既不是电解质也不是非电解质,故B错误;
C.NaCl在水溶液中电离出了可以自由移动的离子,所以NaCl溶液能导电,故C正确;
D.氯化钠固体中的钠离子和氯离子不能自由移动,在水分子的作用下电离出阴阳离子,故D错误;
故选C.
点评 本题考查电解质、非电解质的判断,侧重考查对概念的理解,注意概念中的关键词,注意二者的区别,注意:单质和混合物既不是电解质也不是非电解质,为易错点,题目较简单.


 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:解答题
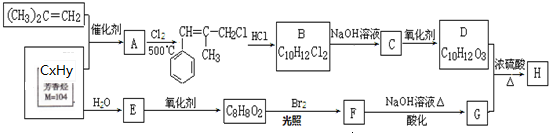
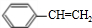
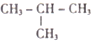 合成(CH3)2C=CH2的路线为:
合成(CH3)2C=CH2的路线为: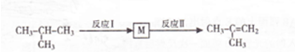 ,反应Ⅰ的条件为光照,写出反应Ⅱ的化学方程式
,反应Ⅰ的条件为光照,写出反应Ⅱ的化学方程式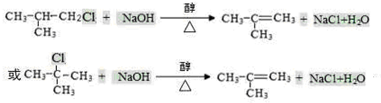
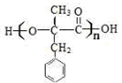
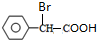 +2NaOH $→_{△}^{水}$
+2NaOH $→_{△}^{水}$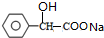 +NaBr+H2O
+NaBr+H2O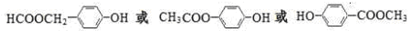 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,向20.00mL0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol•L-1的NaOH溶液,pH随NaOH溶液体积的变化如图所示.下列说法不正确的是( )
常温下,向20.00mL0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol•L-1的NaOH溶液,pH随NaOH溶液体积的变化如图所示.下列说法不正确的是( )| A. | 在反应过程中,c(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| B. | pH=5时,c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | pH=6时,c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1000 mol•Lˉ1 | |
| D. | pH=7时,消耗NaOH溶液的体积小于20.00mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
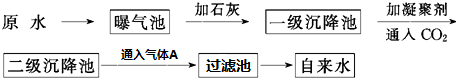
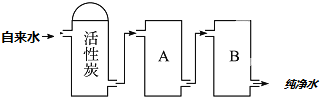
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的 O2和O3在相同条件下所占的体积相同 | |
| B. | 电解精炼铜时,若转移6.02X1023个电子,则阳极溶解32g铜 | |
| C. | 1molCl2溶于足量水中,转移的电子数为NA | |
| D. | 2L0.2mol•L-1硝酸与适量铁恰好完全反应(还原产物为NO),生成NO的分子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
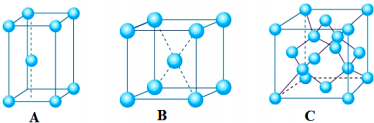
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 观察K2SO4溶液的颜色 | |
| B. | 加水稀释CuSO4溶液,溶液颜色变浅 | |
| C. | 向CuSO4溶液中滴加过量NaOH溶液,振荡后静置,溶液变成无色 | |
| D. | 向CuSO4溶液中滴加过量Ba(NO3)2溶液,振荡后静置,溶液未变成无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com