
【题目】现有以异丁烯为原料合成某二酸的合成路线如下:

已知:R-CH2CN![]() R-CH2COONa+NH3
R-CH2COONa+NH3
(1)A的系统命名是_______________,B的官能团名称是_______________________。
(2)步骤③的反应类型是____________________________。
(3) 同一有机物中的两个同种官能团在反应时,一者参与反应占绝大多数,另一者几乎不反应,这被称之为“位置专一性”。请从反应物结构角度,简要解释步骤②中消去氯原子时的位置专一性:______________________________。
(4)步骤⑤的产物C经酸化后,可发生分子内酯化,写出该内酯的结构简式______________________。
(5)写出步骤⑥的化学方程式___________________________________。
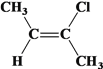
(6)均符合下列条件B的同分异构体有________个。
a.所有碳原子一定共平面; b.核磁共振氢谱有3 组峰。
(7)利用题目给的信息,写出由异丁烯为原料,两步合成 的路线流程______。
的路线流程______。
【答案】 2-甲基-1,2-二氯丙烷 碳碳双键、氯原子 取代反应 因为A物质中有一个Cl-官能团邻位无H原子,故它不易消去HCl而反应 ![]() 2CH2=C(CH2OH)CH2COOH + O2
2CH2=C(CH2OH)CH2COOH + O2 ![]() 2H2O + 2CH2=C(CHO)CH2COOH 3
2H2O + 2CH2=C(CHO)CH2COOH 3 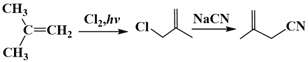
【解析】考查有机物的推断和合成,(1)根据CH2=C(CH3)2,推出反应①的类型为加成反应,即A的结构简式为CH2ClCCl(CH3)2,A的命名为2-甲基-1,2-二氯丙烷;A→B发生消去反应,根据反应③的产物,推出B的结构简式为CH2=C(CH3)CH2Cl,含有的官能团是碳碳双键和氯原子;(2)步骤③应是CN-取代氯原子位置,此反应属于取代反应;(3)因为A物质中有一个Cl官能团邻位无H原子,故它不易消去HCl而反应;(4)根据信息,C的结构简式为CH2=C(CH2Cl)CH2CN,C的结构简式为CH2=C(CH2OH)CH2COONa,C经酸化后得出物质为CH2=C(CH2OH)CH2COOH,通过酯化反应生成内酯,其结构简式为![]() ;(5)反应⑥为氧化反应,羟基被氧化成醛,即反应⑥化学方程式为 2CH2=C(CH2OH)CH2COOH + O2
;(5)反应⑥为氧化反应,羟基被氧化成醛,即反应⑥化学方程式为 2CH2=C(CH2OH)CH2COOH + O2 ![]() 2H2O + 2CH2=C(CHO)CH2COOH;(6)所有碳原子一定共面,根据乙烯空间构型为平面进行判断,有3组峰,说明有3种不同的氢原子,符合条件的同分异构体是
2H2O + 2CH2=C(CHO)CH2COOH;(6)所有碳原子一定共面,根据乙烯空间构型为平面进行判断,有3组峰,说明有3种不同的氢原子,符合条件的同分异构体是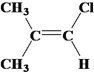 、
、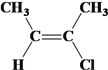 、
、 ;(7)异丁烯结构简式为CH2=C(CH3)2,然后与氯气发生取代反应,然后与NaCN发生取代反应,即合成路线:
;(7)异丁烯结构简式为CH2=C(CH3)2,然后与氯气发生取代反应,然后与NaCN发生取代反应,即合成路线: 。
。


科目:高中化学 来源: 题型:
【题目】如图所示,“二氧化碳是否在有水存在时,才能与过氧化钠反应?”这个问题可通过以下实验加以证明。

(1)按图装置,在干燥的试管Ⅲ中装入Na2O2后,在通入CO2之前,应事先将活塞(K1、K2)关闭好,目的何在?____。
(2)试管I内的试剂X是__时,打开活塞K1、K2,加热试管Ⅲ约5分钟后,将带火星的小木条插入试管Ⅱ的液面上,可观察到带火星的小木条不能剧烈地燃烧起来,且Ⅲ内淡黄色粉末未发生变化,则所得的结论是____。
(3)试管I内试剂为CO2饱和水溶液时,其他操作同(2),通过____的现象,可以证明Na2O2与潮湿的CO2能反应且放出O2。
(4)CO2与过氧化钠反应机理也可用示踪原子分析加以证明,请完成下列反应方程式:
__Na2O2+____C18O2+____H218O→____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素性质的递变情况错误的是( )
A. Na、Mg、Al原子最外层电子数依次增多
B. P、S、Cl元素最高正价依次升高
C. N、O、F第一电离能依次增大
D. Na、K、Rb电负性逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制100mL 0.50 mol·L-1 NaOH溶液时,必须用到的仪器是
A.100mL容量瓶B.100mL集气瓶C.100mL烧瓶D.100mL滴瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素性质的递变情况错误的是 ( )
A. Li、Be、B原子最外层电子数依次增多
B. P、S、Cl元素最高正价依次升高
C. N、O、F电负性依次增大
D. Na、K、Rb第一电离能逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素原子的价电子排布式是3s23p4,则它在周期表中的位置是 ( )
A. 第二周期第ⅣA族 B. 第三周期第ⅣA族
C. 第四周期第ⅡA族 D. 第三周期第ⅥA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘及其化合物主要用于医药、照相及染料等。碘是合成碘化物的基本原料。
(一) 实验室测定KI溶液中I-的含量
量取25.00mLKI溶液溶液于250mL锥形瓶中,分别加入少量稀H2SO4和稍过量的NH4Fe(SO4)2·12H2O溶液,摇匀。小火加热蒸发至碘完全升华,取下锥形瓶冷却后,加入稀H2SO4,再加入几滴二苯胺磺酸钠(用作指示剂,被强氧化剂氧化为紫色),用0.0250mol·L-1标准K2Cr2O7溶液进行滴定至终点。重复3次,平均每次消耗K2Cr2O7溶液20.00mL(已知反应:①2Fe3++2I-=2Fe2++I2 ②6Fe2++Cr2O72-+14H+==6Fe3++2Cr3++7H2O
(1)在滴定过程中,下列操作(其他操作正确)会造成测定结果有误差的是_________________。
A.终点读数时俯视读数,滴定前平视读数
B.锥形瓶水洗后未干燥
C.滴定管未用标准K2Cr2O7溶液润洗
D.盛标准K2Cr2O7溶液的滴定管,滴定前有气泡,滴定后无气泡
(2)该实验达到滴定终点时,现象为__________________。
(3)根据滴定有关数据,该KI溶液中I-含量是________g·L-1。
(二) 某实验小组认为氧气可以氧化KI 溶液中的I-,其做了下列实验探究影响该反应的因素。
实验 | 气体a | 编号及现象 |
| 空气(含HCl) | Ⅰ.溶液迅速呈黄色 |
空气(含CO2) | Ⅱ.长时间后,溶液呈很浅的黄色 | |
空气 | Ⅲ.长时间后,溶液无明显变化 |
(4)装置A (含导管)的名称为_________________。
(5)通入a为空气(含HCl)时,发生反应的离子方程式为______________________。
(6)实验Ⅲ的作用是________________________。
(7)用CCl4萃取Ⅰ、Ⅱ、Ⅲ的溶液,萃取后下层溶液的颜色均无色。取萃取后上层溶液,用淀粉检验:Ⅰ、Ⅱ的溶液变蓝;Ⅲ的溶液未变蓝。溶液变蓝说明Ⅰ、Ⅱ中生成了__________________________。
(8)查阅资料: I2易溶于KI 溶液。下列实验证实了该结论并解释Ⅰ、Ⅱ的萃取现象。

现象X是_____。用KI萃取Ⅰ、Ⅱ的溶液,萃取后下层溶液颜色均无色的原因是_________________。
(9)综合实验证据说明影响I-被氧化的因素及对应关系:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用Na2SO4溶液沉淀Ba2+、Pb2+、Ca2+三种金属离子(M2+),所需SO42-最低浓度的对数值p(SO42-)=-lgc(SO42-)与p(M2+)=-lgc(M2+)关系如图所示。下列说法正确的是

A. KSP(CaSO4)<KSP(PbSO4)<KSP(BaSO4)
B. a点可表示CaSO4的饱和溶液,且c(Ca2+)=c(SO42-)
C. b点可表示PbSO4的不饱和溶液,且c(Pb2+)<c(SO42-)
D. 向Ba2+浓度为10-5mol·L-1的废水中加入CaSO4粉末,会有BaSO4沉淀析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
2Zn(s)+O2(g)=2ZnO(s) △H1
4Ag(s)+O2(g)=2Ag2O(S) △H2
则Zn(s)+Ag2O(s)=2Ag(s)+ZnO(s),△H值为
A. △H2-△H1 B. △H2+△H1 C. ![]() (△H1-△H2) D.
(△H1-△H2) D. ![]() (△H2-△H1)
(△H2-△H1)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com