
| A. | OF2(F显正价) | B. | CN-(N显正价) | C. | NH2-(H显正价) | D. | SiC (C显正价) |
科目:高中化学 来源: 题型:选择题
| A. | 苯与浓溴水反应制溴苯 | |
| B. | 在浓溴水中加几滴苯酚观察到白色沉淀 | |
| C. | 将乙醛滴入银氨溶液中制银镜 | |
| D. | 1mol/L CuSO4溶液2mL和0.5mol/L NaOH溶液4mL混合后加入40%乙醛溶液0.5mL,加热煮沸观察沉淀颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同体积的CO和CO2 | B. | 同温同压下,1L CO和1L CO2 | ||
| C. | 常温常压下,1g CO和1g N2 | D. | 在0℃时,同压下等体积的CO2和H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
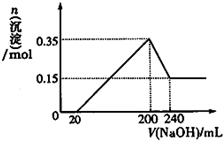 A、B、C、D均为中学化学中常见的物质,它们之间转化关系如图(部分产物已略去):A$→_{一定条件}^{+D}$B$→_{一定条件}^{+D}$C
A、B、C、D均为中学化学中常见的物质,它们之间转化关系如图(部分产物已略去):A$→_{一定条件}^{+D}$B$→_{一定条件}^{+D}$C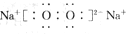
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑦ | B. | ②③④⑤ | C. | ③④⑥⑦ | D. | ①③⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
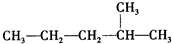 :2-甲基戊烷;CH2=CHCH2CH3:1-丁烯;
:2-甲基戊烷;CH2=CHCH2CH3:1-丁烯;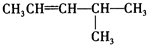 :4-甲基-2-戊烯;
:4-甲基-2-戊烯; 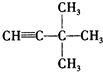 :3,3-二甲基-1-丁炔;
:3,3-二甲基-1-丁炔;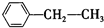 :乙苯;
:乙苯;| 2,3-二甲基丁烷 | 3,4,4-三甲基-1-戊炔 | 3,5-二甲基-2-己烯 |
| CH3CH(CH3)CH(CH3)CH3 | CH≡C-CH(CH3)C(CH3)2CH3 | CH3CH=C(CH3)CH2CH(CH3)CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
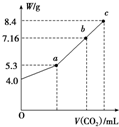 钠有多种化合物,如氧化钠、过氧化钠、氢氧化钠、碳酸钠、碳酸氢钠,这些物质在实际生活中有广泛的应用,在一定条件下相互间能进行转化.
钠有多种化合物,如氧化钠、过氧化钠、氢氧化钠、碳酸钠、碳酸氢钠,这些物质在实际生活中有广泛的应用,在一定条件下相互间能进行转化.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com